技术摘要:
本发明提出了一种α‑半乳糖抗原活性前体及其合成方法和应用。本发明的合成方法包括以下步骤:在化合物I中加入尿苷二磷酸葡萄糖、可溶性镁盐和Tris‑HCl缓冲液,配制成水溶液;在水溶液中添加UDP‑葡萄糖‑4‑差向异构酶和α‑1,3‑半乳糖基转移酶,反应,得初产物;在 全部
背景技术:
单克隆抗体药物在生物制药行业占据重要的地位,在全球市场中,抗体药物正成 为国际制药业争夺的焦点。在这类抗体药物中,利妥昔单抗和曲妥珠单抗为代表的治疗性 单抗药物的开发和应用成为肿瘤分子靶向治疗领域最为成功的代表。这类单抗药物以肿瘤 靶向抗原作为分子靶标,通过与抗原结合,介导补体依赖的细胞毒性作用,抗体依赖的细胞 毒性等多种机制杀伤癌细胞。在单抗药物杀伤癌细胞的过程中,选择合适的靶向抗原是成 功设计和开发肿瘤治疗性单抗的前提和关键。 α-半乳糖抗原活性前体(英文简称α-gal)是广泛存在于猪、牛、鼠等非灵长类哺乳 动物体内的一类碳水化合物表位,然而,人体α- 1 ,3半乳糖基转移酶 (α- 1 , 3Galactosyltransferase,α-1,3GT)基因功能失活而不表达α-半乳糖基 (α-galactosyl, α-gal)表位,但是,天然存在着大量抗α-gal抗体;异种器官移植研究结果提示,在人肿瘤细 胞上重新表达异种移植抗原α-gal,可能诱发类似于宿主抗移植物超急性排斥反应的抗肿 瘤效应。 志贺样毒素又称为VT毒素(vero toxin,VT),O157:H7大肠埃希菌产生志贺样毒 素。1982年发现以来,O157:H7大肠埃希菌感染的发病率在发达国家呈上升趋势。1996年5月 至8月间,在日本发生了一次世界上最大的暴发流行, 10 000余人感染,近10人死亡,受到 了全世界的关注。而α-半乳糖抗原活性前体对志贺样毒素具有抑制作用,有望作为先导分 子发展成为高灵敏性的诊断试剂,用以早期诊断志贺毒素产生菌感染。 目前,现有技术中α-半乳糖抗原活性前体大多采用纯化学合成的方式来制备,具 体地,先将寡糖链用化学合成的方式制备出来,然后,通过化学偶连法将保护的寡糖分子和 连接分子进行偶连,最后,再将连接分子的末端转化为活化基团。这种化学方法合成α-半乳 糖抗原活性前体的过程中需要涉及繁琐官能团的保护以及脱官能团保护的操作,工艺路线 长,分离困难,产率低,不利于实现工业化生产。
技术实现要素:
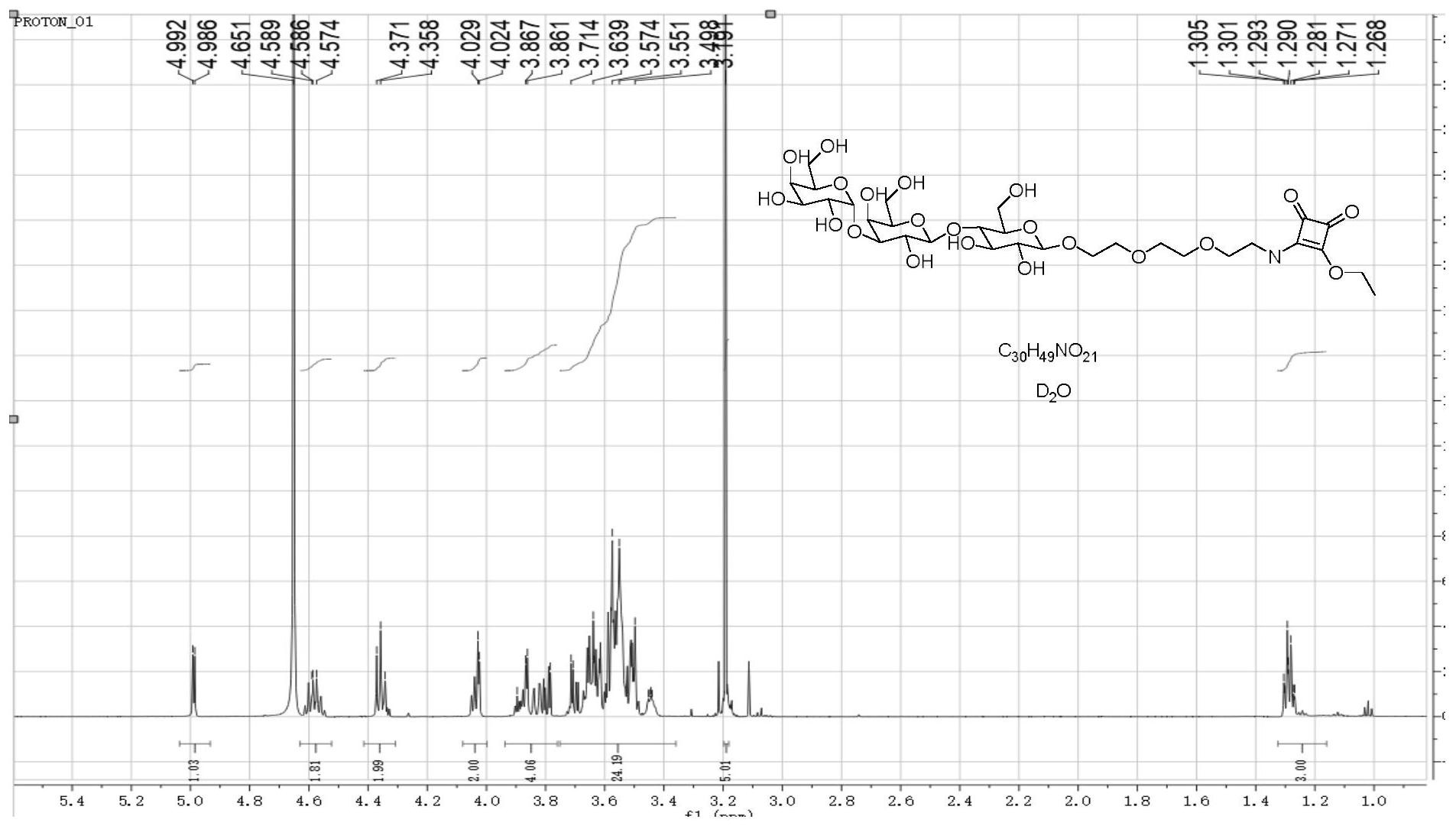
本发明提出一种α-半乳糖抗原活性前体及其合成方法和应用,旨在解决了现有技 术中在化学方法合成α-半乳糖抗原活性前体的过程中存在繁琐的官能团保护和脱官能团 操作而导致其工艺路线长、分离困难和产率低的问题。 为了解决上述技术问题,本发明的技术方案是这样实现的: 在一个方面,本发明的一种α-半乳糖抗原活性前体的合成方法,包括以下步骤: 1)取结构式为式I的化合物I,加入尿苷二磷酸葡萄糖、可溶性镁和Tris-HCl 缓冲 液,配制成水溶液;尿苷二磷酸葡萄糖与化合物I的摩尔比为1.3-3.0:1,可溶性镁与化合物 5 CN 111593080 A 说 明 书 2/9 页 I的摩尔比为10-30:1,Tris-HCl缓冲液与化合物I的摩尔比为 20-40:1,Tris-HCl缓冲液的 pH值为5-9; R为羟基、氨基、醋酰胺基、三氟乙酰氨基,n为自然数,取值为1-10; 2)在所述水溶液中,添加UDP-葡萄糖-4-差向异构酶和α-1 ,3-半乳糖基转移酶, UDP-葡萄糖-4-差向异构酶的添加量为0.3-3.0%,α-1,3-半乳糖基转移酶的添加量为0.2- 2.0%,在15-40℃下,反应5-100h,得初产物; 3)将所述初产物的pH值调节至6.5-9.0,添加β-半乳糖苷酶,β-半乳糖苷酶的添加 量为0.5-5.0%,在20-40℃下,反应1-24h,纯化,得结构式为式II的化合物II; 4)取所述化合物II,溶解于有机溶剂中,添加催化剂,并在氢气条件下,室温反应 20-30h,过滤,浓缩,得化合物III,结构式如式III的化合物III; 5)取所述化合物III,溶解于有机溶剂中,得溶液A,采用有机碱,使溶液 A的pH值 调节至7-9,将型酸二乙酯添加至溶液A中,并在室温下搅拌反应10-20h,浓缩,纯化,得α-半 乳糖抗原活性前体,α-半乳糖抗原活性前体的结构式如式IV; 本发明的α-半乳糖抗原活性前体的合成方法中,首先,在α-1 ,3-半乳糖基转移酶 的催化作用下,将糖链延长;其中,尿苷二磷酸葡萄糖(UDP-glucose)在 UDP-葡萄糖-4-差 向异构酶(GalE)的作用下差向异构化为尿苷二磷酸半乳糖 (UDP-galactose),也可以直接 使用尿苷二磷酸半乳糖(UDP-galactose);然后,通过化学反应方法与方型酸二乙酯反应转 6 CN 111593080 A 说 明 书 3/9 页 化为活性前体。本发明通过酶法和化学法的有机结合,集成了化学法的结构普适性和酶法 的高效专一性,可以高效的合成α-半乳糖抗原活性前体及其衍生物,该合成方法具有很强 的普适性,这种合成方法工艺流程短,操作简单,分离方便,产率高,易于实现产业化;该抗 原活性前体对志贺样毒素具有抑制作用,可用于志贺样毒素检测试剂盒。 作为一种优选的实施方案,所述步骤3)中,纯化之前,还需要在反应液中加入与反 应液等体积的无水乙醇,孵育20-60min,无水乙醇的温度为2-6℃,孵育的温度为2-6℃。本 发明在酶法延长糖链的过程中,采用β-半乳糖苷酶(LacZ) 将未反应的二糖水解除掉,以提 高糖的纯度。 作为一种优选的实施方案,所述步骤4)中,有机溶剂为甲醇,催化剂为钯碳,钯碳 中钯的质量百分含量为10%,钯碳与化合物II的质量比为0.01-0.1:1。利用钯碳催化剂对 三糖化合物的末端进行加氢,这种方法操作方便,易于实现产业化。 作为一种优选的实施方案,所述步骤5)中,溶液A所用的有机溶剂为水和乙醇的混 合液,水和乙醇的体积比为2:1;所述有机碱为二乙胺、三乙胺、季胺、苯胺、苄胺中的任意一 种。本发明中化合物III与方型酸二乙酯均在溶液中进行反应,反应易于控制,还提高了反 应速度。 作为一种优选的实施方案,所述化合物I的制备方法为: S1:以结构式如式V的化合物V为原料,在羧酸酐和羧酸钠的作用下,于 135-140℃ 下,回流反应4-8h,使化合物V中羟基被保护,得结构式如式VI的化合物VI; S2:取步骤S1所得的化合物VI,溶解于有机溶剂中,添加对甲苯硫酚,在催化剂的 作用下,于室温下,反应2-4h,得结构式如式VII的化合物VII; 7 CN 111593080 A 说 明 书 4/9 页 S3:取步骤S2所得的化合物VII,溶解于有机溶剂中,添加多缩乙二醇叠氮,在催化 剂的作用下,于室温下,偶联反应0.5-1.5h,得结构式如式VIII的化合物VIII; S4:取步骤S3所得的化合物VIII,溶解于有机溶剂中,添加烷基醇钠,调节pH值为 9-10,于室温下进行取代反应,反应时间为10-20h,得化合物I。 本发明的化合物I采用化学法合成,充分发挥了化学的结构普适性,进一步提高了 α-半乳糖抗原活性前体及其衍生物的普适性。 作为一种优选的实施方案,所述步骤S1中,羧酸酐为醋酸酐,羧酸钠为醋酸钠。在 二糖的羟基保护过程中,以醋酸酐为保护,在醋酸钠的作用下,使反应充分进行,不会带来 额外杂质,提高了产品的纯度和收率。 作为一种优选的实施方案,所述步骤S2中,所用的有机溶剂为二氯甲烷,所用的催 化剂为三氟化硼乙醚。本发明中在二糖活性基团的取代过程中,采用二氯甲烷为有机溶剂, 采用三氟化硼乙醚为催化剂,反应速度快,效率高。 作为一种优选的实施方案,所述步骤S3中,所用的有机溶剂为二氯甲烷,所用的催 化剂为三氟甲磺酸银和四丁基碘化铵,三氟甲磺酸银和四丁基碘化铵的摩尔比为1:20-30; 优选地,所述步骤S4中,所用的有机溶剂为甲醇,所用的烷基醇钠为甲醇钠。本发明在二糖 与连接臂的偶联反应过程中,采用二氯甲烷为有机溶剂,采用三氟甲磺酸银和四丁基碘化 铵为催化剂,使连接臂分子准确有效地连接在二糖的活性取代基团上;同时,在化合物VIII 的脱保护过程中,在甲醇钠的保护作用下,使甲醇中的羟基与化合物VIII上的钠离子进行 取代反应,从而得到化合物I。 在另一个方面,本发明的一种α-半乳糖抗原活性前体,所述α-半乳糖抗原活性前 体是根据上面任意一项所述的α-半乳糖抗原活性前体的合成方法制备而成的。本发明的α- 半乳糖抗原活性前体具有很强的普适性,合成工艺流程短,操作简单,分离方便,产率高,易 于实现产业化。 在再一个方面,本发明的一种α-半乳糖抗原活性前体的应用,根据上面任意一项 所述的α-半乳糖抗原活性前体的合成方法制备而成的α-半乳糖抗原活性前体用于志贺样 毒素检测试剂盒。该抗原活性前体对志贺样毒素具有抑制作用,可用于志贺样毒素检测试 剂盒。 与现有技术相比,本发明的有益效果是:本发明的α-半乳糖抗原活性前体的合成 方法中,首先,在α-1,3-半乳糖基转移酶的催化作用下,将糖链延长;然后,通过化学反应方 法与方型酸二乙酯反应转化为活性前体;本发明通过酶法和化学法的有机结合,集成了化 学法的结构普适性和酶法的高效专一性,可以高效的合成α-半乳糖抗原活性前体及其衍生 物,该合成方法具有很强的普适性,这种合成方法工艺流程短,操作简单,分离方便,产率 高,易于实现产业化;该抗原活性前体对志贺样毒素具有抑制作用,可用于志贺样毒素检测 试剂盒。 8 CN 111593080 A 说 明 书 5/9 页 附图说明 图1为本发明所得α-半乳糖抗原活性前体的1H-NMR图; 图2为本发明所得α-半乳糖抗原活性前体的13C-NMR图; 图3为本发明所得α-半乳糖抗原活性前体的质谱图。












