技术摘要:
本发明公开一种治疗牙本质过敏的药物组合物及其制备方法、应用,属于牙骨质再生技术领域,该药物组合物包括药效学上有效量的两亲性寡肽,所述两亲性寡肽包括氨基酸序列为如SEQ ID No.1所示的亲水性肽和疏水性尾部,以及,药学上可接受的药物辅料;本发明使用模拟CEMP1 全部
背景技术:
牙本质过敏症(Dentine hypersensitivity,DH)是口腔科的常见病及多发病,DH 在普通人群中的患病率约为15-25%。DH可定义为对口腔环境中的刺激(如温度、化学物质、 渗透压和机械效应)做出反应的短暂而剧烈的疼痛或不适。DH的发生被认为是由于牙釉质、 表层牙本质和牙骨质的丧失而引起的深层牙本质的暴露。牙本质小管被牙冠部的牙釉质、 表层牙本质和牙根上的牙骨质覆盖和缠绕,保护深层牙本质免受外部刺激。患DH的患者在 服用刺激性食物时经常会感到疼痛或不适,因此在大多数情况下需要进行干预。 流体动力学理论是目前被广泛接受的DH发病机制。根据这一理论,牙本质小管中 的液体在外部刺激后双向流动并作用于暴露的深层牙本质,再反过来激活牙髓/牙本质边 界区域中的伤害感受器并引起疼痛。基于此,牙本质表面的釉质样和牙骨质样矿化结构的 重建是治疗牙本质过敏症的有效方法。牙本质硬组织的主要成分是磷灰石微晶,其形成和 生长主要由天然非胶原蛋白(NCPs)控制。例如,釉原蛋白在牙釉质的定向生长过程中起主 要的结构作用。牙本质磷蛋白(DPP)是牙本质细胞外基质中的主要非胶原蛋白之一,并被认 为在牙本质的矿化中起关键作用。牙骨质蛋白1(CEMP1)是仅在牙骨质中表达的组织特异性 蛋白,并且影响磷灰石微晶的成核、组成和形态,调控牙骨质的矿化这些天然的非胶原蛋白 由于含有许多带电荷的氨基酸,如天冬氨酸、谷氨酸和磷丝氨酸等。因此,这些非胶原蛋白 具有很高的阴离子特性,能够吸引钙离子来诱导生物矿化。而这些生物矿化过程能够在深 层牙本质表面构建一层无机矿物,保护牙本质牙髓免受外部刺激。然而,由于天然NCPs的提 取和纯化在不易获得,其在口腔临床中的广泛应用仍然有限。 仿天然非胶原蛋白的仿生寡肽类含有大量的功能性重复序列,如天冬氨酸、谷氨 酸和磷酸化丝氨酸,它们被认为是促进磷灰石微晶形成的关键。基于此,人们制造了不同种 类的多肽或寡肽来重建牙体硬组织结构。例如,一种模拟釉原蛋白的两亲性寡肽被用于釉 质样组织的重建。来源于DPP的天冬氨酸-丝氨酸-丝氨酸重复氨基酸序列已被证明能够诱 导矿化和封闭牙本质小管,因此在牙本质过敏症的治疗中具有应用潜能。
技术实现要素:
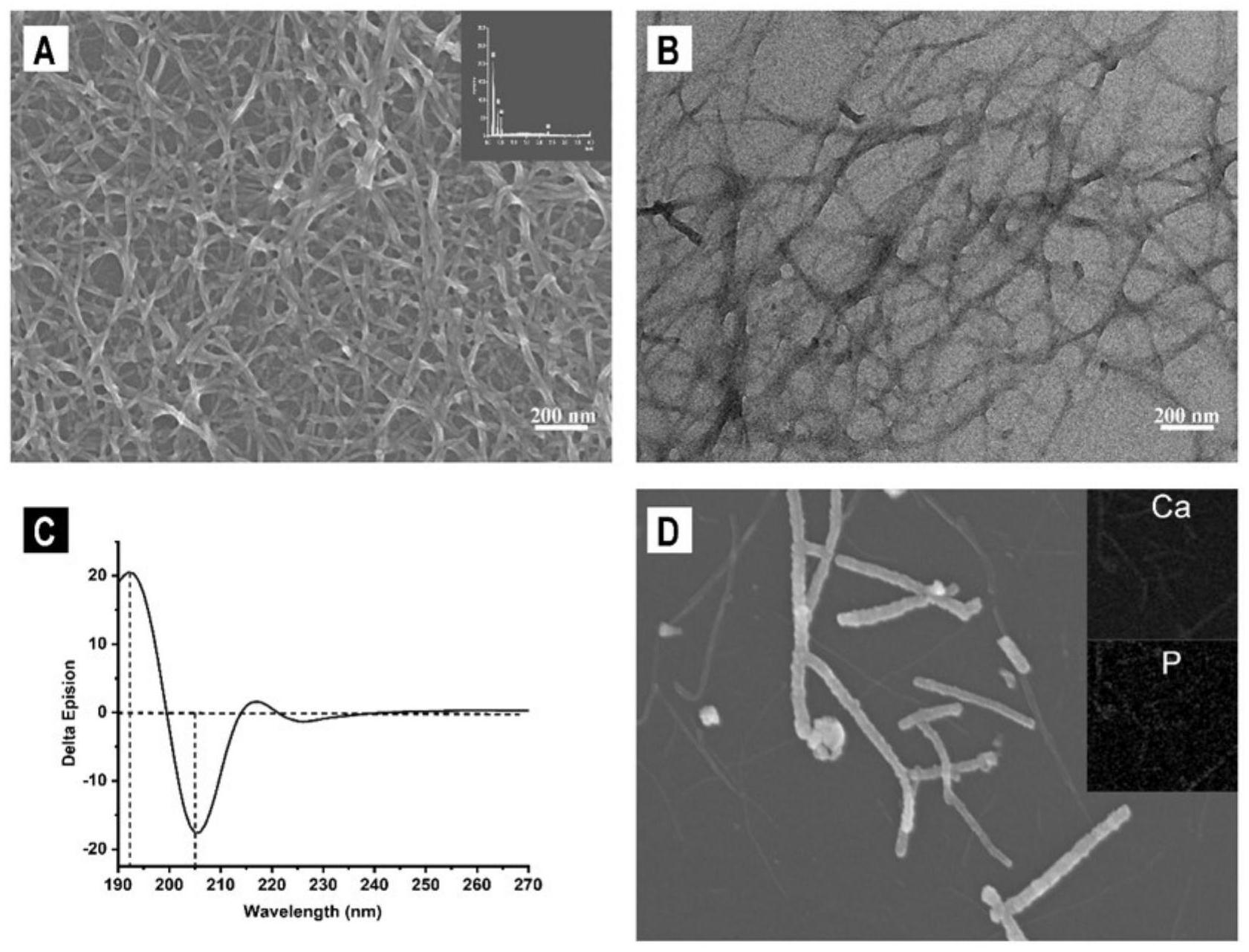
本发明的目的是提供一种治疗牙本质过敏的药物组合物及其制备方法、应用,以 解决上述现有技术存在的问题。 为实现上述目的,本发明提供了如下方案: 本发明提供一种药物组合物,包括: 药效学上有效量的两亲性寡肽,所述两亲性寡肽包括氨基酸序列为如SEQ ID No.1所示的亲水性肽和疏水性尾部;以及,药学上可接受的药物辅料。 3 CN 111544568 A 说 明 书 2/7 页 进一步地,所述疏水性尾部为硬脂酸衍生物。 进一步地,所述药学上可接受的药物辅料选自聚乙二醇、聚乳酸、聚乳酸-羟基乙 酸共聚物、聚乙烯吡咯烷酮、壳聚糖、葡聚糖、磷脂酰甘油。 本发明还提供一种上述的药物组合物的制备方法,包括以下步骤: (1)合成寡肽粉末 通过固相合成法合成,使用自动合成仪从C末端到N末端逐步进行; (2)两亲性寡肽的自组装 将寡肽粉末溶解在去离子水中,用1mol/L氯化钙溶液引发两亲性寡肽的自组装; (3)将步骤(2)的悬浮液超声混合,4℃孵育,得到自组装后的两亲性寡肽; (4)使药物辅料负载自组装后的两亲性寡肽。 本发明还提供一种上述的药物组合物在制备治疗/预防牙本质过敏的药物中的应 用。 本发明公开了以下技术效果: 本发明使用模拟CEMP1的寡肽在牙本质表面再生釉质样组织并封闭牙本质小管, 从而改善牙本质过敏症的治疗。自组装寡肽对酸蚀牙本质具有很强的结合能力,促进磷灰 石微晶的沉积和定向生长,从而在牙本质表面构建了一个釉质样结构。然后,再生的微晶在 牙本质小管内深度沉积,并确保牙本质小管的有效阻塞。因此,模拟CEMP1的两亲性寡肽在 未来牙本质过敏症的治疗中具有很大的应用潜力。 附图说明 为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例中所 需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本发明的一些实施 例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获 得其他的附图。 图1为两亲性寡肽的自组装特性,其中,A为自组装寡肽的扫描电镜图像,B为自组 装寡肽的透射电镜图像,C为自组装寡肽的圆二色谱结果,D为与无机钙和磷相互作用后的 自组装寡肽的扫描电镜图像和元素分布图; 图2为酸蚀牙本质的特征,其中,A为酸蚀牙本质的扫描电镜图像的表面视图,B为A 图的放大,C为酸蚀牙本质的扫描电镜图像的断面视图,D为酸蚀牙本质的能谱分析;白色箭 头为牙本质小管; 图3为自组装寡肽与酸蚀牙本质的结合能力,其中,A为自组装寡肽与酸蚀牙本质 结合的扫描电镜图像,B为A图的放大,C为两亲性寡肽粉的红外光谱分析,D为自组装寡肽与 酸蚀牙本质结合的红外光谱分析;黑色箭头为两亲性寡肽自组装形成的纳米纤维结构; 图4为寡肽诱导矿物质沉积,其中,A为一天内矿物沉积的扫描电镜图像的表面视 图,B为A图的放大,A1为A的断面视图,B1为B的断面视图,C为两天内矿物沉积的扫描电镜图 像的表面视图,D为C图的放大,C1为C的断面视图;D1为D的剖面图; 图5为寡肽在牙本质表面构建了釉质样组织,并诱导牙本质小管阻塞。其中,A为扫 描电镜图像的表面视图,B为A放大,C为能谱分析,D为A的断面视图,E为D放大,F为牙本质小 管阻塞图; 4 CN 111544568 A 说 明 书 3/7 页 图6为釉质样组织的XRD分析; 图7为自组装寡肽的细胞相容性,其中,A为自组装寡肽上的细胞增殖实验,B为实 验组光镜图像,C为对照组光镜图像。












