技术摘要:
本发明提供了一种miR‑122及其抑制剂在预防/治疗放射性脑损伤中的应,通过实验研究发现,miR‑122‑5p在照射后的小鼠海马及临床鼻咽癌放疗病人中的表达显著上调;而通过miR‑122干预后,在RBI动物模型中不仅能缓解神经炎症损伤,改善行为认知等;且体外细胞放射性损伤 全部
背景技术:
放射性脑损伤(Radiation-induced Brain Injury,RBI)是头颈部肿瘤尤其是鼻 咽癌(Nasopharyngeal Carcinoma,NPC)放射治疗下的主要剂量限制性不良事件,也是放射 治疗最为严重的并发症之一,从广义上来说,放射性脑损伤是放射治疗后神经细胞和颅内 血管受损后出现的一系列病理生理改变,可有影像学可见的脑部病灶。最常表现为广泛脑 水肿引起的进行性颅内压增高、脑疝形成,并在疾病后期出现认知功能障碍、癫痫和严重痴 呆等中枢神经系统(Central nervous system,CNS)损害。一旦发生将不可逆,目前尚无有 效治疗方法。 RBI的发病机制以神经元凋亡、神经炎症、小胶质细胞和星形胶质细胞的极化最受 关注。但目前治疗只依赖部分脑保护治疗药物及其它对症支持治疗,包括胞二磷胆碱、神经 节苷脂、注射用鼠神经生长因子、维生素B12等。但对于肿瘤放射治疗后产生神经系统损伤 的患者,不建议长期大剂量使用维生素B12。因其可通过叶酸促进细胞分裂,文献报道具有 诱发肺癌风险。而研究表明,注射用鼠神经生长因子有减轻动物血脑屏障受损、修复微血管 等作用,提示其能促进放射性脑损伤恢复,但其主要采用注射用药方式,且仅改善了脑水 肿。 因此,找寻RBI发生发展通路中的可能靶点进行精准调控以及选择何种方式能快 速直接地穿过血脑屏障,从而使药物进入到中枢神经系统对疾病进行干预是主要困难。 小胶质细胞激活及M1/M2表型转换与RBI、脑出血,帕金森病,阿尔兹海默病,多发 性硬化等疾病发生及转归密切相关。小胶质细胞是CNS特有的免疫细胞,激活后的小胶质细 胞通常处于经典的促炎型(M1)和抗炎修复型(M2)的动态平衡之中,其状态的转变与其所处 的局部微环境及病理刺激有关。在损伤状态或炎性因素刺激下,激活的小胶质细胞胞体增 大、突起变短、细胞形态呈圆形或杆状;此时小胶质细胞通常趋于M1样极化,产生促炎细胞 因子,具有较强的微生物灭杀特征,但M1样过度活化会通过释放促炎因子及神经毒性介质 造成细胞毒性,进而引发神经损伤的恶性循环。而M2型通常细胞突起变长或减少消失、细胞 形态呈阿米巴状,并具有吞噬功能,可以抑制炎症并参与促进组织修复。照射刺激常引起 CNS中的氧化应激,导致小胶质细胞向M1型过度激活,导致炎症因子如IL-1β、IL-6、TNF-α等 被大量释放,从而介导RBI的发生。 而MiRNA(microRNA)作为经典的短链非编码单链RNA,通过与靶基因3'UTR结合,从 而调控单个通路中的多种基因或多种交互通路,是CNS生理和病理进程的关键调节剂,是小 胶质细胞活化和极化以及正常和病变中枢神经系统中巨噬细胞分化的普遍调节因子。小胶 质细胞参与血脑屏障稳态维持,小胶质细胞极化相关的炎症转化及级联损伤是RBI病理进 程的关键环节。目前,虽然围绕RBI中小胶质细胞相关通路的干预研究不断开展,但miRNA对 3 CN 111593114 A 说 明 书 2/6 页 RBI的直接预防或治疗用途还未被探索。
技术实现要素:
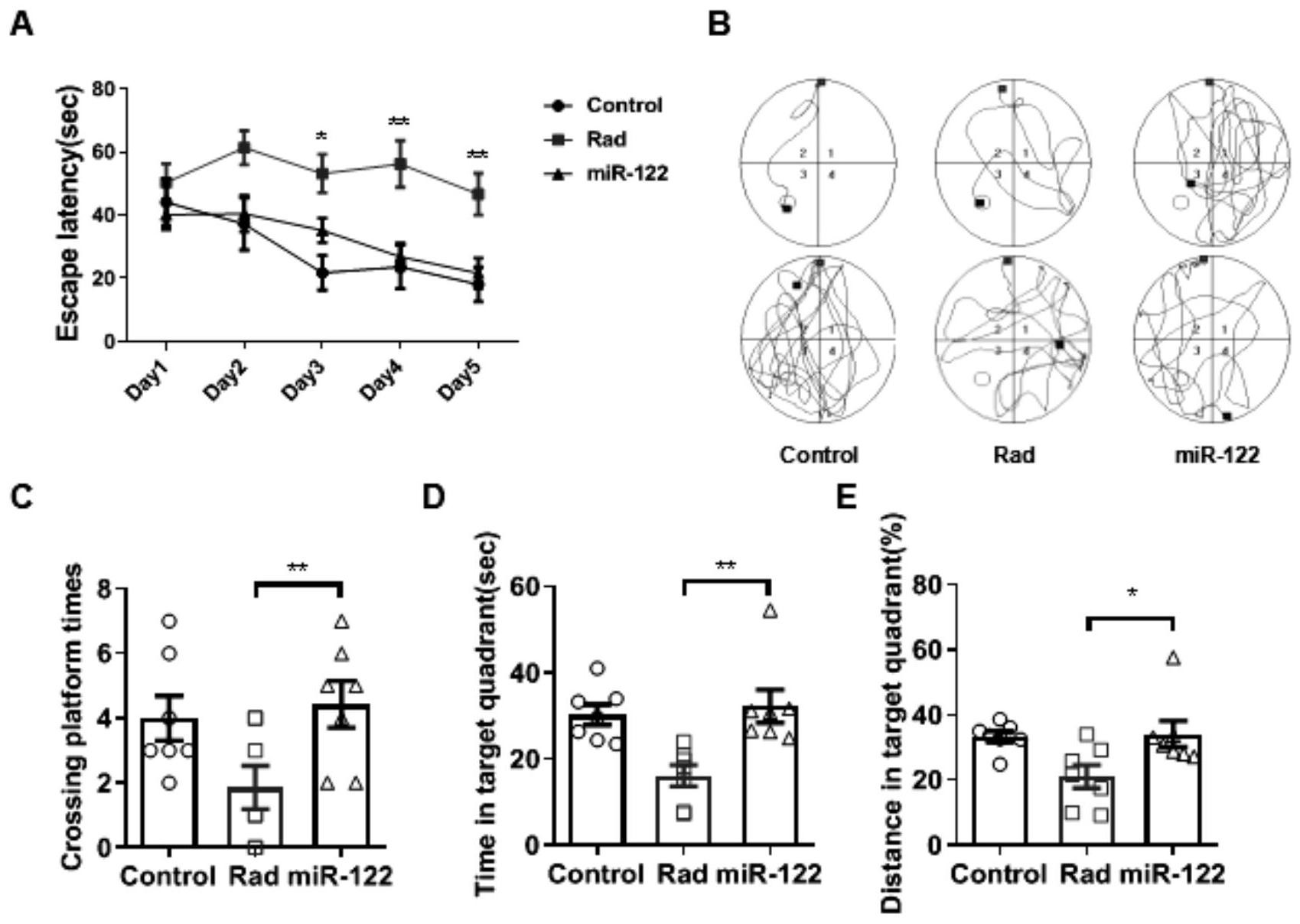
针对现有技术中存在的问题,本发明的目的在于提供一种miR-122及其抑制剂在 预防/治疗放射性脑损伤中的应用,以解决当前常用的放射性脑损伤药物存在副作用、治疗 不理想的问题。 为了实现上述目的,本发明采用以下技术方案予以实现。 (一)miR-122在制备用于预防放射性脑损伤的药物中的应用。 优选的,所述放射性脑损伤为鼻咽癌放疗引起的放射性脑损伤。 (二)miR-122在制备用于治疗放射性脑损伤的药物中的应用。 优选的,所述用于治疗放射性脑损伤的药物还包括糖皮质激素、贝伐珠单抗、胞二 磷胆碱、神经节苷脂、艾地苯醌、超氧化物歧化酶和维生素E中的至少一种。 (三)miR-122抑制剂在制备用于预防放射性脑损伤的药物中的应用。 (四)miR-122抑制剂在制备用于治疗放射性脑损伤的药物中的应用。 优选的,所述miR-122抑制剂为AntagomiR-122。 优选的,所述AntagomiR-122减少放射导致的小胶质细胞相关炎症因子的释放。 优选的,所述AntagomiR-122促进被照射后的小胶质细胞向M2型极化。 相比于现有技术,本发明的有益效果在于: 1)本发明的实验研究发现,miR-122-5p在照射后的小鼠海马及临床鼻咽癌放疗病 人中的表达显著上调;而通过miR-122干预后,在RBI动物模型中不仅能缓解神经炎症损伤, 改善行为认知等;且体外细胞放射性损伤模型中miR-122的抑制能调控小胶质细胞趋于M2 型极化。 2)本发明的实验还表明,TNS1与miR-122具有潜在的结合作用。而现有的研究证 明,TNS1参与调控人乳腺癌细胞生物学行为及放疗抵抗,也参与肿瘤细胞外基质重塑、细胞 极化,迁移和侵袭过程;并且与创伤性脑损伤模型中的神经功能恢复、局灶性脑缺血性损伤 等发生发展密切相关。因此,结合胶质细胞及神经炎症相关通路预测并检测筛选出miR-122 的潜在下游靶点TNS1,miR-122干预能调控小胶质细胞向M2型极化从而缓解RBI中炎症级联 损伤,来预防或治疗放射性脑损伤疾病。 3)由于所述用于预防放射性脑损伤的药物包括有效剂量的miR-122抑制剂,特别 是AntagomiR-122,因此,所述药物能够抑制体内的miR-122发挥作用,从而降低炎症因子的 表达,达到预防或治疗放射性脑损伤的目的。 附图说明 图1为RBI模型小鼠及NPC放疗后患者的差异表达miRNA的筛选图;其中,图1A为小 鼠行为学测试水迷宫数据及小鼠脑组织切片海马区组织的HE染色结果图;图1B~C为小鼠 海马miRNA二代测序及RT-qPCR验证结果图;图1D为鼻咽癌患者放疗前后的S100B、miR-122 和IL-1β的表达水平变化图。 图2为Antagomir-122鼻腔给药改善照射后行为认知图;其中,图2A为小鼠行为学 测试水迷宫数据图;图2B为小鼠水迷宫测试的活动轨迹图;图2C为小鼠水迷宫测试的穿越 4 CN 111593114 A 说 明 书 3/6 页 平台次数图;图2D为小鼠水迷宫测试的目标象限活动时间图;图2E为小鼠水迷宫测试的目 标象限路程占比百分图。 图3为Antagomir-122鼻腔给药改善照射后病理损伤图。 图4为Antagomir-122鼻腔给药改善照射后小胶星胶及神经元炎症损伤图;其中, 图4A为小鼠海马区RT-qPCR的数据图;图4B为小鼠海马区TNF-α的表达水平图;图4C为小鼠 海马区S100B的表达水平图;图4D为小鼠海马区Iba-1/DAPI图;图4E为小鼠海马区GFAP/ DAPI图;图4F为小鼠海马区TUBBLIN/DAPI图。 图5为体外放射性损伤细胞模型干预通过调控小胶质细胞极化改善小胶质细胞炎 症级联损伤图;其中,图5A为小胶质细胞体外转染Antagomir-122及450nm处吸光度值数据 图;图5B为IL-1β和IL-6炎症因子水平表达数据图;图5C为人神经母细胞瘤细胞SH-SY5Y中 转染Antagomir-122后miR-122相对表达的转染效率;图5D为小胶质细胞BV2和神经元细胞 SH-SY5Y共培养之后神经元细胞采用流式细胞术Tunel染色标记出的晚期凋亡和坏死的情 况;图5E为小胶质细胞BV2和神经元细胞SH-SY5Y共培养之后神经元细胞采用流式细胞术 Tunel染色标记出的早期凋亡情况;图5F为小胶质细胞BV2和神经元细胞SH-SY5Y共培养之 后的流式凋亡展示图。 图6为miR-122轴调控小胶质细胞极化下游靶点筛选图;其中,图6A为转录组分析 mRNA测序图;图6B为TNS1与miR-122序列图;图6C为TNS1与miR-122构建双荧光素酶载体图; 图6D为蛋白免疫印迹验证图。












