技术摘要:
本发明提供一种基于重组皮肤模型的光致敏性评价方法,所述方法包括以下步骤:S1.复苏重组皮肤模型;S2.涂抹受试物;S3.清洗受试物;S4.选取光源;S5.评价光致敏性;其中,所述评价光致敏性包括:利用双末端测序法分析全基因组,通过与未照射组比较致敏相关基因上调个数 全部
背景技术:
光致敏性是光感物质经皮吸收或通过循环到达皮肤后与吸收的光线在表皮细胞 层发生的反应,临床表现为组织损伤、细胞变性坏死炎症反应、产生表皮炎症如红斑、水肿 及丘疹等,有扩散性和反应持久性,一般无色素沉着,患者会感觉瘙痒和疼痛,严重者会引 起全身症状。卤化水杨酰苯胺、氯丙嗪、奎尼丁、非甾体抗炎类(最常见的是酮洛芬)、磺胺类 药物等具有光致敏性,化妆品中也存在许多光致敏性物质,这些物质通过皮肤接触、口服、 注射等途径进入体内,在光线照射后会引起光致敏性反应。 皮肤光致敏反应的有害结局路径(AOP)由四个关键事件组成:(1)起始事件:在光 照条件下,光致敏物与皮肤内的蛋白形成具有免疫原性的半抗原-蛋白结合物;(2)角质形 成细胞反应事件:角质细胞发生炎性反应并启动特定细胞通路基因表达(例如抗氧化/亲电 子剂反应元件依赖型通路),角质形成细胞反应事件的主要目的是促进朗格汉斯细胞捕获 抗原以及发生迁移;(3)树突状细胞反应事件:在角质细胞(keratinocyte,KC)提供的危险 信号下,皮肤内的朗格汉斯细胞(langerhans cell,LCs)捕获抗原,LCs在光致敏性的诱导 阶段发挥着重要的作用;(4)T细胞反应事件:LCs细胞被激活后移行至局部淋巴结,将抗原 呈递给初始T细胞,促使其活化和增殖分化,最终诱导记忆T细胞、辅助性T细胞(T helper cell,Th细胞)和细胞毒性T细胞(T cytotoxic cell,Tc细胞)的产生,完成光致敏作用的诱 导过程。当人体再次接触相同或有交叉反应的光致敏物时,局部淋巴结的记忆T细胞会迅速 活化,从而激发特异性的细胞免疫应答。Tc细胞通过释放穿孔素和蛋白酶,直接破坏抗原特 异性的靶细胞,引起组织坏死。Th细胞则可通过释放IFN-γ,IL-2,IL-8等细胞因子、炎症因 子,激活巨噬细胞和自然杀伤细胞(natural killercell,NK),引起单个核细胞浸润为主的 组织损伤,完成光致敏作用的激发过程。 对于光致敏性的评价方法,传统的方法主要采用动物实验。(1)豚鼠光致敏试验, 豚鼠光致敏试验方法的优点在于可以完整地模拟人的光致敏反应过程,灵敏度和准确度较 高,但该方法存在以下缺点:使用动物数量多、试验周期长,对动物损伤大,不符合动物福利 及3R原则,仅能通过肉眼观察并打分进行评价,评价结果易受试验者主观因素和水平的影 响,缺乏客观定量的评价指标,并且无法对有色化合物的光致敏性进行评价等;(2)光照条 件下小鼠局部淋巴结试验:与传统的豚鼠光致敏试验相比,光照条件下局部淋巴结试验优 势在于具有客观的评价指标,使用动物数减少,试验周期缩短,并且可以评价有色受试物, 但是通过在诱导期检测受试物引起局部淋巴结增殖进行光致敏性评价,光刺激剂可能会出 现假阳性结果;从而使这些方法特异性受到一定影响。 目前光致敏体外评价方法,比如:以角质细胞(keratinocyte,KC)为光致敏模型的 体外评价方法;以树突状细胞为模型的体外评价方法;基于人类细胞系激活试验(human 3 CN 111596047 A 说 明 书 2/10 页 cell lineactivation test,h-CLAT)评价方法。这几种方法一方面都处于验证阶段,另一 方面,这些方法最大的一个弊端是都基于细胞水平所开展的检测,而对于不容易分散的化 学品及化妆品成品不适用。 Epikutis是以中国人皮肤组织分离出的角质形成细胞为种子细胞,经专利技术构 建而成的3D重组表皮模型。Epikutis重组人表皮模型具有完整的表皮结构:基底层、棘层、 颗粒层、角质层,与人表皮结构高度类似,而且是国内首款产业化的3D皮肤模型。 因此,开展基于重组皮肤模型Epikutis的光致敏性评价方法对国人而言具有重要 的意义。
技术实现要素:
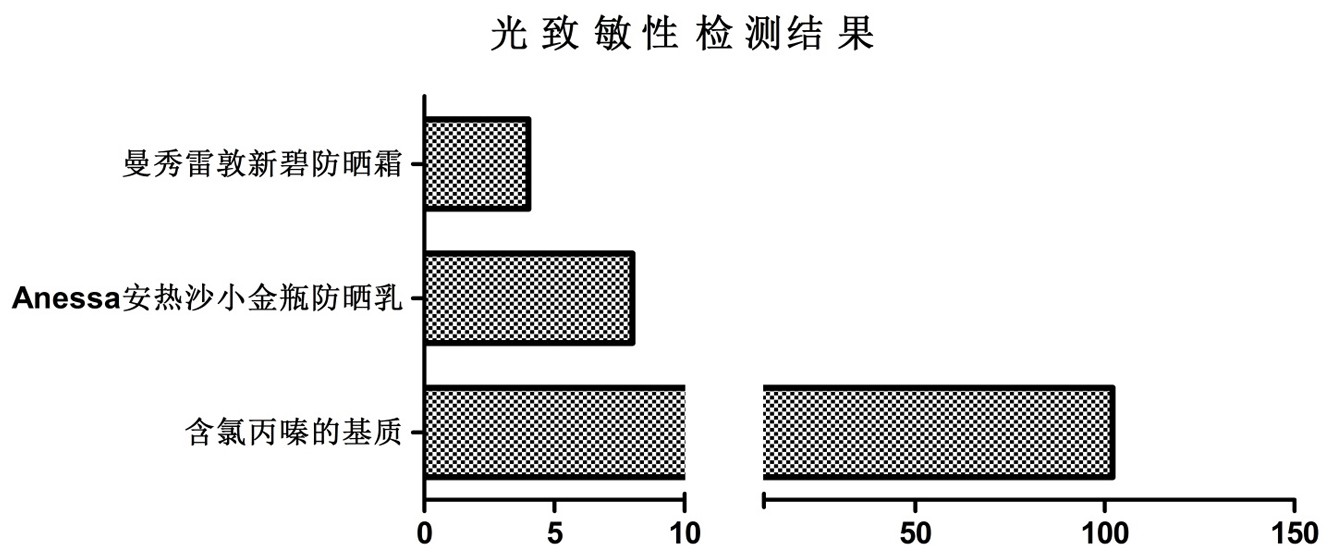
有鉴于此,本发明的目的在于提供一种基于重组皮肤模型的光致敏性评价方法, 不仅能够检测容易分散的化学品,还能检测不容易分散的化学品及化妆品成品。 为此,本发明提供了以下技术方案。 第一方面,本发明提供了一种基于重组皮肤模型的光致敏性评价方法,其中,所述 方法包括以下步骤: S1.复苏重组皮肤模型; S2.涂抹受试物; S3.清洗受试物; S4.选取光源; S5.评价光致敏性; 其中,所述评价光致敏性包括: 利用双末端测序法分析全基因组,通过与未照射组比较致敏相关基因上调个数来评价 受试物的光致敏性。 在优选的实施方式中,所述复苏重组皮肤模型包括: 在6孔板中培养重组皮肤模型,每孔中1个重组皮肤模型,每孔添加900μL复苏液,置于 温度为36-38℃、相对湿度为92-95%和4-6%CO2的培养箱中孵育55-65min后,更换复苏液, 过夜孵育18-22h,在复苏过程中,将损坏的以及表面上存在大量水分的重组皮肤模型丢弃, 复苏结束后对重组皮肤模型表观进行评价,表观正常后进行后续操作。 在优选的实施方式中,所述光源为波长为320-400nm的UVA;例如,所述光源为波长 为320nm、330nm、340nm、350nm、360nm、370nm、380nm、390nm或400nm的UVA。 在更优选的实施方式中,所述UVA的剂量为0.5-60J/cm2;例如,所述UVA的剂量为 0.5J/cm2、1J/cm2、2J/cm2、3J/cm2、4J/cm2、5J/cm2、6J/cm2、7J/cm2、8J/cm2、9J/cm2、10J/cm2、 12J/cm2、15J/cm2、17J/cm2、20J/cm2、22J/cm2、25J/cm2、28J/cm2、30J/cm2、33J/cm2、37J/cm2、 40J/cm2、41J/cm2、45J/cm2、50J/cm2、52J/cm2、55J/cm2、57J/cm2或60J/cm2。 在本发明中,UVA的照射时间根据所测量的照射强度进行计算,其中照射剂量为 20-60J/cm2,照射强度采用UVA剂量仪进行测量,根据以下公式计算出照射时间: 在优选的实施方式中,所述涂抹受试物包括: 4 CN 111596047 A 说 明 书 3/10 页 用移液枪吸取20-60μL受试物,然后垂直将受试物加到重组表皮模型的表皮表面,再用 带有软胶头的涂抹棒,轻轻涂抹重组皮肤模型表面的受试物,使其均匀分布于重组皮肤模 型表面,再将涂抹有受试物的重组表皮模型置于置于温度为36-38℃、相对湿度为92-95% 和4-6%CO2的培养箱中培养20-60min。 在优选的实施方式中,所述清洗受试物包括: 用装有PBS的无菌洗瓶清洗重组皮肤模型表面残留的受试物,轻轻吹打清洗10-20次, 对于较为粘稠的受试物,先用棉签将表面残留物擦拭,再用装有PBS的无菌洗瓶清洗。 在优选的实施方式中,所述重组皮肤模型为重组皮肤模型Epikutis。 在优选的实施方式中,所述受试物包括能够形成分散体系的化学品、不能形成分 散体系的化学品和油状或膏状的化妆品成品。 在优选的实施方式中,所述表观正常表现为重组皮肤模型表面无气泡、无褶皱、不 潮湿。 在本发明中,所述重组皮肤模型为重组皮肤模型Epikutis,重组皮肤模型 Epikutis是以中国人皮肤组织分离出的角质形成细胞为种子细胞,经专利技术构建而成的 3D重组表皮模型。重组皮肤模型Epikutis具有完整的表皮结构:基底层、棘层、颗粒层、角质 层,与人表皮结构高度类似。 在本发明中,可以采用广东博溪生物科技有限公司生产的重组皮肤模型 Epikutis,货号为PM1011;可以采用广东博溪生物科技有限公司生产的培养液,货号为 PY3021;可以采用广东博溪生物科技有限公司生产的复苏液,货号为PY3031。 相对于现有技术,本发明的有益效果在于: 本发明基于重组皮肤模型的光致敏性评价方法,不仅能够检测容易分散的化学品,还 能检测不容易分散的化学品及油状、膏状的化妆品成品,本发明基于重组皮肤模型的光致 敏性评价方法不仅模拟了人体皮肤对不同类外源性物质的生物反应变化,同时扩大了待测 物质的检测范围,不再局限于容易分散的化学品,还包括了不容易分散的化学品以及各种 性状的化妆品成品。 另一方面,本发明通过选用特定波长的UVA,选用特定剂量的UVA以及选用特定的 UVA照射时间,进一步保证了本发明基于重组皮肤模型的光致敏性评价方法的准确性,若受 试物中添加了一定浓度的光致敏性物质后,可以用本发明的重组皮肤模型Epikutis,配合 本发明的光致敏评价方法准确的检测出来。 附图说明 图1为化学标准品光致敏性评价结果图; 图2为化妆品成品光致敏性评价结果图; 图3为不分散化学品的光致敏性评价结果图。












