技术摘要:
一种肿瘤双靶向的诊疗连用光敏剂及其制备方法与应用,所述光敏剂的结构如式I所示,同一结构集肿瘤双靶向递送、近红外荧光成像诊断及光动力治疗于一体。体内外实验证明,本发明提供的光敏剂在菁染料正电性及吗啉环的双靶向作用下可选择性富集于肿瘤组织,对肿瘤乏氧微环 全部
背景技术:
恶性肿瘤是严重威胁人类健康的重大疾病之一,设计研发高效、安全和经济适用 的集肿瘤诊断、评价及治疗于一体的诊治联用药物,对于改善肿瘤治疗效果,减轻患者经济 负担、提高患者生存质量具有十分重要意义。一些特殊物质(如光敏剂)经一定波长的光照 射达到激发态后,会把能量传递给组织周围的氧气分子生成活性氧物种(ROS),最终开启细 胞的凋亡途径,有效抑制肿瘤的生长,即光动力治疗过程,目前已广泛应用于肿瘤治疗研究 中。另一方面,肿瘤快速生长过程中,肿瘤细胞对氧气的需求量会增加,最终导致部分瘤内 微环境处于明显的乏氧状态(3~0.1%O2)。乏氧是所有实体肿瘤的共同特征,目前,乏氧状 态已成为一种在临床上评估肿瘤恶化程度的重要指标。研究表明,乏氧状态下,细胞内的硝 基还原酶(NTR)的表达量会大大增高,因而,发展特异性的NTR检测技术,将可以有效地评估 肿瘤组织和细胞的乏氧程度,进而应用于肿瘤的荧光成像诊断。综上,集乏氧响应和光动力 治疗于一体的多功能光敏剂将在肿瘤的早期诊断、术前评估、术中导航和临床治疗中有着 良好的应用前景。 线粒体是真核细胞内最重要的细胞器之一,具有较大的跨膜电位,与正常细胞相 比,肿瘤细胞线粒体膜电位要高出约60mV。在线粒体膜电位的驱动下,一些离域亲脂阳离 子,如三苯基膦、正电性的菁类染料等,可选择性靶向至肿瘤细胞线粒体,这一性质目前已 广泛应用于肿瘤靶向药物输送。而作为真核细胞的另一种重要细胞器,溶酶体拥有微酸性 内环境(pH 4.5~5.5),以助于其内部的各种水解酶行使各自功能。溶酶体在肿瘤细胞中的 低酸水平成为研究者们开发溶酶体靶向药物的特征。如吗啉基团由于其为弱碱性(pH值约 为9~10),故其成为研究者们作为溶酶体靶向药物递送的基团之一。因此,基于线粒体和溶 酶体的靶向药物传递成为当前研究的热点,为开发新的肿瘤靶向药物提供了新的希望。
技术实现要素:
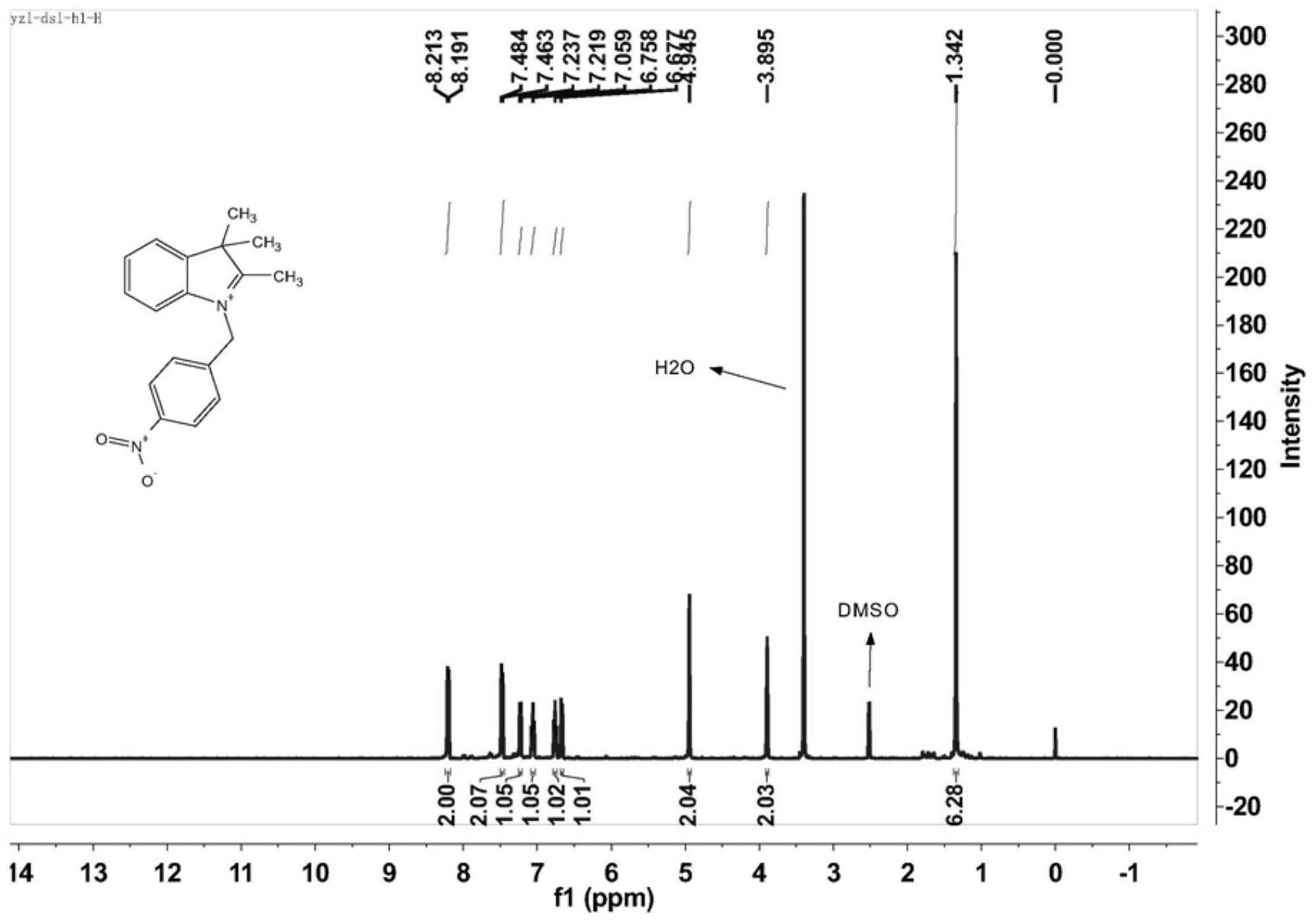
本发明所要解决的是改善肿瘤治疗效果,减轻患者经济负担、提高患者生存质量 的技术问题。 为了解决上述技术问题,本发明采用如下技术方案: 一种肿瘤双靶向的诊疗连用光敏剂,其结构式如式I所示: 4 CN 111569069 A 说 明 书 2/7 页 所述的肿瘤双靶向的诊疗连用光敏剂I的合成方法,包括如下步骤: 步骤一:4-(4羟基苯基)环己酮在二氯甲烷和DMF内于草酰氯作用下生成中间体1; 步骤二:2,3,3-三甲基吲哚与对硝基苄溴在甲苯内反应生成中间体2; 步骤三:中间体1和中间体2在乙醇内经乙酸钠催化,生成中间体3; 步骤四:中间体3和N-(2-氨基乙基)吗啉于乙腈内反应制得式I所示肿瘤双靶向的 诊疗连用光敏剂;见以下反应路线: 所述肿瘤双靶向的诊疗连用光敏剂在成像诊断中的应用。 所述成像诊断为分子影像学中的近红外荧光成像诊断。 采用上述技术方案的有益效果是: 1.本发明具有正电性和吗啉环结构特征,对肿瘤组织具有双重靶向作用; 2.本发明的荧光响应位于近红外区域,组织穿透能力强,对生物样品光损伤小; 3.本发明可对肿瘤组织乏氧微环境中的NTR给出近红外荧光打开响应,进而实现 肿瘤的近红外荧光成像诊断; 4.本发明在近红外光辐射下,可对肿瘤细胞表现出明显的光毒性; 5.本发明经尾静脉注射后,在近红外光辐射下,可显著抑制小鼠肿瘤的生长; 6.本发明对小鼠毒性低,满足临床用药基本要求; 7.本发明结构简单、组成确定、易于制备纯化,可批量生产,且易于储存。 5 CN 111569069 A 说 明 书 3/7 页 附图说明 图1为本发明中间体2的1H NMR谱图。 图2为本发明中间体2的13C NMR谱图。 图3为本发明中间体3的1H NMR谱图。 图4为本发明中间体3的13C NMR谱图。 图5为本发明中间体3的高分辨质谱图。 图6为本发明式I所示光敏剂的1H NMR谱图。 图7为本发明式I所示光敏剂的13C NMR谱图。 图8为本发明式I所示光敏剂的高分辨质谱图。 图9为本发明式I所示光敏剂(10μM)的吸收光谱(乙醇溶液)和荧光激发/发射光谱 (甲醇溶液)。 图10为本发明式I所示光敏剂(10μM)对不同浓度NTR的响应荧光光谱。 图11为本发明式I所示光敏剂对4T1细胞和HeLa细胞的乏氧荧光成像。 图12为本发明4T1建模BALB/c小鼠尾静脉注射式I所示光敏剂(2.5μmol/kg)荧光 活体成像。 图13为本发明4T1建模BALB/c小鼠尾静脉注射式I所示光敏剂(2.5μmol/kg)2h后 肿瘤部位注射NTR(10μg)辅助荧光活体成像。图14为本发明DPBF与式I所示光敏剂在660nm 二极管激光灯辐射下的光降解曲线。 图15为本发明DPBF在式I所示光敏剂存在时经660nm二极管激光灯辐射后411nm处 的吸光度变化。 图16为本发明式I所示光敏剂对4T1细胞的光毒性和暗毒性。 图17为本发明4T1建模BALB/c小鼠经式I所示光敏剂光动力治疗7天肿瘤体积变 化。 图18为本发明式I所示光敏剂光动力治疗7日后各组小鼠肿瘤体积大小情况。 图19为本发明式I所示光敏剂给药组和不给药组的各项血清生化指标。 图20为本发明式I所示光敏剂光动力治疗7日后各脏器组织切片的H&E染色图像。












