技术摘要:
本发明实施例涉及医学检测技术领域,特别是涉及一种用于检测同型半胱氨酸的试剂盒,包括:壳体、试剂以及信息卡。信息卡存储有吸光度值与浓度值的标准曲线,信息卡存储有校正因子,校正因子用于当待检测血液样本为全血时,校正血液样本中的同型半胱氨酸的浓度。试剂包 全部
背景技术:
同型半胱氨酸(HCY)是动脉粥样硬化血管疾病重要的危险因素,它是甲硫氨酸代 谢形成的中间产物。血液中同型半胱氨酸(HCY)浓度升高(浓度≥12umol/L)是冠心病、中 风、外周血管粥样硬化及动静脉栓塞的危险因子,血液中同型半胱氨酸(HCY)升高使心血管 疾病发病率及死亡率增加,因此测定血液中同型半胱氨酸(HCY)浓度在临床意义上十分重 要。 目前测定同型半胱氨酸(HCY)的方法主要有以下几种:循环酶法技术;高效液相色 谱法(HPLC)、酶免疫分析法(EIA)、离子色谱法、毛细管电泳法、荧光偏振免疫分析法。目前 全球市场上,循环酶法技术主要分为两种,即水解酶循环酶法和胱硫醚循环酶法。其中 但是,本发明的发明人在实现本发明实施例的过程中,发现:胱硫醚循环酶法主要 是通过测量同型半胱氨酸(HCY)转化为β-胱硫醚产生的胱硫醚来确定同型半胱氨酸(HCY) 的含量,却不能消除病人自身所带的胱硫醚的干扰;水解酶循环酶法特异性高,抗干扰能力 强,然而目前的测试试剂灵敏度低且操作复杂。
技术实现要素:
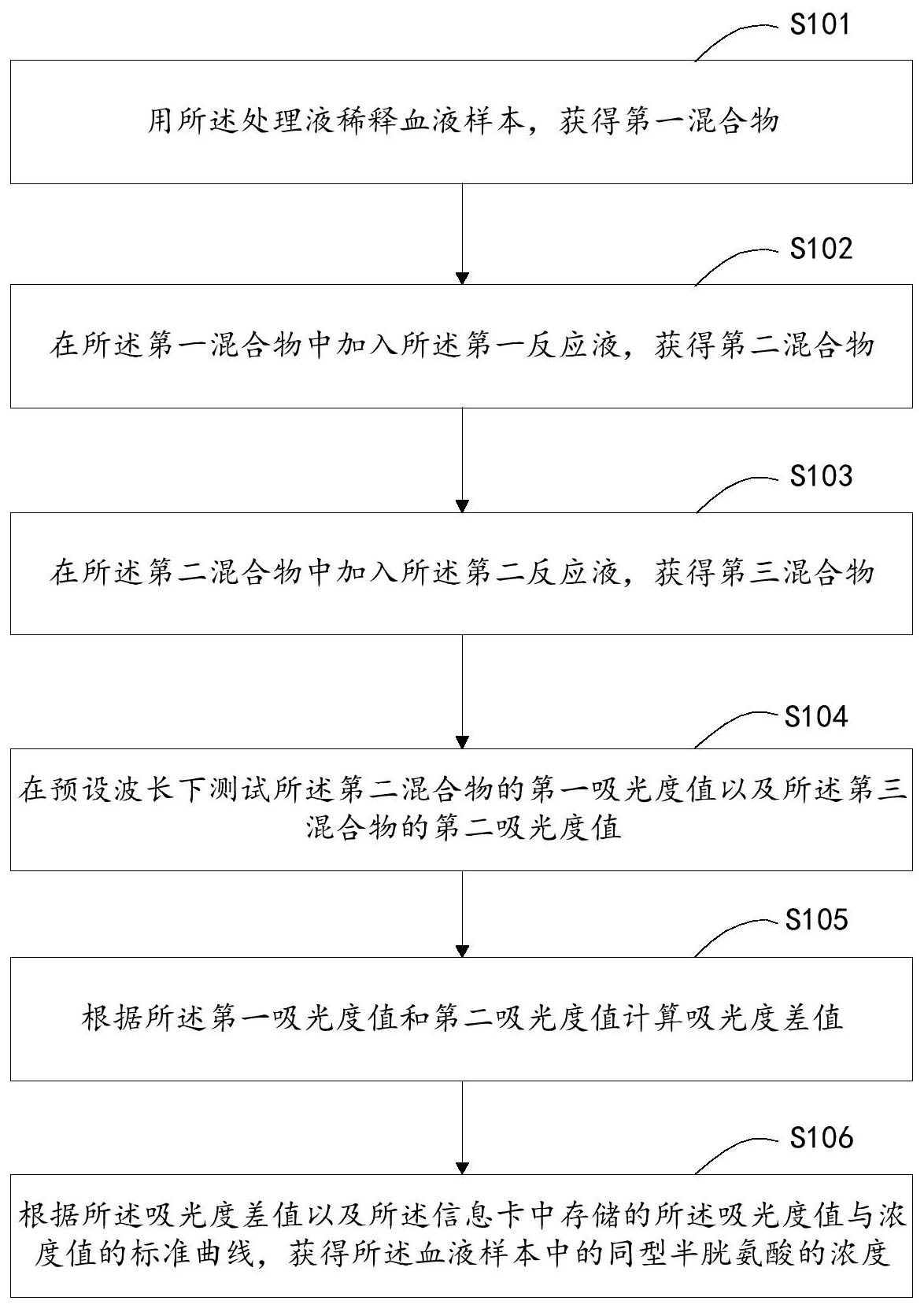
鉴于上述问题,本发明实施例提供了一种用于检测同型半胱氨酸的试剂盒,克服 了上述问题或者至少部分地解决了上述问题。 根据本发明实施例的一个方面,提供了一种用于检测同型半胱氨酸的试剂盒,包 括壳体、试剂以及信息卡;所述壳体设置有收容空间,所述试剂收容于所述收容空间内,所 述信息卡设置于所述壳体,所述信息卡存储有吸光度值与浓度值的标准曲线,所述信息卡 存储有校正因子,所述校正因子用于当待检测血液样本为全血时,校正所述血液样本中的 同型半胱氨酸的浓度;所述试剂包括:处理液、第一反应液和第二反应液;所述处理液用于 将所述血液样本中的蛋白结合型同型半胱氨酸转换为游离型同型半胱氨酸;所述第一反应 液包括还原型烟酰胺腺嘌呤二核苷酸磷酸、二硫苏糖醇、α-酮戊二酸、修饰化HCY甲基转移 酶、琥珀酸脱氢酶以及乙酸钠,其中,所述还原型烟酰胺腺嘌呤二核苷酸磷酸的含量为 0.2%-0.3%,所述二硫苏糖醇的含量为0.1%-0.12%,所述α-酮戊二酸的含量为0.6%- 0 .8%,所述修饰化HCY甲基转移酶的浓度为3.0KU/L-6 .0KU/L,琥珀酸脱氢酶的浓度为 5.0KU/L-8.0KU/L,所述乙酸钠的含量为0.1%-0.15%;所述第二反应液包括修饰化S-腺苷 同型半胱氨酸水解酶、腺苷脱氨酶、蛋氨酸腺苷转移酶、牛血清白蛋白以及曲拉通X-100,其 中,所述修饰化S-腺苷同型半胱氨酸水解酶的浓度为3.0KU/L-6.0KU/L,所述腺苷脱氨酶的 浓度为4.0KU/L-8.0KU/L,所述蛋氨酸腺苷转移酶的浓度为4.0KU/L-8.0KU/L,所述牛血清 白蛋白的含量为0.5%-1,所述曲拉通X-100的含量为0.1%-0.5%。 4 CN 111593091 A 说 明 书 2/11 页 在一种可选的方式中,所述处理液包括PEG6000、乙二胺四乙酸钠、十二烷基硫酸 钠以及proclin300,其中,所述PEG6000的含量为0.1%-0.5%,所述乙二胺四乙酸钠的含量 为0.01%-0.05%,所述十二烷基硫酸钠的含量为0.01%-0.2%,所述proclin300的含量为 0.1%-0.3%。 在一种可选的方式中,所述处理液还包括第一Tris缓冲液,所述第一Tris缓冲液 的浓度为50mmol/L,并且所述第一Tris缓冲液在温度为25℃时的PH为7.4。 在一种可选的方式中,所述第一反应液还包括第二Tris缓冲液,所述第二Tris缓 冲液的浓度为100mmol/L,并且所述第二Tris缓冲液在温度为25℃时的PH为9.2。 在一种可选的方式中,所述第二反应液还包括第三Tris缓冲液,所述第三Tris缓 冲液的浓度为80mmol/L,并且所述第三Tris缓冲液在温度为25℃时的PH为7.6。 根据本发明实施例的一个方面,提供了一种同型半胱氨酸的检测方法,应用于分 析仪,所述检测方法使用上述的用于检测同型半胱氨酸的试剂盒,包括:用所述处理液稀释 血液样本,获得第一混合物;在所述第一混合物中加入所述第一反应液,获得第二混合物; 在所述第二混合物中加入所述第二反应液,获得第三混合物;在预设波长下测试所述第二 混合物的第一吸光度值以及所述第三混合物的第二吸光度值;根据所述第一吸光度值和第 二吸光度值计算吸光度差值;根据所述吸光度差值以及所述信息卡中存储的所述吸光度值 与浓度值的标准曲线,获得所述血液样本中的同型半胱氨酸的浓度。 在一种可选的方式中,当所述血液样本为全血时,所述根据所述第一吸光度值和 第二吸光度值计算吸光度差值的步骤,进一步包括:计算所述第二吸光度值、第一吸光度值 以及校正因子的差值,所述第二吸光度值、第一吸光度值以及校正因子的差值即为所述吸 光度差值。 在一种可选的方式中,当所述血液样本为血清时,所述根据所述第一吸光度值和 第二吸光度值计算吸光度差值的步骤,进一步包括:计算所述第二吸光度值与第一吸光度 值的差值,所述第二吸光度值与第一吸光度值的差值即为所述吸光度差值。 在一种可选的方式中,所述在预设波长下测试所述第二混合物的第一吸光度值以 及所述第三混合物的第二吸光度值之前,所述检测方法还包括:在预设波长下测试生理盐 水的第三吸光度值,并将所述第三吸光度值调零。 根据本发明实施例的一个方面,提供了一种检测系统,包括分析仪以及上述的用 于检测同型半胱氨酸的试剂盒。 本发明实施例的有益效果是:区别于现有的用于检测同型半胱氨酸的试剂盒,本 发明实施例提供的试剂盒包括:壳体、试剂以及信息卡。所述信息卡存储有吸光度值与浓度 值的标准曲线,所述信息卡存储有校正因子,所述校正因子用于当待检测血液样本为全血 时,校正所述血液样本中的同型半胱氨酸的浓度。所述试剂包括处理液、第一反应液和第二 反应液;所述处理液用于将所述血液样本中的蛋白结合型同型半胱氨酸转换为游离型同型 半胱氨酸;所述第一反应液包括还原型烟酰胺腺嘌呤二核苷酸磷酸、二硫苏糖醇、α-酮戊 二酸、修饰化HCY甲基转移酶、琥珀酸脱氢酶以及乙酸钠,其中,所述还原型烟酰胺腺嘌呤二 核苷酸磷酸的含量为0.2%-0.3%,所述二硫苏糖醇的含量为0.1%-0.12%,所述α-酮戊 二酸的含量为0.6%-0.8%,所述修饰化HCY甲基转移酶的浓度为3.0KU/L-6.0KU/L,琥珀酸 脱氢酶的浓度为5.0KU/L-8.0KU/L,所述乙酸钠的含量为0.1%-0.15%;所述第二反应液包 5 CN 111593091 A 说 明 书 3/11 页 括修饰化S-腺苷同型半胱氨酸水解酶、腺苷脱氨酶、蛋氨酸腺苷转移酶、牛血清白蛋白以及 曲拉通X-100,其中,所述修饰化S-腺苷同型半胱氨酸水解酶的浓度为3.0KU/L-6.0KU/L,所 述腺苷脱氨酶的浓度为4.0KU/L-8 .0KU/L,所述蛋氨酸腺苷转移酶的浓度为4.0KU/L- 8.0KU/L,所述牛血清白蛋白的含量为0.5%-1,所述曲拉通X-100的含量为0.1%-0.5%。使 用所述用于检测同型半胱氨酸的试剂盒在分析仪上检测同型半胱氨酸的浓度,分析仪根据 信息卡中存储的吸光度值与浓度值的标准曲线可直接获得同型半胱氨酸的浓度,非常方 便。此外,由于所述信息卡中存储有校正因子,所述用于检测同型半胱氨酸的试剂盒适用于 检测全血样本中的同型半胱氨酸的浓度。 附图说明 一个或多个实施例通过与之对应的附图中的图片进行示例性说明,这些示例性说 明并不构成对实施例的限定,附图中具有相同参考数字标号的元件表示为类似的元件,除 非有特别申明,附图中的图不构成比例限制。 图1是本发明实施例提供的用于检测同型半胱氨酸的试剂盒的试剂盒的示意图; 图2是本发明实施例提供的吸光度值与浓度值的标准曲线图; 图3是本发明实施例提供的考核试剂和对比试剂的散点图; 图4是本发明实施例提供的考核试剂和对比试剂的绝对偏倚图; 图5是本发明实施例提供的考核试剂和对比试剂的相对偏倚图; 图6是本发明实施例提供的同型半胱氨酸的检测方法的流程示意图。












