技术摘要:
本发明一种嗜碱性粒细胞活化、脱颗粒的测试方法,包括:稀释待测过敏原制成标准待测过敏原,设立阳性对照和阴性对照;所有待测样本为肝素化的患者外周血,需封口孵育;随后加入缓冲液,离心;加入荧光染色混合液,轻混至沉淀物再悬浮,避光孵育;加入红细胞裂解液,漩 全部
背景技术:
随着全球日趋严重的环境污染、化学品滥用、电离辐射、转基因食品、以及各式各 样的食品添加剂等以一系列问题的不断出现,“过敏”成为了人类健康的又一大“杀手”。据 报告,全世界有30%-40%的人被过敏问题困扰,涉及多个器官和系统,例如皮肤过敏反应、 呼吸道过敏反应、胃肠道过敏反应及过敏性休克等。2018年流行病学数据显示,全世界3亿 人患有哮喘,4亿人有湿疹及特异性皮炎,超过5亿人患有变应性鼻炎。过敏性疾病的自然进 程是过敏原的种类日益增多,例如新合成的食品添加剂、工业原料、化学试剂,甚至部分新 型药物等;临床症状多变。过敏是一种复杂的免疫系统疾病,临床表现多样化,如过敏性鼻 炎、哮喘、荨麻疹、过敏性皮炎和湿疹等,严重时导致过敏性休克、喉头水肿,哮喘突发或持 续状态,有生命危险。过敏离我们并不遥远,轻者影响生活质量,严重者亦可有生命威胁,例 如一代歌后邓丽君就是哮喘突发去世的,32岁的好莱坞女星Brittany Murphy则是因药物 过敏抢救无效意外身亡。作为过敏性疾病的主要效应细胞,嗜碱性粒细胞活化、脱颗粒释放 组胺是其发挥生物学功能启动过敏进程的关键步骤。鉴于嗜碱性粒细胞在人外周血中较易 获得的特性,因此,嗜碱性细胞激活实验(Basophil activation test,BAT)是迄今为止目 前国际上相关实验室正在使用的相对有效的体外过敏原检测手段。遗憾的是,实践结果显 示目前常用的生物标记物组合使得BAT检测在不同个体之间的准确度、灵敏性和特异性差 异较大,再加上有些过敏患者本身外周血嗜碱性粒细胞水平就较低,因此,导致目前BAT还 没有被纳入常规的临床检测手段,只是应用于部分临床研究。因此,寻找新的、更特异的嗜 碱性粒细胞激活表面标记物以改进这一基于外周血嗜碱性粒细胞组胺释放的过敏原检测 方法,有望可以有效的克服上述缺陷,达到高效、准确的检测到过敏原的目的。
技术实现要素:
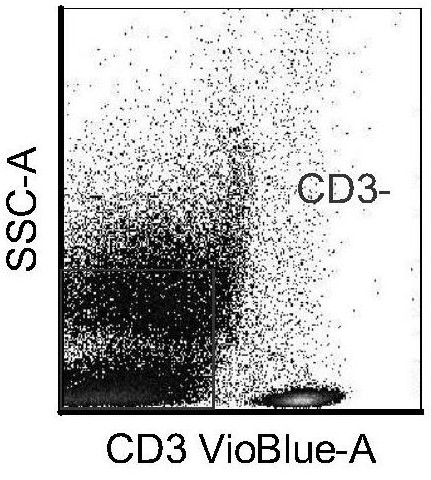
为解决现有临床和科研应用中存在的技术问题,本发明的目的在于提供一种嗜碱 性粒细胞活化、脱颗粒的测试方法。 为实现上述目的,达到上述技术效果,本发明采用以下技术方案来实现: 一种嗜碱性粒细胞活化、脱颗粒的测试方法,包括以下步骤: 步骤(一)、样品和相关试剂准备 S1、对待测过敏原进行等比例稀释,按顺序编号后作为标准待测过敏原; S2、制备阳性对照和阴性对照; S3、用无菌双蒸水按1:10-12的比例稀释红细胞裂解液,备用; 步骤(二)、样品孵育和检测 S4、将步骤S1-S2制备的阳性对照、阴性对照和标准待测试过敏原样品分别转移至 4 CN 111549091 A 说 明 书 2/6 页 流式细胞上样管中,每管中分别添加100-120μL待测肝素化患者血液,封口孵育; S5、向上述步骤中得到的所有样本中加入2-4mL PBS/EDTA,于4℃、340g离心力条 件下离心10-15min,吸出上清液; S6、向所有样本中分别加入50-60μL荧光染色混合液,轻混至沉淀物再悬浮,室温 避光孵育; S7、向所有样本中分别加入红细胞裂解液,漩涡10-15s,避光孵育; S8、向所有样本中加入PBS缓冲液,离心,弃上清; S9、重悬沉淀物,随后过滤,制成单细胞悬液; S10、向所有样本中添加300-320μL MACS缓冲液,保存,等待检测; 将上述所得样本采用流式细胞仪进行检测,在门控模式下根据染色标记物的平均 荧光强度来分析嗜碱性粒细胞活化、脱颗粒的比例。 进一步的,步骤S1中,使用RPMI 1640培养基作为稀释缓冲液,选择牛奶、花粉、尘 螨、花生等易致敏物质的提取液作为待测过敏原,使用RPMI 1640培养基对待测过敏原进行 1:7-9等比例稀释,依次稀释后按顺序编号,作为标准待测过敏原样品。 进一步的,步骤S2中,制备阳性对照的步骤为: 步骤S21、将人源性IgE抗体使用PBS稀释成1:10-12; 步骤S22、用90-100μL培养基稀释10-20μL步骤S21所得人源性IgE抗体,制成阳性 对照。 进一步的,所述培养基为RPMI 1640培养基,其组分包括:10%FCS、100U青霉素、 100μg/mL链霉素。 进一步的,步骤S3中,所述红细胞裂解液为:取8.29g NH4Cl、1.00g KHCO3、37.2mg Na2EDTA,溶于1000mL蒸馏水中制配而成。 进一步的,步骤S4中,将步骤(一)中的步骤S1-S2所得阳性对照、阴性对照和标准 待测试过敏原分别等量转移至带编号的流式细胞上样管中,每管的总体积均为100-120μL, 随后向每管中添加100-120μL肝素化待测患者血液,用封口膜密封所有样本,轻轻摇动并放 置在孵育箱中,于37.0-37.5℃、3-5%CO2条件下孵育10-15min。 进一步的,步骤S6中,所有样本中分别加入50-60μL荧光染色混合液,轻轻混合,不 涡旋,轻轻的重悬细胞,在室温、黑暗中孵育30-45min。 进一步的,向所有样本中分别加入50-60μL荧光染色混合液(CD3、CD63、CD203c以 及CCR3),轻轻混合,不涡旋,轻轻的重悬,在室温、黑暗中孵育样品30-45分钟,再分别加入 红细胞裂解液,在漩涡振荡器上低速漩涡样本10-15秒,并在室温、暗处孵育5-10min。 进一步的,步骤S6中,所述荧光染色混合液为:取35-39μL FACS缓冲液,依次加入 1-2μL丙种球蛋白、2-3μL VioBlue荧光标记的CD3、5-6μL FITC荧光标记的CD63、2-3μL PE 荧光标记的CD203c和3-4μL APC荧光标记的CCR3制配而成。 进一步的,步骤S10中,向上述得到的所有样本中加入2-4mL PBS,将样品在4℃、 340g离心力条件下离心10-15min,弃上清液,再次重悬,若肉眼仍可见红色,重复离心,经过 多次离心、悬浮直至没有红色沉淀物出现为止;以30μm孔径的无菌细胞滤器过滤所有样品, 制备成单细胞悬液,随后向所有样本中添加300-320μL MACS缓冲液,在4℃温度下保存,等 待检测。 5 CN 111549091 A 说 明 书 3/6 页 进一步的,步骤S10中,所述MACS缓冲液为溶解于PBS中的1%BSA和2mmol/L EDTA。 与现有技术相比,本发明的有益效果为: 本发明公开了一种嗜碱性粒细胞活化、脱颗粒的测试方法,包括以下步骤:稀释待 测过敏原作为标准待测过敏原,同时设立人源性IgE抗体为阳性对照,培养基为阴性对照; 所有待测样本为肝素化的患者外周血,需封口孵育;随后加入PBS/EDTA,离心,吸出上清液; 接着加入荧光染色混合液(CD3、CD63、CD203c以及CCR3),轻混至沉淀物再悬浮,避光孵育; 再次加入红细胞裂解液,漩涡混匀,避光孵育;稀释,离心,吸出上清液,再悬沉淀物;过滤后 添加MACS缓冲液,采用流式细胞仪进行检测,在门控模式下根据染色标记物的平均荧光强 度来分析嗜碱性粒细胞活化、脱颗粒的比例。本发明提供的嗜碱性粒细胞活化、脱颗粒的测 试方法,无需分离纯化嗜碱性粒细胞,选用新的特异性嗜碱性粒细胞标记物组合,所测试样 本用量小,重复性好,误差小,能有效分辨嗜碱性粒细胞的活化、脱颗粒程度,更好地为相关 疾病临床鉴别诊断和科研项目提供检测和技术支持。 附图说明 图1本发明设置门为CD3阴性的示意图; 图2本发明设置门为CCR3阳性的示意图; 图3为本发明的阳性对照活化的嗜碱性粒细胞; 图4为本发明的阴性对照活化的嗜碱性粒细胞; 图5为本发明的阳性对照中所有CD203c阳性细胞表达CD203c的平均荧光强度; 图6为本发明的阳性对照的脱粒细胞和未脱粒细胞的点阵图; 图7为本发明的阴性对照的脱粒细胞和未脱粒细胞的点阵图。












