技术摘要:
本发明涉及安全性和抗癌作用有所改善的溶瘤病毒及其用途。通过将编码HSV‑TK片段的基因插入TK基因区域以缺失牛痘病毒的TK,可以获得本发明的安全性和抗癌作用得到改善的溶瘤病毒。另外,本发明的溶瘤病毒表达HSV‑TK片段以使GCV磷酸化,从而可以杀死被溶瘤病毒感染的癌 全部
背景技术:
随着基因重组技术的全面应用,人们已经开始了使用具有提高的肿瘤选择性和抗 癌功效的溶瘤病毒的临床研究。文献中报道的第一种重组溶瘤病毒是单纯疱疹病毒。从那 时起,人们就积极开展了使用其他病毒进行溶瘤的研究(Martuza等,1991年;Hwang等,2011 年;Kaufaman等,2015年;Khuri等,2000年;Park等,2008年)。 由于最近在美国和欧洲,基于疱疹病毒的T-Vec (溶瘤病毒,Talimogene laherparepvec)在治疗晚期黑素瘤方面的成功商业化,溶瘤病毒的使用受到了广泛关注。 同时,缺乏胸腺嘧啶激酶(TK)基因的牛痘病毒具有很大的临床实用性,但是由于其狭窄的 治疗窗口,在最大化其临床效果方面存在限制。缺乏TK的牛痘病毒的治疗范围狭窄,这意味 着高病毒剂量具有很大的临床疗效,但由于病毒的毒性而具有临床风险。 实际上,在Pexa-Vec(JX-594;SillaJen公司)的II期临床试验中(该试验在三十 (30)例原发性肝癌患者中进行),结果表明,与低剂量组(108pfu)相比,高剂量组(109pfu)的 生存率有所增加(Heo等,2013年)。但是,在进行肿瘤内给药的I期临床试验中,在3x109pfu 处观察到剂量限制性毒性(DLT),从而最大耐受剂量(MTD)被限制为1x109pfu。据报道,这与 药物无关。但是,已经报道了许多溶瘤病毒治疗后不久死亡的病例,这表明不需要的病毒复 制可能会导致不可预测的结果。这些剂量依赖性的功效增加和剂量限制性毒性表明,需要 开发更安全、更有效的牛痘病毒。 另一方面,更昔洛韦(GCV)是抗单纯疱疹病毒、巨细胞病毒和水痘带状疱疹病毒的 抗病毒药物。当与单纯疱疹病毒的TK结合时,GCV的5’端被磷酸化,然后转化为更昔洛韦三 磷酸(GCV-TP)。GCV-TP抑制病毒DNA聚合酶的活性,并附着在病毒DNA的3’端,从而终止DNA 延伸。GCV-TP是一种剧毒物质,它可以通过阻止细胞中的DNA合成而表现出细胞毒性。 目前,已有研究通过将HSV-TK插入溶瘤病毒中以通过共同施用GCV来诱导癌细胞 凋亡,从而在溶瘤病毒治疗中使用HSV-TK/GCV系统。在这种疗法中,首先溶瘤病毒感染肿瘤 细胞以诱导直接的抗癌作用,并且被HSV1-TK(自杀基因)磷酸化的GCV抑制肿瘤细胞的增 殖,从而展现出额外的抗癌作用(Oliver W等,人类基因疗法,第10卷,第16期,1999年)。 HSV1-TK/GCV系统主要用于以腺病毒为载体的溶瘤病毒疗法。但是,共同施用GCV预期产生 的其他细胞毒性作用仍存在争议。 特别是,观察到当带有HSV-TK的具有复制能力的腺病毒与GCV联合施用时,对神经 胶质瘤细胞的细胞毒性作用显著增强。但是,并非所有研究都显示出一致的结果 (Lambright ES等,基因疗法,第8页:946-53)。其原因是HSV-TK/GCV系统不仅涉及病毒复 制,而且还涉及肿瘤细胞增殖,其总作用由于冲突作用而被抵消(Widner O、Morris JC, 2000年)。 因此,有必要研究在将HSV-TK/GCV系统应用于溶瘤病毒疗法中同时确保安全性并 5 CN 111556899 A 说 明 书 2/17 页 且增强抗癌作用的具体方法。
技术实现要素:
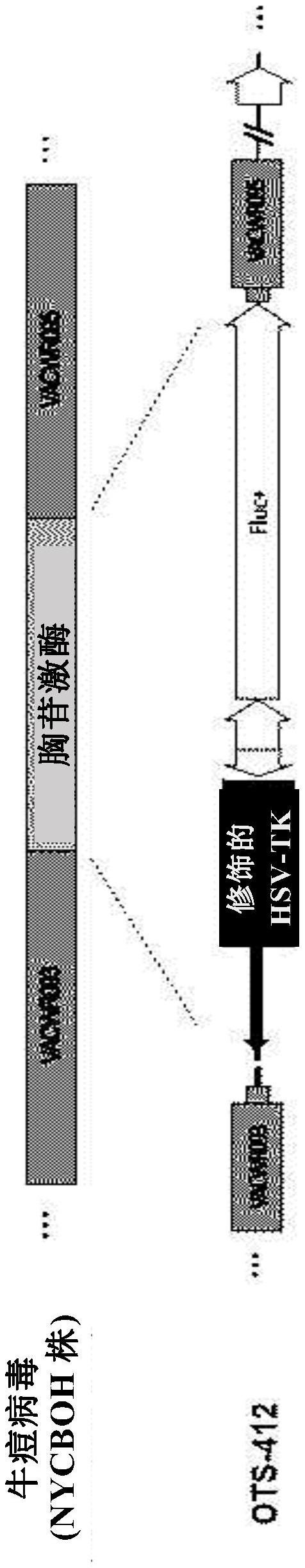
技术问题 因此,本发明人已经进行了研究以开发具有改善的安全性和抗癌作用的溶瘤病 毒,并且通过开发包含编码HSV1-TK片段的基因(HSV1-TKmut)的重组牛痘病毒(其中HSV1- TK的C端部分被截短或者是其变体),并证实重组牛痘病毒与GCV联合施用具有良好的安全 性和抗癌作用,来完成了本发明。 解决方案 为了实现上述目的,本发明的一个方面提供了一种重组病毒载体,其包含编码 HSV-TK(单纯疱疹病毒胸苷激酶)片段或其变体的核苷酸序列。 本发明的另一方面提供了一种溶瘤病毒,其包含编码HSV-TK片段或其变体的核苷 酸序列。 本发明的另一方面提供了一种用于治疗癌症的药物组合物,其包含所述溶瘤病 毒。 本发明的另一方面提供了一种用于治疗癌症的药物组合物,其包含所述溶瘤病 毒,和GCV(更昔洛韦)或ACV(阿昔洛韦)作为活性成分。 本发明的另一方面提供了一种治疗癌症的方法,其包括施用所述溶瘤病毒,和GCV 或ACV。 本发明的另一方面提供了一种制备重组牛痘病毒的方法,其包括以下步骤:i)将 包含编码HSV-TK片段或其变体的核苷酸序列的穿梭质粒转染到宿主细胞中,并且用野生型 牛痘病毒处理所述宿主细胞;ii)培养所述宿主细胞;和iii)从培养物中获得重组牛痘病 毒。 本发明的另一方面提供了所述溶瘤病毒在治疗癌症中的用途。 本发明的另一方面提供了所述药物组合物在治疗癌症中的用途。 本发明的另一方面提供了所述溶瘤病毒在制备用于治疗癌症的药物中的用途。 本发明的另一方面提供了所述药物组合物在制备用于治疗癌症的药物中的用途。 发明的有益效果 具有改善的安全性和抗癌作用的本发明的溶瘤病毒归因于其编码HSV-TK片段或 其变体的编码基因,其被插入到牛痘病毒的天然TK基因的缺失区域中。此外,本发明的溶瘤 病毒可以表达HSV-TK片段或其变体以使GCV磷酸化,从而杀死被溶瘤病毒感染的癌细胞,甚 至杀死周围的癌细胞。此外,GCV还可以抑制病毒复制,因此在施用高剂量病毒的情况下,它 可以控制由病毒引起的不良副作用。此外,尽管由于GCV抑制病毒复制,病毒颗粒的数量减 少了,但其抗癌作用却增强了。因此,具有改善的安全性和抗癌作用的本发明的溶瘤病毒可 以用于治疗癌症。 附图简要说明 图1是用于制备重组牛痘病毒的携带HSV1-TK基因的穿梭质粒载体的示意图。 图2是显示重组牛痘病毒的一个实例(OTS-412)的示意图,其中HSV1-TKmut基因和 萤火虫荧光素酶基因被插入其TK基因区域。 6 CN 111556899 A 说 明 书 3/17 页 图3显示了制备表达HSV1-TK片段的重组牛痘病毒(OTS-412)的步骤。 图4描绘了用于确认HSV1-TK片段在OTS-412中的表达的蛋白质印迹的结果。 图5显示了用于确认HSV1-TKmut基因在OTS-412DNA中的插入的限制性内切酶图谱 的结果。 图6显示了在HCT-116癌细胞系中感染24和48小时后,OTS-412的复制的图。 图7显示了在OTS-412处理的NCI-H460和NCI-H23癌细胞系中,GCV对病毒复制的抑 制的图。 图8显示了在OTS-412处理的HCT-116癌细胞系中,GCV对细胞毒性的增强的图。 图9显示了分别单独施用OTS-412或将其与GCV联合施用后,A549、NCI-H460、HT-29 和HCT-116癌细胞系的细胞生存力的图。 图10显示了分别施用GCV、OTS-412,或联合施用OTS-412和GCV后,A549和NCI-H460 癌细胞系的凋亡和坏死模式。 图11显示了分别施用GCV、OTS-412,或联合施用OTS-412和GCV后,A549和NCI-H460 癌细胞系的细胞生存力的图。 图12显示了对移植有HCT-116癌细胞系的小鼠施用盐水、OTS-412或联合施用OTS- 412和GCV后12天,肿瘤大小变化的图。 图13是生物发光图像,其显示了在向小鼠施用PBS、OTS-412,或联合施用OTS-412 和GCV后,在移植有HCT-116癌细胞系的小鼠中OTS-412的分布。 图14显示了在单独施用OTS-412或将其与GCV联合施用于小鼠后,从移植有HCT- 116癌细胞系的小鼠获得的肿瘤组织中计数的病毒DNA拷贝数的图。 图15显示了向HCT-116荷瘤小鼠施用盐水、OTS-412,或联合施用OTS-412和GCV后 12天,体重变化的图。 图16显示了在向Renca荷瘤小鼠施用盐水、OTS-412,或联合施用OTS-412和GCV后 24天,肿瘤大小的变化的图。 图17显示了在施用盐水、OTS-412,或联合施用OTS-412和GCV后,从Renca荷瘤小鼠 获得的肿瘤组织中的病毒颗粒总数目的图。 图18显示了对小鼠施用盐水、OTS-412,或联合施用OTS-412和GCV后,从移植有 Renca癌细胞系的小鼠获得的肿瘤组织的TUNEL染色结果。 图19显示了在对小鼠施用盐水、OTS-412,或联合施用OTS-412和GCV后,从移植有 Renca癌细胞系的小鼠获得的肿瘤组织的TUNEL染色中观察到的凋亡部分的定量的图。 图20显示了在向HCT-116荷瘤小鼠施用盐水、OTS-412,或联合施用OTS-412和GCV 后21天,肿瘤大小变化的图。 图21显示了在施用盐水、OTS-412,或联合施用OTS-412和GCV后,从移植有HCT-116 癌细胞系的小鼠获得的肿瘤组织的免疫组织化学(IHC)结果。 图22显示了在施用盐水、OTS-412,或联合施用OTS-412和GCV后,从移植有HCT-116 癌细胞系的小鼠获得的肿瘤组织的免疫组织化学(IHC)结果中观察到的染色部分的定量的 图。 图23显示了在施用盐水、OTS-412,或联合施用OTS-412和GCV后,从移植有HCT-116 癌细胞系的小鼠获得的肿瘤组织的H&E染色中观察到的坏死部分的定量的图。 7 CN 111556899 A 说 明 书 4/17 页 图24显示了在对小鼠施用盐水、OTS-412,或联合施用OTS-412和GCV后,从HCT-116 荷瘤小鼠获得的肿瘤组织的H&E染色所得到的后肿瘤存活区的图。 图25显示了对移植有HCT-116癌细胞系的小鼠施用盐水、OTS-412或其组合21天, 用OTS-412和GCV处理的每组小鼠的体重的图。 图26显示了用OTS-412处理后,十三(13)种不同癌细胞系的细胞生存力评估的图。 图27显示了在HCT-116、SK-MEL-28和DU145癌细胞系中施用的OTS-412的IC50的图。 图28是生物发光图像,其显示了在第3天和第7天在HCT-116荷瘤小鼠中腹膜内注 射的OTS-412的病毒分布。 本发明的最佳实施方式 在下文中,将详细描述本发明。 本发明提供了一种重组病毒载体,其包含编码HSV-TK(单纯疱疹病毒胸苷激酶)片 段或其变体的核苷酸序列。 如本文所用,术语“TK(胸苷激酶)”是指胸苷激酶,其是参与核苷酸的生物合成的 酶。TK是一种酶,用于细胞和病毒中核苷酸的生物合成。TK可能源自单纯疱疹病毒。此处,所 述单纯疱疹病毒可以是1型单纯疱疹病毒(HSV1)或2型单纯疱疹病毒(HSV2)。 如本文所用,术语“HSV-TK(单纯疱疹病毒胸苷激酶)”是指单纯疱疹病毒的胸苷激 酶。具体而言,HSV-TK可以是HSV1-TK(1型单纯疱疹病毒胸苷激酶)。HSV1-TK是一种在单纯 疱疹病毒的DNA合成过程中参与初始磷酸化反应的酶。HSV-TK还参与抗病毒剂GCV(更昔洛 韦)或ACV(阿昔洛韦)的磷酸化。特别是,对于GCV或ACV,HSV1-TK的敏感度是其他类型病毒 中存在的其他任何TK的十倍左右。 如本文所用,术语“HSV-TK片段”是指HSV-TK的一些氨基酸残基缺失后的片段。具 体地,所述HSV-TK片段可以是其中HSV-TK的N-末端或C-末端的一部分缺失后的片段。优选 地,所述HSV-TK片段可以是其中HSV-TK的C-末端的一部分被缺失后的片段。在一个实施方 式中,所述HSV-TK片段可以是HSV-TK的C-末端的1至195个氨基酸残基连续缺失后的片段。 所述HSV-TK片段可以是其中HSV-TK的C-末端的1个、2个、3个、4个、5个、6个、7个、8个、9个、 10个、11个、12个、13个、14个、15个、16个、17个、18个、19个、20个、21个、22个、23个、24个、25 个、26个、27个、28个、29个、30个、31个、32个、33个、34个、35个、36个、37个、38个、39个、40 个、41个、42个、43个、44个、45个、46个、47个、48个、49个、50个、60个、70个、80个、90个、100 个、110个、120个、130个、140个、150个、160个、170个、180个、190个,或195个氨基酸残基连 续缺失后的片段。 本发明的HSV1-TK片段或其变体可以源自通过诱导适应性进化而突变的病毒。为 了开发表达优化的HSV1-TK片段或其变体的牛痘病毒,本发明人制备了含有HSV1-TK基因的 重组牛痘病毒,并在不存在TK的情况下诱导了适应性进化。对所得的重组牛痘病毒进行用 于确认荧光素酶活性的实验、基因组分析以及用于确认对GCV的敏感性的实验,并且筛选了 表达HSV1-TK片段或其变体的牛痘病毒OTS-412。尽管HSV1-TK的C-末端有重要的截短,但 HSV1-TK片段或其变体仍对GCV敏感。此外,已经证实,当将表达HSV1-TK片段或其变体的牛 痘病毒与GCV联合施用时,抗癌作用增强。 所述HSV-TK片段可以是HSV1-TK片段。HSV1-TK片段的一个实施方式可以是以下片 段中的任何一个:SEQ ID NO:1所示的氨基酸序列的C-末端有1至195个、24至149个,或30至 8 CN 111556899 A 说 明 书 5/17 页 46个氨基酸残基连续缺失后的片段。具体地,所述HSV-TK片段可以是以下片段之一:SEQ ID NO:1所示的氨基酸序列的C-末端的1个、2个、3个、4个、5个、6个、7个、8个、9个、10个、11个、 12个、13个、14个、15个、16个、17个、18个、19个、20个、21个、22个、23个、24个、25个、26个、27 个、28个、29个、30个、31个、32个、33个、34个、35个、36个、37个、38个、39个、40个、41个、42 个、43个、44个、45个、46个、47个、48个、49个、50个、60个、70个、80个、90个、100个、110个、 120个、130个、140个、150个、160个、170个、180个、190个,或195个氨基酸残基连续缺失后的 片段。优选地,所述HSV1-TK片段可以是以下片段之一:SEQ ID NO:1所示的氨基酸序列的C- 末端的24个、30个、70个、99个、149个或195个氨基酸残基连续缺失后的片段。所述HSV1-TK 片段可能由于C-末端某些氨基酸残基的缺失而降低了对GCV的敏感性。 所述HSV1-TK片段的实例可以是以下片段之一:SEQ ID NO:1所示的氨基酸序列的 C-末端的195个、149个、99个、70个、46个、30个或24个氨基酸残基连续缺失后的片段。具体 地,所述HSV1-TK片段可以具有选自下组的任何一种氨基酸序列:SEQ ID NO:2-6。 编码所述HSV1-TK片段的核苷酸序列可以是编码以下任何HSV1-TK片段的核苷酸 序列:SEQ ID NO:1所示的氨基酸序列的C-末端的1至195个、24至149个,或30至46个氨基酸 残基连续缺失后的片段。具体而言,编码所述HSV1-TK片段的核苷酸序列可以是编码以下任 何一种氨基酸序列的核苷酸序列:SEQ ID NO:2-6。优选地,编码所述HSV1-TK片段的核苷酸 序列可以是SEQ ID NO:9所示的核苷酸序列。 所述HSV-TK片段的变体可以是HSV1-TK片段的变体。具体地,所述HSV1-TK片段的 变体可以是构成所述HSV1-TK片段的至少一个氨基酸残基被取代的变体。特别地,所述 HSV1-TK片段的变体可以包含如SEQ ID NO:1所示的氨基酸序列的第1位至第145位氨基酸 残基。在一个实施方式中,所述HSV1-TK片段的变体可以具有如SEQ ID NO:7或8所示的氨基 酸序列。编码所述HSV1-TK片段的变体的核苷酸序列可以是SEQ ID NO:10或11。 病毒载体是用于将基因导入细胞或产生病毒的载体。所述病毒载体可以衍生自腺 病毒、单纯疱疹病毒、慢病毒、逆转录病毒、腺相关病毒、牛痘病毒或痘病毒。 本发明的另一方面提供了一种溶瘤病毒,其包含编码HSV-TK片段或其变体的核苷 酸序列。 如本文所用,术语“溶瘤病毒”是指破坏癌细胞的重组病毒,所述病毒的基因被操 纵以在癌细胞中特异性复制。所述溶瘤病毒可以衍生自腺病毒、单纯疱疹病毒、麻疹病毒、 慢病毒、逆转录病毒、巨细胞病毒、杆状病毒、呼肠孤病毒、腺相关病毒、粘液瘤病毒、水疱性 口炎病毒、脊髓灰质炎病毒、新城疫病毒、细小病毒、柯萨奇病毒、塞内卡病毒、牛痘病毒或 痘病毒。优选地,所述溶瘤病毒可以衍生自牛痘病毒。 所述牛痘病毒可以是西储(Western Reserve)(WR)、NYVAC(纽约牛痘病毒)、Wyeth (纽约市卫生局;NYCBOH)、LC16m8、李斯特(Lister)、哥本哈根(Copenhagen)、天坛(Tian Tan)、USSR、塔什干(TashKent),埃文斯(Evans)、IHD-J(国际卫生科-J)或IHD-W(国际卫生 科-白)菌株,但不限于此。 所述HSV-TK片段可以是HSV1-TK片段。HSV1-TK片段的一个实施方式可以是以下片 段中的任何一个:SEQ ID NO:1所示的氨基酸序列的C-末端的1至195个、24至149个,或30至 46个氨基酸残基连续缺失后的片段。具体地,所述HSV-TK片段可以是以下片段之一:SEQ ID NO:1所示的氨基酸序列的C-末端的1个、2个、3个、4个、5个、6个、7个、8个、9个、10个、11个、 9 CN 111556899 A 说 明 书 6/17 页 12个、13个、14个、15个、16个、17个、18个、19个、20个、21个、22个、23个、24个、25个、26个、27 个、28个、29个、30个、31个、32个、33个、34个、35个、36个、37个、38个、39个、40个、41个、42 个、43个、44个、45个、46个、47个、48个、49个、50个、60个、70个、80个、90个、100个、110个、 120个、130个、140个、150个、160个、170个、180个、190个,或195个氨基酸残基连续缺失后的 片段。优选地,所述HSV1-TK片段可以是以下片段之一:SEQ ID NO:1所示的氨基酸序列的C- 末端的24个、30个、70个、99个、149个或195个氨基酸残基连续缺失后的片段。所述HSV1-TK 片段可能由于C-末端某些氨基酸残基的缺失而降低了对GCV的敏感性。 所述HSV1-TK片段的实例可以是以下片段之一:SEQ ID NO:1所示的氨基酸序列的 C-末端的195个、149个、99个、70个、46个、30个或24个氨基酸残基连续缺失后的片段。具体 地,所述HSV1-TK片段可以具有选自下组的任何一种氨基酸序列:SEQ ID NO:2-6。 编码所述HSV1-TK片段的核苷酸序列可以是编码以下任何HSV1-TK片段的核苷酸 序列:SEQ ID NO:1所示的氨基酸序列的C-末端的1至195个、24至149个,或30至46个氨基酸 残基连续缺失后的片段。具体而言,编码所述HSV1-TK片段的核苷酸序列可以是编码以下任 何一种氨基酸序列的核苷酸序列:SEQ ID NO:2-6。优选地,编码所述HSV1-TK片段的核苷酸 序列可以是SEQ ID NO:9所示的核苷酸序列。 所述HSV-TK片段的变体可以是HSV1-TK片段的变体。具体地,所述HSV1-TK片段的 变体可以是构成所述HSV1-TK片段的至少一个氨基酸残基被取代的变体。特别地,所述 HSV1-TK片段的变体可以包含如SEQ ID NO:1所示的氨基酸序列的第1位至第145位氨基酸 残基。在一个实施方式中,所述HSV1-TK片段的变体可以具有如SEQ ID NO:7或8所示的氨基 酸序列。编码所述HSV1-TK片段的变体的核苷酸序列可以是SEQ ID NO:10或11。 所述溶瘤病毒可能缺失了天然TK基因。具体而言,所述溶瘤病毒可以是通过将编 码所述HSV1-TK片段的核苷酸序列插入到或取代天然TK基因区域中而缺失天然TK基因的病 毒。在本发明的一个实施方式中,通过将编码所述HSV1-TK片段的核苷酸序列插入牛痘病毒 的天然TK基因区域中来缺失痘苗病毒的天然TK基因。 如本文所用,属于“基因缺失”是指由于基因的部分或全部缺失或外源基因插入到 所述基因,而导致的所述基因不表达。部分基因缺失可以是5’末端或3’末端的部分缺失。 即,所述溶瘤病毒的天然TK基因可以被部分或全部缺失。 在本发明的一个实例中,将包含编码所述HSV-TK片段的基因的重组牛痘病毒OTS- 412感染到HCT-116癌细胞系中,并确认了感染和复制效率(图6)。此外,在十三(13)种不同 的癌细胞系中施用OTS-412,并且在培养72小时后,测量细胞活力以显示出OTS-412的细胞 毒性(图26)。因此,包含编码所述HSV-TK片段的核苷酸序列的本发明的溶瘤病毒可有效地 用于治疗癌症。 本发明的另一方面提供了一种用于预防或治疗癌症的药物组合物,其包含溶瘤病 毒作为活性成分,所述溶瘤病毒包含编码所述HSV-TK片段或其变体的核苷酸序列。 包含在所述药物组合物中作为活性成分的溶瘤病毒如上所述。 所述溶瘤病毒的剂量根据个体的状况和体重、疾病的严重程度、药物的类型、给药 的途径和时间而变化,并且可以由本领域技术人员适当地选择。所述剂量可以是使患者接 受1×103至1×1018个病毒颗粒、传染性病毒单位(TCID50)或噬菌斑形成单位(pfu)。具体地, 所述剂量可以是1×103、2×103、5×103、1×104、2×104、5×104、1×105、2×105、5×105、1× 10 CN 111556899 A 说 明 书 7/17 页 106、2×106、5×106、1×107、2×107、5×107、1×108、2×108、5×108、1×109、2×109、5×109、 1×1010、5×1010、1×1011、5×1011、1×1012、1×1013、1×1014、1×1015、1×1016、1×1017、1× 1018或更多个病毒颗粒、传染性病毒单位(TCID50)或噬菌斑形成单元(pfu),其中可以包括 它们之间的各种值和范围。优选地,所述溶瘤病毒可以以1×103至1×1010pfu的剂量施用。 在本发明的一个实例中,所述溶瘤病毒以1×106、1×107和1×108pfu的剂量施用。 癌症可以选自下组:肺癌、大肠癌、前列腺癌、甲状腺癌、乳腺癌、脑癌、头颈癌、食 道癌、皮肤癌、胸腺癌、胃癌、结肠癌、肝癌、卵巢癌、子宫癌、膀胱癌、直肠癌、胆囊癌、胆道 癌、胰腺癌、非小细胞肺癌、骨癌、眼内黑素瘤、肛周癌、输卵管癌、子宫内膜癌、子宫颈癌、阴 道癌、外阴癌、霍奇金斯病、小肠癌、内分泌腺癌、甲状旁腺癌、肾上腺癌、软组织肉瘤、尿道 癌、阴茎癌、慢性白血病、急性白血病、淋巴细胞性淋巴瘤、肾癌、输尿管癌、肾细胞癌、肾盂 癌、中枢神经系统肿瘤、原发性中枢神经系统淋巴瘤、脊髓肿瘤、脑干神经胶质瘤、垂体腺 瘤,或其组合。 本发明的药物组合物可以进一步包含生理上可接受的载体。另外,本发明的药物 组合物可进一步包含常规用于制备药物组合物的合适的赋形剂和稀释剂。另外,可以根据 常规方法将其配制成注射剂形式。 可以将所述药物组合物配制成用于肠胃外给药的无菌水溶液、非水溶液、悬浮液、 乳剂、冻干制剂、栓剂等。对于非水溶液和悬浮液,可以使用丙二醇、聚乙二醇、植物油(例如 橄榄油)、可注射酯(例如油酸乙酯)等。作为栓剂基质,可以使用WitepsolTM、聚乙二醇 (macrogol)、TweenTM61、可可脂、月桂脂、甘油明胶等。 所述药物组合物可以以各种途径和量施用于受试者,这取决于患者的状况以及是 否存在副作用,并且本领域技术人员可以在合适的范围内选择最佳的给药途径、剂量和频 率。另外,所述药物组合物可以与疾病治疗效果已知的其他药物或生理活性物质联合施用, 或者可以与其他药物组合配制。 所述药物组合物可以肠胃外给药,包括瘤内、腹膜内、皮下、皮内、结节内和静脉内 施用等。优选地,它可以是瘤内、腹膜内或静脉内施用。另一方面,所述药物组合物的剂量可 以根据施用方案、剂量和患者的健康状况来确定。 本发明人在A549、NCI-H460、HT-29和HCT-116癌细胞系中将OTV-412与GCV联合施 用、评估了癌细胞系的存活力,并证实了通过联合治疗提高了抗癌作用(图9)。另外,已确认 即使将OTS-412和GCV联合施用于癌细胞系,该病毒也保持一定水平的复制能力(图14)。因 此,包含编码所述HSV-TK片段或其变体的核苷酸序列的溶瘤病毒与GCV的组合可有效地用 于治疗癌症。 本发明的另一方面提供了一种用于预防或治疗癌症的药物组合物,其包含溶瘤病 毒,以及GCV(更昔洛韦)或ACV(阿昔洛韦)作为有效成分,所述溶瘤病毒包含编码所述HSV- TK片段或其变体的核苷酸序列。 所述药物组合物中包含的溶瘤病毒和GCV或ACV可以同时、顺序或以相反顺序施 用。具体地,可以同时施用药物组合物中包含的所述溶瘤病毒和GCV或ACV。另外,可以首先 施用所述溶瘤病毒,然后施用GCV或ACV。另外,首先施用溶瘤病毒,然后施用GCV或ACV,然后 再次施用溶瘤病毒。 包含在所述药物组合物中作为活性成分的溶瘤病毒如上所述。 11 CN 111556899 A 说 明 书 8/17 页 所述溶瘤病毒的剂量根据个体的状况和体重、疾病的严重程度、药物的类型、给药 的途径和时间而变化,并且可以由本领域技术人员适当地选择。所述剂量可以是使患者接 受1×103到1×1018个病毒颗粒、传染性病毒单位(TCID50)或噬菌斑形成单位(pfu)。具体地, 所述剂量可以是1×103、2×103、5×103、1×104、2×104、5×104、1×105、2×105、5×105、1× 106、2×106、5×106、1×107、2×107、5×107、1×108、2×108、5×108、1×109、2×109、5×109、 1×1010、5×1010、1×1011、5×1011、1×1012、1×1013、1×1014、1×1015、1×1016、1×1017、1× 1018或更多个病毒颗粒、传染性病毒单位(TCID50)或噬菌斑形成单位(pfu),其中可以包括 它们之间的各种值和范围。优选地,所述溶瘤病毒可以以1×103至1×1010pfu的剂量施用。 在本发明的一个实例中,所述溶瘤病毒以1×106、1×107和1×108pfu的剂量施用。 如本文所用,术语“GCV”是指一种抗病毒剂,其被称为更昔洛韦,并且其对单纯疱 疹病毒、巨细胞病毒和水痘带状疱疹病毒有效。GCV在5’端被病毒的TK磷酸化,然后转化为 更昔洛韦三磷酸(GCV-TP)。GCV-TP抑制病毒DNA聚合酶的活性,并附着在病毒DNA的3’端,从 而终止DNA延伸。另外,磷酸化的GCV可以阻止细胞DNA复制,从而抑制细胞生长。GCV由以下 式1表示。 [式1] 如本文所用,术语“ACV”是指一种抗病毒剂,其被称为阿昔洛韦,并且其对单纯疱 疹病毒、水痘带状疱疹病毒和爱泼斯坦-巴尔病毒有效。ACV被病毒的TK磷酸化,然后转化为 阿昔洛韦三磷酸(ACV-TP)。ACV-TP抑制病毒DNA聚合酶的活性,并附着在病毒DNA的3’端,从 而终止DNA延伸。ACV由以下式2表示。 [式2] 此外,GCV或ACV的日剂量可以是0.1μg/kg至50mg/kg。具体来说,GCV或ACV的日剂 量可以是0.1μg/kg至50mg/kg、1μg/kg至40mg/kg、5μg/kg至30mg/kg,或10μg/kg至20mg/kg。 在本发明的一个实例中,以50mg/kg的日剂量施用GCV。 癌症可以选自下组:肺癌、大肠癌、前列腺癌、甲状腺癌、乳腺癌、脑癌、头颈癌、食 道癌、皮肤癌、胸腺癌、胃癌、结肠癌、肝癌、卵巢癌、子宫癌、膀胱癌、直肠癌、胆囊癌、胆道 癌、胰腺癌、非小细胞肺癌、骨癌、眼内黑素瘤、肛周癌、输卵管癌、子宫内膜癌、子宫颈癌、阴 道癌、外阴癌、霍奇金斯病、小肠癌、内分泌腺癌、甲状旁腺癌、肾上腺癌、软组织肉瘤、尿道 癌、阴茎癌、慢性白血病、急性白血病、淋巴细胞性淋巴瘤、肾癌、输尿管癌、肾细胞癌、肾盂 癌、中枢神经系统肿瘤、原发性中枢神经系统淋巴瘤、脊髓肿瘤、脑干神经胶质瘤、垂体腺 12 CN 111556899 A 说 明 书 9/17 页 瘤,或其组合。 本发明的药物组合物可以进一步包含生理上可接受的载体。另外,本发明的药物 组合物可进一步包含常规用于制备药物组合物的合适的赋形剂和稀释剂。另外,可以根据 常规方法将其配制成注射剂形式。 可以将所述药物组合物配制成用于肠胃外给药的灭菌水溶液、非水溶液、悬浮液、 乳剂、冻干制剂、栓剂等。对于非水溶液和悬浮液,可以使用丙二醇、聚乙二醇、植物油(例如 橄榄油)、可注射酯(例如油酸乙酯)等。作为栓剂基质,可以使用WitepsolTM、聚乙二醇 (macrogol)、TweenTM61、可可脂、月桂脂、甘油明胶等。 所述药物组合物可以以各种途径和量施用于受试者,这取决于患者的状况以及是 否存在副作用,并且本领域技术人员可以在合适的范围内选择最佳的给药途径、剂量和频 率。另外,所述药物组合物可以与疾病治疗效果已知的其他药物或生理活性物质联合施用, 或者可以与其他药物组合制剂的形式配制。 所述药物组合物可以肠胃外给药,包括瘤内、腹膜内、皮下、皮内、结节内和静脉内 施用等。优选地,它可以是瘤内、腹膜内或静脉内施用。另一方面,所述药物组合物的剂量可 以根据施用方案、剂量和患者的健康状况来确定。 本发明的另一方面提供了一种治疗癌症的方法,包括向有所需要的个体施用溶瘤 病毒以及GCV或ACV,所述溶瘤病毒包含编码所述HSV-TK片段或其变体的核苷酸序列。 所述溶瘤病毒、GCV和ACV如上所述。 所述溶瘤病毒的剂量根据个体的状况和体重、疾病的严重程度、药物的类型、给药 的途径和时间而变化,并且可以由本领域技术人员适当地选择。所述剂量可以是使患者接 受1×103到1×1018个病毒颗粒、传染性病毒单位(TCID50)或噬菌斑形成单位(pfu)。具体地, 所述剂量可以是1×103、2×103、5×103、1×104、2×104、5×104、1×105、2×105、5×105、1× 106、2×106、5×106、1×107、2×107、5×107、1×108、2×108、5×108、1×109、2×109、5×109、 1×1010、5×1010、1×1011、5×1011、1×1012、1×1013、1×1014、1×1015、1×1016、1×1017、1× 1018或更多个病毒颗粒、传染性病毒单位(TCID50)或噬菌斑形成单位(pfu),其中可以包括 它们之间的各种值和范围。优选地,所述溶瘤病毒可以以1×103至1×1010pfu的剂量施用。 在本发明的一个实例中,所述溶瘤病毒以1×106、1×107和1×108pfu的剂量施用。 另外,GCV或ACV可以以0.1μg/kg至50mg/kg的日剂量施用。具体来说,GCV或ACV的 日剂量可以是0.1μg/kg至50mg/kg、1μg/kg至40mg/kg、5μg/kg至30mg/kg,或10μg/kg至 20mg/kg。在本发明的一个实例中,以50mg/kg的日剂量施用GCV。 在溶瘤病毒施用期间或之后,GCV或ACV至少施用一次。具体而言,GCV或ACV可以在 施用溶瘤病毒后24小时开始施用约2周。施用溶瘤病毒后,GCV或ACV可以每周两次连续施用 5至18天。 癌症可以选自下组:肺癌、大肠癌、前列腺癌、甲状腺癌、乳腺癌、脑癌、头颈癌、食 道癌、皮肤癌、胸腺癌、胃癌、结肠癌、肝癌、卵巢癌、子宫癌、膀胱癌、直肠癌、胆囊癌、胆道 癌、胰腺癌、非小细胞肺癌、骨癌、眼内黑素瘤、肛周癌、输卵管癌、子宫内膜癌、子宫颈癌、阴 道癌、外阴癌、霍奇金斯病、小肠癌、内分泌腺癌、甲状旁腺癌、肾上腺癌、软组织肉瘤、尿道 癌、阴茎癌、慢性白血病、急性白血病、淋巴细胞性淋巴瘤、肾癌、输尿管癌、肾细胞癌、肾盂 癌、中枢神经系统肿瘤、原发性中枢神经系统淋巴瘤、脊髓肿瘤、脑干神经胶质瘤、垂体腺 13 CN 111556899 A 说 明 书 10/17 页 瘤,或其组合。 本发明的药物组合物可以进一步包含生理上可接受的载体。另外,本发明的药物 组合物可进一步包含常规用于制备药物组合物的合适的赋形剂和稀释剂。另外,可以根据 常规方法将其配制成注射剂形式。 可以将所述药物组合物配制成用于肠胃外给药的灭菌水溶液、非水溶液、悬浮液、 乳剂、冻干制剂、栓剂等。对于非水溶液和悬浮液,可以使用丙二醇、聚乙二醇、植物油(例如 橄榄油)、可注射酯(例如油酸乙酯)等。作为栓剂基质,可以使用WitepsolTM、聚乙二醇 (macrogol)、TweenTM61、可可脂、月桂脂、甘油明胶等。 所述药物组合物可以以各种途径和量施用于受试者,这取决于患者的状况以及是 否存在副作用,并且本领域技术人员可以在合适的范围内选择最佳的给药途径、剂量和频 率。另外,所述药物组合物可以与疾病治疗效果已知的其他药物或生理活性物质联合施用, 或者可以与其他药物联合配制。 所述药物组合物可以肠胃外给药,包括瘤内、腹膜内、皮下、皮内、结节内和静脉内 施用等。优选地,它可以是瘤内、腹膜内或静脉内施用。另一方面,所述药物组合物的剂量可 以根据施用方案、剂量和患者的健康状况来确定。 如本文所用,术语“个体”是指可以通过施用本发明的靶向癌细胞的组合物来缓 解、抑制或治疗疾病的人,或患有所述疾病的人。 另外,所述溶瘤病毒和GCV可以与疾病治疗效果已知的其他药物或生理活性物质 联合施用,或者可以与其他药物组合制剂的形式配制。 本发明的另一方面提供了一种制备表达HSV-TK片段或其变体的重组牛痘病毒的 方法,包括步骤:i)将包含编码HSV-TK片段或其变体的核苷酸序列的穿梭质粒转染到宿主 细胞中,并且用野生型牛痘病毒处理所述宿主细胞;ii)培养所得宿主细胞;和iii)从所得 培养物中获得重组牛痘病毒。 所述HSV-TK片段可以是HSV1-TK片段。HSV1-TK片段的一个实施方式可以是以下片 段中的任何一个:SEQ ID NO:1所示的氨基酸序列的C-末端的1至195个、24至149个,或30至 46个氨基酸残基连续缺失后的片段。具体地,所述HSV-TK片段可以是以下片段之一:SEQ ID NO:1所示的氨基酸序列的C-末端的1个、2个、3个、4个、5个、6个、7个、8个、9个、10个、11个、 12个、13个、14个、15个、16个、17个、18个、19个、20个、21个、22个、23个、24个、25个、26个、27 个、28个、29个、30个、31个、32个、33个、34个、35个、36个、37个、38个、39个、40个、41个、42 个、43个、44个、45个、46个、47个、48个、49个、50个、60个、70个、80个、90个、100个、110个、 120个、130个、140个、150个、160个、170个、180个、190个,或195个氨基酸残基连续缺失后的 片段。优选地,所述HSV1-TK片段可以是以下片段之一:SEQ ID NO:1所示的氨基酸序列的C- 末端的24个、30个、70个、99个、149个或195个氨基酸残基连续缺失后的片段。所述HSV1-TK 片段可能由于C-末端某些氨基酸残基的缺失而降低了对GCV的敏感性。 所述HSV1-TK片段的实例可以是以下片段之一:SEQ ID NO:1所示的氨基酸序列的 C-末端的195个、149个、99个、70个、46个、30个或24个氨基酸残基连续缺失后的片段。具体 地,所述HSV1-TK片段可以具有选自下组的任何一种氨基酸序列:SEQ ID NO:2-6。 编码所述HSV1-TK片段的核苷酸序列可以是编码以下任何HSV1-TK片段的核苷酸 序列:SEQ ID NO:1所示的氨基酸序列的C-末端的1至195个、24至149个,或30至46个氨基酸 14 CN 111556899 A 说 明 书 11/17 页 残基连续缺失后的片段。具体而言,编码所述HSV1-TK片段的核苷酸序列可以是编码以下任 何一种氨基酸序列的核苷酸序列:SEQ ID NO:2-6。优选地,编码所述HSV1-TK片段的核苷酸 序列可以是SEQ ID NO:9所示的核苷酸序列。 所述HSV-TK片段的变体可以是HSV1-TK片段的变体。具体地,所述HSV1-TK片段的 变体可以是构成所述HSV1-TK片段的至少一个氨基酸残基被取代的变体。特别地,所述 HSV1-TK片段的变体可以包含如SEQ ID NO:1所示的氨基酸序列的第1位至第145位氨基酸 残基。在一个实施方式中,所述HSV1-TK片段的变体可以具有如SEQ ID NO:7或8所示的氨基 酸序列。编码所述HSV1-TK片段的变体的核苷酸序列可以是SEQ ID NO:10或11。 转染可以通过各种方法进行。具体而言,可以适用的转染方法如CaCl2沉淀、 Hanahan法(通过在CaCl2沉淀中使用DMSO(二甲基亚砜)来提高效率)、电穿孔、磷酸钙沉淀、 原生质体融合、与碳化硅纤维搅拌、农杆菌介导的转染、使用PEG、硫酸葡聚糖、脂质转染胺 进行转染,以及干燥/抑制介导的转染。 另外,宿主细胞可以是酵母细胞(例如酿酒酵母和粟酒裂殖酵母等);真菌细胞(例 如毕赤酵母);昆虫细胞(例如果蝇和斜纹夜蛾Sf9细胞);动物细胞(例如CHO细胞、HeLa细 胞、COS细胞、NSO细胞、293细胞和弓黑素瘤细胞);或植物细胞。在一实施方式中,所述宿主 细胞可以是HeLa细胞。 所述野生型牛痘病毒可以是西储(Western Reserve)(WR)、NYVAC(纽约牛痘病 毒)、Wyeth(纽约市卫生局;NYCBOH)、LC16m8、李斯特(Lister)、哥本哈根(Copenhagen)、天 坛(Tian Tan)、USSR、塔什干(TashKent),埃文斯(Evans)、IHD-J(国际卫生科-J)或IHD-W (国际卫生科-白)菌株,但不限于此。 所述穿梭质粒和野生型牛痘病毒可以包含同一牛痘病毒基因的同源区域。所述穿 梭质粒和野生型牛痘病毒可以优选包含不同的复制起点和/或标记,从而可以筛选每个元 件。 可以使用本领域已知的方法培养宿主细胞。具体地,培养方法没有特别限制,只要 其可以产生表达本发明的HSV1-TK片段的重组牛痘病毒即可。具体地,可以以分批补料或重 复的分批补料工艺连续进行培养。 用于培养的培养基可以是包含适当碳源、氮源、氨基酸、维生素等的常规培养基, 其中可以在有氧条件下,通过调节温度、pH等适当方式满足特定菌株的需要。作为碳源,可 以使用葡萄糖和木糖的混合糖作为主要碳源。其他碳源可能包括糖和碳水化合物,例如蔗 糖、乳糖、果糖、麦芽糖、淀粉和纤维素;油脂(例如大豆油、葵花籽油、蓖麻油和椰子油);脂 肪酸(例如棕榈酸、硬脂酸和亚油酸);醇(例如甘油和乙醇);有机酸(例如乙酸)。另外,碳源 可以单独使用或混合使用。在一实施方式中,培养基可以是含有胎牛血清的EMEM培养基。 另外,可以在培养基中使用合适的前体。可以在培养过程中通过合适的方法以分 批、补料分批或连续的方式将原料加入培养物中,但不特别限于此。培养物的pH可以通过使 用碱性化合物或酸性化合物以合适的方式调节,所述碱性化合物如氢氧化钠、氢氧化钾、 氨,所述酸性化合物如磷酸或硫酸。 另外,通过使用消泡剂(例如脂肪酸聚乙二醇酯)可以抑制气泡的形成。为了维持 有氧条件,将氧气或含氧气体(例如空气)注入培养物中。培养物的温度范围通常为27℃至 37℃,最好为30℃至35℃。培养时间可以为2小时至80小时。优选地,培养时间可以为4小时 15 CN 111556899 A 说 明 书 12/17 页 至76小时。 从培养物中获得病毒的方法包括:收获宿主细胞,使细胞经历重复的冷冻/融化循 环以获得细胞裂解物,对细胞裂解物进行重复的冷冻/融化循环以获得粗病毒,对粗病毒重 复进行噬菌斑分离从而获得纯重组牛痘病毒。然而,所述方法不限于此。 本发明的另一方面提供了所述溶瘤病毒在治疗癌症中的用途。 本发明的另一方面提供了所述药物组合物在治疗癌症中的用途。 本发明的另一方面提供了所述溶瘤病毒在制备用于治疗癌症的药物中的用途。 本发明的另一方面提供了所述药物组合物在制备用于治疗癌症的药物中的用途。 发明方式 在下文中,将参考实施例详细描述本发明。然而,以下实施例仅用于说明目的,并 不意图限制本发明的范围。 实施例1.重组牛痘病毒(OTS-412)的制备 实施例1.1.穿梭质粒载体的构建 野生型牛痘病毒(NYC卫生部菌株,VR-1536)购自美国典型培养物保藏中心 (ATCC)。为了重组,将包含HSV1-TK基因(pSE/L启动子)和萤火虫荧光素酶报道基因(p7.5启 动子)的pUC57amp (美国Genewiz)用作穿梭质粒载体(图1)。 实施例1.2.重组牛痘病毒的制备 为了确保重组病毒的安全,在6孔板中以4×105个细胞/孔的浓度,在含有10%胎 牛血清的EMEM培养基中制备HeLa细胞(ATCC)。然后,用0.05MOI的野生型牛痘病毒处理细 胞。2小时后,用含有2%胎牛血清的EMEM培养基替换培养基,然后通过使用XfectTM聚合物 (Clontech 631317,USA),用4μg实施例1.1中构建的线性化的穿梭质粒载体转染细胞。孵育 4小时后,用含有2%胎牛血清的新鲜EMEM培养基更换培养基,然后将细胞进一步孵育72小 时。证实HeLa细胞中的荧光素酶活性,从而获得了含有HSV1-TK基因的重组牛痘病毒。 此后,在用于筛选缺乏TK功能的细胞的生化条件(TK选择压力)下,在BrdU(胸苷类 似物,15μg/ml)存在下,从TK-骨肉瘤细胞系(骨肉瘤143TK-)中的十次连续继代培养物中获 得HSV1-TK突变体。突变牛痘病毒的氨基酸测序委托Macrogen公司进行。结果证实,在突变 牛痘病毒中,编码HSV1-TK的C末端的第46个氨基酸谷氨酰胺(Gln)的密码子(caa)被突变为 终止密码子。另外,证实了在突变的牛痘病毒中HSV1-TK的C末端的第46位之后的氨基酸残 基被缺失。最后,获得了表达遗传稳定的HSV1-TK片段的突变牛痘病毒OTS-412(图2和3)。 此外,分析了一些突变体的HSV1-TK基因,以确认其从HSV1-TK的C端缺失了24个、 30个、70个、99个、149个或195个氨基酸。此外,对其他突变体的HSV1-TK基因的分析显示, HSV1-TK片段的变体由181或227个氨基酸组成,包括HSV1-TK的N末端第1至145位氨基酸残 基。 实施例2.OTS-412中HSV1-TK片段表达的鉴定 为了确认实施例1.2中制备的OTS-412表达HSV1-TK片段,将OTS-412感染HeLa细 胞,并在24小时后收集所得细胞并裂解以提取蛋白质。使提取的蛋白质变性,然后上样至 SDS-PAGE凝胶(每个样品40μg)。电泳后,蛋白条带被转移到PVDF膜上,并与一抗(HSV1-TK抗 体)反应。用PBST洗涤后,使蛋白条带与第二抗体(HRP标记的抗山羊抗体)反应。用PBST洗涤 后,用化学发光试剂处理蛋白质条带,并用化学发光图像系统(Davinch K)检测。结果,证实 16 CN 111556899 A 说 明 书 13/17 页 了HSV1-TK片段蛋白在病毒中表达(图4)。 实施例3.证实OTS-412中HSV1-TKmut基因的表达 为了证实在OTS-412中引入了HSV1-TKmut基因表达,通过限制性内切酶图谱鉴定了 野生型牛痘病毒和OTS-412。将野生型牛痘病毒和OTS-412分别感染人骨肉瘤细胞后,分离 病毒并提取病毒基因组DNA,以获得阴性对照(野生型VV)和阳性对照(OTS-412)。 用Hind III限制酶(10单位/2.5μg)消化获得的病毒DNA,并使用DNA电泳仪按大小 进行分离(图5)。结果,当比较阴性对照组和阳性对照组时,鉴定出4kb和8kb之间的四个相 应的带(箭头)和一个错配的带(虚线箭头)。该错配带具有较大的基因大小,这表明HSV1- TKmut基因和萤火虫荧光素酶基因已插入牛痘病毒的TK区域。证实其为OTS-412的独特条带 模式,其不同于野生型牛痘病毒。将野生型牛痘病毒和OTS-412经过几次传代后与对照组进 行比较,观察到与各个对照组相同的条带模式,从而确认OTS-412中的HSV1-TKmut基因具有 遗传稳定性。 实施例4.证实通过GCV给药(体外)使得OTS-412复制性降低 实施例1.2中制备的OTS-412感染癌细胞的能力和增殖的能力确认如下。用1MOI (1pfu/细胞)的OTS-412处理HCT-116癌细胞系,分别在24小时和48小时后,通过噬菌斑测定 法测量病毒滴度。 结果,在24小时后,证实癌细胞系被OTS-412感染。48小时后,证实与感染后24小时 相比,病毒复制增加了约2.5倍(图6)。 为了确认GCV在OTS-412复制中的作用,基于E9L进行了定量PCR分析(qPCR),E9L仅 在牛痘病毒中特异性表达。 具体地,制备了在仅结合两条互补DNA链之一时识别E9L基因的探针。当病毒复制 一次时,所制备的探针使得一种发光被测量出。将NCI-H460和NCI-H23癌细胞分别用1或 0.1MOI(1或0.1pfu/细胞)的OTS-412单独处理或将其与GCV联合处理2小时,并将得到的感 染细胞培养48小时。然后,使用病毒DNA提取试剂盒提取病毒DNA并稀释至1ng/5μl的浓度, 然后使用其进行qPCR。 结果,证实了在NCI-H460和NCI-H23癌细胞系中,与仅施用OTS-412的情况相比,当 OTS-412与GCV联合施用时,OTS-412的复制能力降低了约45%(图7)。该结果证明OTS-412中 的HSV1-TK片段对GCV敏感。 实施例5.OTS-412的细胞毒性(体外) 尽管GCV抑制OTS-412病毒复制,为了确定OTS-412的细胞毒性是否得以维持,比较 了以下各组的细胞毒性:用表达野生型HSV1-TK的牛痘病毒单独处理或与GCV联合处理的 组,以及用OTS-412单独处理或与GCV联合处理的组。具体而言,用0.05MOI(0.05pfu/细胞) 的表达野生型HSV1-TK的牛痘病毒或OTS-412单独处理,或将其与GCV(50μg)联合处理HCT- 116癌细胞。将所得细胞培养72小时,并使用CCK8(细胞计数试剂盒8)分析细胞毒性。 结果,用OTS-412和GCV联合处理的细胞毒性维持在用OTS-412单独处理组的95% 或更高,而表达野生型HSV1-TK的牛痘病毒几乎没有细胞毒性(图8)。这证明表达野生型 HSV1-TK的牛痘病毒对GCV的敏感性高于插入了HSV1-TKmut的OTS-412,并且由于完全被抑制 了病毒复制而几乎未观察到癌细胞的杀伤作用。 实施例6.证实将OTS-412与GCV联合施用时的抗癌作用(体外) 17 CN 111556899 A 说 明 书 14/17 页 为了证实OTS-412和GCV联合施用的抗癌作用,对施用OTS-412和GCV对两种人肺癌 细胞系(A549和NCI-H460癌细胞系)和两种人结肠直肠癌细胞系(HT-29和HCT-116癌细胞 系)的细胞毒性进行了评估。 具体而言,用OTS-412以0.01、0.1或1MOI感染A549、NCI-H460、HT-29和HCT-116癌 细胞系。用100μM GCV处理三种感染的癌细胞系(A549、NCI-H460和HT-29),并且用50μM GCV 处理感染的HCT-116癌细胞系。将细胞培养72小时,并使用CCK8(细胞计数试剂盒8)分析细 胞毒性。 结果,在NCI-H460和HCT-116癌细胞系中,用OTS-412和GCV的联合处理的癌细胞的 存活率显著低于单独用OTS-412处理的癌细胞。另一方面,在A549和HT-29癌细胞系中,用 OTS-412和GCV联合处理的癌细胞与单独用OTS-412处理的癌细胞之间没有观察到显著差 异。该结果证明GCV具有额外的细胞毒性作用,OTS-412具有直接的癌细胞死亡作用(图9)。 另外,通过流式细胞术(FACS)证实了用OTS-412和GCV的联合施用引起的凋亡和坏 死。具体地,分别用单独的GCV、单独的OTS-412,或OTS-412和GCV联合处理A549和NCI-H460 细胞系,并对细胞进行膜联蛋白V/PI染色,然后进行流式细胞术。目前,根据以下事实确定 细胞的活力:膜联蛋白V和PI在活细胞中均为阴性;膜联蛋白V在细胞凋亡的早期是阳性的, 其中细胞膜的通透性改变;膜联蛋白V和PI在凋亡末期均为阳性,其中细胞核由于细胞膜被 破坏而暴露。 结果,仅通过GCV处理的细胞未被证实凋亡。然而,当单独用OTS-412处理A549细胞 时,观察到凋亡率是19.64%,而用OTS-412和GCV联合处理时,凋亡率是35.06%。另外,当单 独用OTS-412处理NCI-H460细胞时,观察到凋亡率是6.58%,而用OTS-412和GCV联合处理 时,凋亡率是12.78%(图10)。此外,对FACS结果进行了量化和相互比较。结果,证实了与单 独用OTS-412处理的组相比,GCV具有另外的毒性作用(图11)。 实施例7.证实联合施用OTS-412和GCV后的抗癌作用(体内) 实施例7.1.使用植入HCT-116癌细胞系的小鼠模型证实OTC-412和GCV联合给药的 抗癌作用(瘤内给药) 将获自Orient Bio(Busan)的Balb/c小鼠(雌性,8周)适应一个星期,并用5×106 个细胞的HCT-116人结肠癌细胞系(韩国细胞系银行)进行异种移植。当肿瘤大小达到 100mm3至150mm3时,将OTS-412单独或与GCV联合瘤内给药。 将由此制备的植入人结肠癌细胞的小鼠分为三组。将瘤内接受生理盐水的组作为 阴性对照,并且将以瘤内方式接受溶瘤病毒(OTS-412,1×106pfu)的组作为阳性对照。另 外,瘤内接受溶瘤病毒(OTS-412,1×106pfu)和GCV(25mg/kg)的组合的组被设置为实验组。 每种药物在第1天给药一次。 给药后第12天,测量每组小鼠的肿瘤大小。阴性对照小鼠的肿瘤大小为600mm3,而 阳性对照小鼠的肿瘤大小为200mm3,比阴性对照小鼠小约66%。另一方面,测得的实验组小 鼠的肿瘤尺寸为150mm3,比阴性对照小鼠的肿瘤尺寸小约75%(图12)。这证实了用OTS-412 和GCV联合处理人结肠癌细胞系可提高抗癌效果。 为了确认病毒分布,在第7天对每组进行了生物发光图像分析。将小鼠固定在 OPTIX MX3设备上,并在麻醉情况下向其注射D-荧光素以获得生物发光图像。比较单独施用 OTS-412或将其与GCV联合施用的组的荧光强度,可以确认与GCV组合后病毒复制受到抑制 18 CN 111556899 A 说 明 书 15/17 页 (图13)。 为了确认对病毒复制的抑制作用,从第12天处死的小鼠中分离出肿瘤组织,并从 中提取基因组DNA。进行了基于E9L的定量PCR分析(qPCR) ,其中E9L仅在牛痘病毒中特异性 表达。 结果,当联合施用OTS-412和GCV时,发现OTS-412病毒的DNA拷贝数比单独施用 OTS-412的组低约50%,并且还观察到统计学上的显著差异。因此,证实了病毒复制被GCV抑 制(图14)。 另外,为了确认单独使用OTS-412以及OTS-412和GCV的联合施用的安全性,向对照 组和实验组分别给药,然后在给药当天、第3天、第6天、第9天,和第12天对小鼠称重。通过从 测得的体重中减去肿瘤重量来计算小鼠的体重。 结果,所有三个组中的小鼠均表现出体重增加,并且各组之间几乎没有差异(图 15)。因此,确认了OTS-412与GCV联合施用的安全性。 上述HCT-116移植小鼠实验表明,OTS-412和GCV的联合施用可有效控制病毒复制, 同时保持抗癌作用。 实施例7.2.使用植入Renca癌细胞系的小鼠模型证实OTS-412和GCV联合给药的抗 癌作用 将获自Orient Bio(Busan)的Balb/c小鼠(雌性,7周)适应一个星期,并用5×107 个细胞的Renca癌细胞系(韩国细胞系银行)进行同种异体移植。当肿瘤大小达到300mm3至 500mm3时,开始施用溶瘤病毒。尽管小鼠癌细胞中的病毒复制受到限制,但该实验的进行显 示了OTS-412和GCV的组合在同种异体移植小鼠模型中的抗肿瘤作用。 将由此制备的植入小鼠肾细胞癌细胞系的小鼠分为三组。将瘤内接受生理盐水的 组设为阴性对照,将接受每周一次溶瘤病毒(OTS-412,1x107pfu)给药的组设为阳性对照。 另外,将每周两次接受溶瘤病毒(OTS-412,5x106pfu)与GCV(25mg/kg)联合给药的组作为实 验组。将溶瘤病毒瘤内施用于小鼠肾细胞癌细胞系移植小鼠,并腹膜内施用GCV。此时,在不 施用溶瘤病毒的当天,分别将PBS和GCV施用于阴性对照组和实验组。 在第24天,测量每组小鼠的肿瘤大小。阴性对照小鼠的肿瘤大小为1350mm3,而阳 性对照小鼠的肿瘤大小为1200mm3,比阴性对照小鼠小约10%。另一方面,测得的实验组小 鼠的肿瘤尺寸为700mm3,比阴性对照小鼠的肿瘤尺寸小约45%。因此,证实了与单独施用病 毒相比,即使在对溶瘤病毒具有抗性的癌细胞系中,OTS-412和GCV的联合施用也显著提高 了抗癌作用(图16)。 从在施用OTS-412后第23天处死的小鼠中分离肿瘤组织,并从中提取基因组DNA。 进行了基于E9L的定量PCR分析,其中E9L仅在牛痘病毒中特异性表达。 结果,当联合施用OTS-412和GCV时,发现OTS-412病毒颗粒数比单独施用OTS-412 的组低约50%,这在统计学上是显著的。因此,证实了GCV有效地控制了病毒复制(图17)。 在施用OTS-412后的第24天,处死小鼠,并从中分离出肿瘤组织进行TUNEL测定。用 多聚甲醛固定组织,然后切成薄片。之后,将切片的组织用蛋白酶K进行抗原回收15分钟,然 后通过使用凋亡检测试剂盒用dUTP标记的FITC进行处理以观察肿瘤组织的凋亡。 结果,证实了OTS-412和GCV联合施用组的细胞凋亡增加(图18)。此处,死细胞以红 色荧光(TRITC)表示,细胞核被蓝色荧光(DAPI)染色。为了对在TUNEL测定中获得的图像进 19 CN 111556899 A 说 明 书 16/17 页 行统计处理,对细胞凋亡区域进行了定量。结果证实,用OTS-412与GCV联合施用的组显示出 的凋亡率是单独OTS-412处理的组的凋亡率的两倍(图19)。 实施例7.3.使用植入HCT-116癌细胞系的小鼠模型证实OTC-412和GCV联合给药的 抗癌作用(腹膜内给药) 将获自Orient Bio(Busan)的Balb/c小鼠(雌性,8周)适应一个星期,并用2.5× 106个细胞的HCT-116人结肠癌细胞系(韩国细胞系银行)进行异种移植。观察直至肿瘤大小 达到100mm3至150mm3后,腹膜内单独施用OTS-412或将其与GCV联合施用。 将由此制备的植入人结肠癌细胞的小鼠分为三组。将瘤内接受生理盐水的组作为 阴性对照,并且将瘤内接受溶瘤病毒(OTS-412,1×108pfu)的组作为阳性对照。另外,接受 溶瘤病毒(OTS-412,1×108pfu)和GCV(50mg/kg)的组合的组被设置为实验组。此时,将所有 药物腹膜内施用于HCT-116移植小鼠,并且腹膜内施用GCV。每周两次施用溶瘤病毒,并且在 不施用溶瘤病毒的当天,分别将PBS和GCV施用于阴性对照组和实验组。 在第21天处死小鼠并测量肿瘤大小,在阴性对照组中肿瘤大小增加了约8倍,但是 联合施用OTS-412与GCV的组比阴性对照组小40%(图20)。 另外,还进行了免疫组织化学(IHC)实验以确定肿瘤组织中病毒感染的程度。分离 肿瘤组织、加工成石蜡块,然后切片。使用二甲苯和乙醇从组织切片中去除石蜡。使用去克 隆室(decloacking chamber)对组织进行抗原回收,使其依次与第一抗体(牛痘病毒抗体, ab35219)和偶联FITC的第二抗体反应,然后在荧光显微镜下观察。 结果,在经PBS处理的阴性对照组的肿瘤组织中未观察到溶瘤病毒,而在施用OTS- 412的组中观察到了溶瘤病毒。在联合施用OTS-412和GCV的组中也检测到了溶瘤病毒,但比 单独施用OTS-412的组中的溶瘤病毒要少(图21和22)。 另外,分离小鼠肿瘤组织并进行H&E染色。具体而言,在第21天处死小鼠,并分离肿 瘤组织、加工成石蜡块,然后切片。从组织切片中除去石蜡,然后将组织切片依次浸入苏木 精和曙红中、干燥、固定,然后使用载玻片扫描仪观察。通过H&E染色来测量肿瘤坏死的百分 比,并且通过从整个肿瘤的大小中减去坏死部分来测量存活的肿瘤大小。结果,证实了与对 照组相比,实验组的肿瘤坏死程度明显高于阴性对照组(图23)。 另外,对每组的所有小鼠的肿瘤组织进行H&E染色,并且测量除坏死部分以外的肿 瘤区域的大小。结果,证实了OTS-412和GCV联合给药的实验组小鼠的肿瘤组织面积与对照 小鼠相比,小约40%(图24)。 在第3天、第7天、第10天、第14天、第17天和第21天对小鼠称重,以评估药物的毒 性。在接受病毒处理的两组中,尽管在注射病毒后第3天体重均有所减轻,但在第7天体重均 已恢复到约95%。此后,OTS-412和GCV联合施用的组的体重一直维持到第21天,从而证实了 给药的安全性(图25)。 实施例8.OTS-412在各种癌细胞系中的细胞毒性(体外) 为了确认OTS-412在各种癌细胞系中的抗癌作用,在HeLa、PC-3、DU-145、HT-29、 HCT-116、A549、NCI-H23、NCI-H460、MCF-7、MDA-MB-231、4T1、Renca和B16F10癌细胞系中评 估了OTS-412的毒性。HeLa、A549、4T1和B16F10癌细胞系获自ATCC(美国),其余九种癌细胞 系获自韩国细胞系银行(KCLB)。 具体地,分别用0.5MOI(1pfu/细胞)的OTS-412感染癌细胞系,并将细胞培养48小 20 CN 111556899 A 说 明 书 17/17 页 时和72小时。之后,通过使用CCK8(细胞计数试剂盒8)分析细胞毒性。 对包括宫颈癌细胞系(HeLa)、肺癌细胞系(A549、NCI-H23和HCI-H460)、前列腺癌 细胞系(PC-3和DU145)、直肠癌细胞系(HT-29和HCT-116)、乳腺癌细胞系(MCF-7、MDA-MB- 231和4T1)、黑素瘤细胞系(B16F10)和大鼠肾细胞癌细胞系(Renca)的13种癌细胞系进行分 析,结果揭示了4T1、Renca和B16F10细胞系显示出80%或更高的存活率,同时显示出较高的 抗性。然而,其余的癌细胞系在72小时后显示出约40%或更少的存活率,表明OTS-412显示 出对这些细胞的高细胞毒性(图26)。 此外,为了测量体外细胞毒性,测量了IC50,该浓度是癌细胞活力被抑制50%的浓 度。此时,分别向HCT-116、SK-MEL-29和DU145细胞施用0.1、0.3、0.6和1.0MOI(pfu/细胞)的 OTS-412。根据制造商的说明,使用CCK-8(细胞计数试剂盒8)测量细胞毒性。结果显示,HCT- 116、SK-MEL-29和DU145细胞中OTS-412的IC50值分别为0.24pfu、0.37pfu和0.08pfu(图27)。 实施例9.证实腹膜内注射OTS-412后的病毒分布(体内) 将高剂量的OTS-412病毒(1x107pfu/小鼠)腹膜内施用于HCT-116癌细胞移植的小 鼠,并证实全身注射的病毒是否靶向并递送至肿瘤。 生物发光图像分析的结果证实,该病毒靶向肿瘤。结果还证实了,在第7天,该病毒 比第3天复制更多,并且信号更强(图28)。 21 CN 111556899 A 序 列 表 1/11 页 序列表 <110> 拜耳诺克斯有限公司 <120> 安全性和抗癌作用得到改善的溶瘤病毒 <130> PCB712075BNX <150> US 62/611,174 <151> 2017-12-28 <150> KR 10-2018-0106841 <151> 2018-09-07 <160> 11 <170> SIPOSequenceListing 1.0 <210> 1 <211> 376 <212> PRT <213> 人工序列(Artificial Sequence) <400> 1 Met Ala Ser Tyr Pro Cys His Gln His Ala Ser Ala Phe Asp Gln Ala 1 5 10 15 Ala Arg Ser Arg Gly His Ser Asn Arg Arg Thr Ala Leu Arg Pro Arg 20 25 30 Arg Gln Gln Glu Ala Thr Glu Val Arg Leu Glu Gln Lys Met Pro Thr 35 40 45 Leu Leu Arg Val Tyr Ile Asp Gly Pro His Gly Met Gly Lys Thr Thr 50 55 60 Thr Thr Gln Leu Leu Val Ala Leu Gly Ser Arg Asp Asp Ile Val Tyr 65 70 75 80 Val Pro Glu Pro Met Thr Tyr Trp Gln Val Leu Gly Ala Ser Glu Thr 85 90 95 Ile Ala Asn Ile Tyr Thr Thr Gln His Arg Leu Asp Gln Gly Glu Ile 100 105 110 Ser Ala Gly Asp Ala Ala Val Val Met Thr Ser Ala Gln Ile Thr Met 115 120 125 Gly Met Pro Tyr Ala Val Thr Asp Ala Val Leu Ala Pro His Val Gly 130 135 140 Gly Glu Ala Gly Ser Ser His Ala Pro Pro Pro Ala Leu Thr Leu Ile 145 150 155 160 Phe Asp Arg His Pro Ile Ala Ala Leu Leu Cys Tyr Pro Ala Ala Arg 165 170 175 Tyr Leu Met Gly Ser Met Thr Pro Gln Ala Val Leu Ala Phe Val Ala 22 CN 111556899 A 序 列 表 2/11 页 180 185 190 Leu Ile Pro Pro Thr Leu Pro Gly Thr Asn Ile Val Leu Gly Ala Leu 195 200 205 Pro Glu Asp Arg His Ile Asp Arg Leu Ala Lys Arg Gln Arg Pro Gly 210 215 220 Glu Arg Leu Asp Leu Ala Met Leu Ala Ala Ile Arg Arg Val Tyr Gly 225 230 235 240 Leu Leu Ala Asn Thr Val Arg Tyr Leu Gln Gly Gly Gly Ser Trp Trp 245 250 255 Glu Asp Trp Gly Gln Leu Ser Gly Thr Ala Val Pro Pro Gln Gly Ala 260 265 270 Glu Pro Gln Ser Asn Ala Gly Pro Arg Pro His Ile Gly Asp Thr Leu 275 280 285 Phe Thr Leu Phe Arg Ala Pro Glu Leu Leu Ala Pro Asn Gly Asp Leu 290 295 300 Tyr Asn Val Phe Ala Trp Ala Leu Asp Val Leu Ala Lys Arg Leu Arg 305 310 315 320 Pro Met His Val Phe Ile Leu Asp Tyr Asp Gln Ser Pro Ala Gly Cys 325 330 335 Arg Asp Ala Leu Leu Gln Leu Thr Ser Gly Met Val Gln Thr His Val 340 345 350 Thr Thr Pro Gly Ser Ile Pro Thr Ile Cys Asp Leu Ala Arg Thr Phe 355 360 365 Ala Arg Glu Met Gly Glu Ala Asn 370 375 <210> 2 <211> 330 <212> PRT <213> 人工序列(Artificial Sequence) <400> 2 Met Ala Ser Tyr Pro Cys His Gln His Ala Ser Ala Phe Asp Gln Ala 1 5 10 15 Ala Arg Ser Arg Gly His Ser Asn Arg Arg Thr Ala Leu Arg Pro Arg 20 25 30 Arg Gln Gln Glu Ala Thr Glu Val Arg Leu Glu Gln Lys Met Pro Thr 35 40 45 Leu Leu Arg Val Tyr Ile Asp Gly Pro His Gly Met Gly Lys Thr Thr 50 55 60 Thr Thr Gln Leu Leu Val Ala Leu Gly Ser Arg Asp Asp Ile Val Tyr 23 CN 111556899 A 序 列 表 3/11 页 65 70 75 80 Val Pro Glu Pro Met Thr Tyr Trp Gln Val Leu Gly Ala Ser Glu Thr 85 90 95 Ile Ala Asn Ile Tyr Thr Thr Gln His Arg Leu Asp Gln Gly Glu Ile 100 105 110 Ser Ala Gly Asp Ala Ala Val Val Met Thr Ser Ala Gln Ile Thr Met 115 120 125 Gly Met Pro Tyr Ala Val Thr Asp Ala Val Leu Ala Pro His Val Gly 130 135 140 Gly Glu Ala Gly Ser Ser His Ala Pro Pro Pro Ala Leu Thr Leu Ile 145 150 155 160 Phe Asp Arg His Pro Ile Ala Ala Leu Leu Cys Tyr Pro Ala Ala Arg 165 170 175 Tyr Leu Met Gly Ser Met Thr Pro Gln Ala Val Leu Ala Phe Val Ala 180 185 190 Leu Ile Pro Pro Thr Leu Pro Gly Thr Asn Ile Val Leu Gly Ala Leu 195 200 205 Pro Glu Asp Arg His Ile Asp Arg Leu Ala Lys Arg Gln Arg Pro Gly 210 215 220 Glu Arg Leu Asp Leu Ala Met Leu Ala Ala Ile Arg Arg Val Tyr Gly 225 230 235 240 Leu Leu Ala Asn Thr Val Arg Tyr Leu Gln Gly Gly Gly Ser Trp Trp 245 250 255 Glu Asp Trp Gly Gln Leu Ser Gly Thr Ala Val Pro Pro Gln Gly Ala 260 265 270 Glu Pro Gln Ser Asn Ala Gly Pro Arg Pro His Ile Gly Asp Thr Leu 275 280 285 Phe Thr Leu Phe Arg Ala Pro Glu Leu Leu Ala Pro Asn Gly Asp Leu 290 295 300 Tyr Asn Val Phe Ala Trp Ala Leu Asp Val Leu Ala Lys Arg Leu Arg 305 310 315 320 Pro Met His Val Phe Ile Leu Asp Tyr Asp 325 330 <210> 3 <211> 277 <212> PRT <213> 人工序列(Artificial Sequence) <400> 3 Met Ala Ser Tyr Pro Cys His Gln His Ala Ser Ala Phe Asp Gln Ala 24 CN 111556899 A 序 列 表 4/11 页 1 5 10 15 Ala Arg Ser Arg Gly His Ser Asn Arg Arg Thr Ala Leu Arg Pro Arg 20 25 30 Arg Gln Gln Glu Ala Thr Glu Val Arg Leu Glu Gln Lys Met Pro Thr 35 40 45 Leu Leu Arg Val Tyr Ile Asp Gly Pro His Gly Met Gly Lys Thr Thr 50 55 60 Thr Thr Gln Leu Leu Val Ala Leu Gly Ser Arg Asp Asp Ile Val Tyr 65 70 75 80 Val Pro Glu Pro Met Thr Tyr Trp Gln Val Leu Gly Ala Ser Glu Thr 85 90 95 Ile Ala Asn Ile Tyr Thr Thr Gln His Arg Leu Asp Gln Gly Glu Ile 100 105 110 Ser Ala Gly Asp Ala Ala Val Val Met Thr Ser Ala Gln Ile Thr Met 115 120 125 Gly Met Pro Tyr Ala Val Thr Asp Ala Val Leu Ala Pro His Val Gly 130 135 140 Gly Glu Ala Gly Ser Ser His Ala Pro Pro Pro Ala Leu Thr Leu Ile 145 150 155 160 Phe Asp Arg His Pro Ile Ala Ala Leu Leu Cys Tyr Pro Ala Ala Arg 165 170 175 Tyr Leu Met Gly Ser Met Thr Pro Gln Ala Val Leu Ala Phe Val Ala 180 185 190 Leu Ile Pro Pro Thr Leu Pro Gly Thr Asn Ile Val Leu Gly Ala Leu 195 200 205 Pro Glu Asp Arg His Ile Asp Arg Leu Ala Lys Arg Gln Arg Pro Gly 210 215 220 Glu Arg Leu Asp Leu Ala Met Leu Ala Ala Ile Arg Arg Val Tyr Gly 225 230 235 240 Leu Leu Ala Asn Thr Val Arg Tyr Leu Gln Gly Gly Gly Ser Trp Trp 245 250 255 Glu Asp Trp Gly Gln Leu Ser Gly Thr Ala Val Pro Pro Gln Gly Ala 260 265 270 Glu Pro Gln Ser Asn 275 <210> 4 <211> 306 <212> PRT <213> 人工序列(Artificial Sequence) 25 CN 111556899 A 序 列 表 5/11 页 <400> 4 Met Ala Ser Tyr Pro Cys His Gln His Ala Ser Ala Phe Asp Gln Ala 1 5 10 15 Ala Arg Ser Arg Gly His Ser Asn Arg Arg Thr Ala Leu Arg Pro Arg 20 25 30 Arg Gln Gln Glu Ala Thr Glu Val Arg Leu Glu Gln Lys Met Pro Thr 35 40 45 Leu Leu Arg Val Tyr Ile Asp Gly Pro His Gly Met Gly Lys Thr Thr 50 55 60 Thr Thr Gln Leu Leu Val Ala Leu Gly Ser Arg Asp Asp Ile Val Tyr 65 70 75 80 Val Pro Glu Pro Met Thr Tyr Trp Gln Val Leu Gly Ala Ser Glu Thr 85 90 95 Ile Ala Asn Ile Tyr Thr Thr Gln His Arg Leu Asp Gln Gly Glu Ile 100 105 110 Ser Ala Gly Asp Ala Ala Val Val Met Thr Ser Ala Gln Ile Thr Met 115 120 125 Gly Met Pro Tyr Ala Val Thr Asp Ala Val Leu Ala Pro His Val Gly 130 135 140 Gly Glu Ala Gly Ser Ser His Ala Pro Pro Pro Ala Leu Thr Leu Ile 145 150 155 160 Phe Asp Arg His Pro Ile Ala Ala Leu Leu Cys Tyr Pro Ala Ala Arg 165 170 175 Tyr Leu Met Gly Ser Met Thr Pro Gln Ala Val Leu Ala Phe Val Ala 180 185 190 Leu Ile Pro Pro Thr Leu Pro Gly Thr Asn Ile Val Leu Gly Ala Leu 195 200 205 Pro Glu Asp Arg His Ile Asp Arg Leu Ala Lys Arg Gln Arg Pro Gly 210 215 220 Glu Arg Leu Asp Leu Ala Met Leu Ala Ala Ile Arg Arg Val Tyr Gly 225 230 235 240 Leu Leu Ala Asn Thr Val Arg Tyr Leu Gln Gly Gly Gly Ser Trp Trp 245 250 255 Glu Asp Trp Gly Gln Leu Ser Gly Thr Ala Val Pro Pro Gln Gly Ala 260 265 270 Glu Pro Gln Ser Asn Ala Gly Pro Arg Pro His Ile Gly Asp Thr Leu 275 280 285 Phe Thr Leu Phe Arg Ala Pro Glu Leu Leu Ala Pro Asn Gly Asp Leu 290 295 300 26 CN 111556899 A 序 列 表 6/11 页 Tyr Asn 305 <210> 5 <211> 346 <212> PRT <213> 人工序列(Artificial Sequence) <400> 5 Met Ala Ser Tyr Pro Cys His Gln His Ala Ser Ala Phe Asp Gln Ala 1 5 10 15 Ala Arg Ser Arg Gly His Ser Asn Arg Arg Thr Ala Leu Arg Pro Arg 20 25 30 Arg Gln Gln Glu Ala Thr Glu Val Arg Leu Glu Gln Lys Met Pro Thr 35 40 45 Leu Leu Arg Val Tyr Ile Asp Gly Pro His Gly Met Gly Lys Thr Thr 50 55 60 Thr Thr Gln Leu Leu Val Ala Leu Gly Ser Arg Asp Asp Ile Val Tyr 65 70 75 80 Val Pro Glu Pro Met Thr Tyr Trp Gln Val Leu Gly Ala Ser Glu Thr 85 90 95 Ile Ala Asn Ile Tyr Thr Thr Gln His Arg Leu Asp Gln Gly Glu Ile 100 105 110 Ser Ala Gly Asp Ala Ala Val Val Met Thr Ser Ala Gln Ile Thr Met 115 120 125 Gly Met Pro Tyr Ala Val Thr Asp Ala Val Leu Ala Pro His Val Gly 130 135 140 Gly Glu Ala Gly Ser Ser His Ala Pro Pro Pro Ala Leu Thr Leu Ile 145 150 155 160 Phe Asp Arg His Pro Ile Ala Ala Leu Leu Cys Tyr Pro Ala Ala Arg 165 170 175 Tyr Leu Met Gly Ser Met Thr Pro Gln Ala Val Leu Ala Phe Val Ala 180 185 190 Leu Ile Pro Pro Thr Leu Pro Gly Thr Asn Ile Val Leu Gly Ala Leu 195 200 205 Pro Glu Asp Arg His Ile Asp Arg Leu Ala Lys Arg Gln Arg Pro Gly 210 215 220 Glu Arg Leu Asp Leu Ala Met Leu Ala Ala Ile Arg Arg Val Tyr Gly 225 230 235 240 Leu Leu Ala Asn Thr Val Arg Tyr Leu Gln Gly Gly Gly Ser Trp Trp 245 250 255 27 CN 111556899 A 序 列 表 7/11 页 Glu Asp Trp Gly Gln Leu Ser Gly Thr Ala Val Pro Pro Gln Gly Ala 260 265 270 Glu Pro Gln Ser Asn Ala Gly Pro Arg Pro His Ile Gly Asp Thr Leu 275 280 285 Phe Thr Leu Phe Arg Ala Pro Glu Leu Leu Ala Pro Asn Gly Asp Leu 290 295 300 Tyr Asn Val Phe Ala Trp Ala Leu Asp Val Leu Ala Lys Arg Leu Arg 305 310 315 320 Pro Met His Val Phe Ile Leu Asp Tyr Asp Gln Ser Pro Ala Gly Cys 325 330 335 Arg Asp Ala Leu Leu Gln Leu Thr Ser Gly 340 345 <210> 6 <211> 352 <212> PRT <213> 人工序列(Artificial Sequence) <400> 6 Met Ala Ser Tyr Pro Cys His Gln His Ala Ser Ala Phe Asp Gln Ala 1 5 10 15 Ala Arg Ser Arg Gly His Ser Asn Arg Arg Thr Ala Leu Arg Pro Arg 20 25 30 Arg Gln Gln Glu Ala Thr Glu Val Arg Leu Glu Gln Lys Met Pro Thr 35 40 45 Leu Leu Arg Val Tyr Ile Asp Gly Pro His Gly Met Gly Lys Thr Thr 50 55 60 Thr Thr Gln Leu Leu Val Ala Leu Gly Ser Arg Asp Asp Ile Val Tyr 65 70 75 80 Val Pro Glu Pro Met Thr Tyr Trp Gln Val Leu Gly Ala Ser Glu Thr 85 90 95 Ile Ala Asn Ile Tyr Thr Thr Gln His Arg Leu Asp Gln Gly Glu Ile 100 105 110 Ser Ala Gly Asp Ala Ala Val Val Met Thr Ser Ala Gln Ile Thr Met 115 120 125 Gly Met Pro Tyr Ala Val Thr Asp Ala Val Leu Ala Pro His Val Gly 130 135 140 Gly Glu Ala Gly Ser Ser His Ala Pro Pro Pro Ala Leu Thr Leu Ile 145 150 155 160 Phe Asp Arg His Pro Ile Ala Ala Leu Leu Cys Tyr Pro Ala Ala Arg 165 170 175 28 CN 111556899 A 序 列 表 8/11 页 Tyr Leu Met Gly Ser Met Thr Pro Gln Ala Val Leu Ala Phe Val Ala 180 185 190 Leu Ile Pro Pro Thr Leu Pro Gly Thr Asn Ile Val Leu Gly Ala Leu 195 200 205 Pro Glu Asp Arg His Ile Asp Arg Leu Ala Lys Arg Gln Arg Pro Gly 210 215 220 Glu Arg Leu Asp Leu Ala Met Leu Ala Ala Ile Arg Arg Val Tyr Gly 225 230 235 240 Leu Leu Ala Asn Thr Val Arg Tyr Leu Gln Gly Gly Gly Ser Trp Trp 245 250 255 Glu Asp Trp Gly Gln Leu Ser Gly Thr Ala Val Pro Pro Gln Gly Ala 260 265 270 Glu Pro Gln Ser Asn Ala Gly Pro Arg Pro His Ile Gly Asp Thr Leu 275 280 285 Phe Thr Leu Phe Arg Ala Pro Glu Leu Leu Ala Pro Asn Gly Asp Leu 290 295 300 Tyr Asn Val Phe Ala Trp Ala Leu Asp Val Leu Ala Lys Arg Leu Arg 305 310 315 320 Pro Met His Val Phe Ile Leu Asp Tyr Asp Gln Ser Pro Ala Gly Cys 325 330 335 Arg Asp Ala Leu Leu Gln Leu Thr Ser Gly Met Val Gln Thr His Val 340 345 350 <210> 7 <211> 227 <212> PRT <213> 人工序列(Artificial Sequence) <400> 7 Met Ala Ser Tyr Pro Cys His Gln His Ala Ser Ala Phe Asp Gln Ala 1 5 10 15 Ala Arg Ser Arg Gly His Ser Asn Arg Arg Thr Ala Leu Arg Pro Arg 20 25 30 Arg Gln Gln Glu Ala Thr Glu Val Arg Leu Glu Gln Lys Met Pro Thr 35 40 45 Leu Leu Arg Val Tyr Ile Asp Gly Pro His Gly Met Gly Lys Thr Thr 50 55 60 Thr Thr Gln Leu Leu Val Ala Leu Gly Ser Arg Asp Asp Ile Val Tyr 65 70 75 80 Val Pro Glu Pro Met Thr Tyr Trp Gln Val Leu Gly Ala Ser Glu Thr 85 90 95 29 CN 111556899 A 序 列 表 9/11 页 Ile Ala Asn Ile Tyr Thr Thr Gln His Arg Leu Asp Gln Gly Glu Ile 100 105 110 Ser Ala Gly Asp Ala Ala Val Val Met Thr Ser Ala Gln Ile Thr Met 115 120 125 Gly Met Pro Tyr Ala Val Thr Asp Ala Val Leu Ala Pro His Val Gly 130 135 140 Gly Gly Gly Trp Glu Phe Thr Cys Pro Ala Pro Gly Pro His Pro His 145 150 155 160 Leu Arg Pro Pro Ser His Arg Arg Pro Pro Val Leu Pro Gly Arg Ala 165 170 175 Ile Pro Tyr Gly Gln His Asp Pro Pro Gly Arg Ala Gly Val Arg Gly 180 185 190 Pro His Pro Ala Asp Leu Ala Arg His Lys His Arg Val Gly Gly Pro 195 200 205 Ser Gly Gly Gln Thr His Arg Pro Pro Gly Gln Thr Pro Ala Pro Arg 210 215 220 Arg Ala Ala 225 <210> 8 <211> 181 <212> PRT <213> 人工序列(Artificial Sequence) <400> 8 Met Ala Ser Tyr Pro Cys His Gln His Ala Ser Ala Phe Asp Gln Ala 1 5 10 15 Ala Arg Ser Arg Gly His Ser Asn Arg Arg Thr Ala Leu Arg Pro Arg 20 25 30 Arg Gln Gln Glu Ala Thr Glu Val Arg Leu Glu Gln Lys Met Pro Thr 35 40 45 Leu Leu Arg Val Tyr Ile Asp Gly Pro His Gly Met Gly Lys Thr Thr 50 55 60 Thr Thr Gln Leu Leu Val Ala Leu Gly Ser Arg Asp Asp Ile Val Tyr 65 70 75 80 Val Pro Glu Pro Met Thr Tyr Trp Gln Val Leu Gly Ala Ser Glu Thr 85 90 95 Ile Ala Asn Ile Tyr Thr Thr Gln His Arg Leu Asp Gln Gly Glu Ile 100 105 110 Ser Ala Gly Asp Ala Ala Val Val Met Thr Ser Ala Gln Ile Thr Met 115 120 125 30 CN 111556899 A 序 列 表 10/11 页 Gly Met Pro Tyr Ala Val Thr Asp Ala Val Leu Ala Pro His Val Gly 130 135 140 Gly Arg Leu Gly Val His Met Pro Arg Pro Arg Pro Ser Pro Ser Ser 145 150 155 160 Ser Thr Ala Ile Pro Ser Pro Pro Ser Cys Ala Thr Arg Pro Arg Asp 165 170 175 Thr Leu Trp Ala Ala 180 <210> 9 <211> 993 <212> DNA <213> 人工序列(Artificial Sequence) <400> 9 ttagtcgtaa tccaggataa agacgtgcat gggacggagg cgtttggcca agacgtccaa 60 ggcccaggca aacacgttat acaggtcgcc gttgggggcc agcaactcgg gggcccgaaa 120 cagggtaaat aacgtgtccc cgatatgggg tcgtgggccc gcgttgctct ggggctcggc 180 accctggggc ggcacggccg tccccgaaag ctgtccccaa tcctcccacc acgacccgcc 240 gccctgcaga taccgcaccg tattggcaag cagcccgtaa acgcggcgaa tcgcggccag 300 catagccagg tcaagccgct cgccggggcg ctggcgtttg gccaggcggt cgatgtgtct 360 gtcctccgga agggccccca acacgatgtt tgtgccgggc aaggtcggcg ggatgagggc 420 cacgaacgcc agcacggcct ggggggtcat gctgcccata aggtatcgcg cggccgggta 480 gcacaggagg gcggcgatgg gatggcggtc gaagatgagg gtgagggccg ggggcggggc 540 atgtgaactc ccagcctccc ccccgacatg aggagccaga acggcgtcgg tcacggcata 600 aggcatgccc attgttatct gggcgcttgt cattaccacc gccgcgtccc cggccgatat 660 ctcaccctgg tcgaggcggt gttgtgtggt gtagatgttc gcgattgtct cggaagcccc 720 cagcacctgc cagtaagtca tcggctcggg tacgtagacg atatcgtcgc gcgaacccag 780 ggccaccagc agttgcgtgg tggtggtttt ccccatcccg tgaggaccgt ctatataaac 840 ccgcagtagc gtgggcattt tctgctccag gcggacttcc gtggcttctt gctgccggcg 900 agggcgcaac gccgtacgtc ggttgctatg gccgcgagaa cgcgcagcct ggtcgaacgc 960 agacgcgtgt tgatggcagg ggtacgaagc cat 993 <210> 10 <211> 684 <212> DNA <213> 人工序列(Artificial Sequence) <400> 10 atggcttcgt acccctgcca tcaacacgcg tctgcgttcg accaggctgc gcgttctcgc 60 ggccatagca accgacgtac ggcgttgcgc cctcgccggc agcaagaagc cacggaagtc 120 cgcctggagc agaaaatgcc cacgctactg cgggtttata tagacggtcc tcacgggatg 180 gggaaaacca ccaccacgca actgctggtg gccctgggtt cgcgcgacga tatcgtctac 240 31 CN 111556899 A 序 列 表 11/11 页 gtacccgagc cgatgactta ctggcaggtg ctgggggctt ccgagacaat cgcgaacatc 300 tacaccacac aacaccgcct cgaccagggt gagatatcgg ccggggacgc ggcggtggta 360 atgacaagcg cccagataac aatgggcatg ccttatgccg tgaccgacgc cgttctggct 420 cctcatgtcg gggggggagg ctgggagttc acatgccccg cccccggccc tcaccctcat 480 cttcgaccgc catcccatcg ccgccctcct gtgctacccg gccgcgcgat accttatggg 540 cagcatgacc ccccaggccg tgctggcgtt cgtggccctc atcccgccga ccttgcccgg 600 cacaaacatc gtgttggggg cccttccgga ggacagacac atcgaccgcc tggccaaacg 660 ccagcgcccc ggcgagcggc ttga 684 <210> 11 <211> 546 <212> DNA <213> 人工序列(Artificial Sequence) <400> 11 atggcttcgt acccctgcca tcaacacgcg tctgcgttcg accaggctgc gcgttctcgc 60 ggccatagca accgacgtac ggcgttgcgc cctcgccggc agcaagaagc cacggaagtc 120 cgcctggagc agaaaatgcc cacgctactg cgggtttata tagacggtcc tcacgggatg 180 gggaaaacca ccaccacgca actgctggtg gccctgggtt cgcgcgacga tatcgtctac 240 gtacccgagc cgatgactta ctggcaggtg ctgggggctt ccgagacaat cgcgaacatc 300 tacaccacac aacaccgcct cgaccagggt gagatatcgg ccggggacgc ggcggtggta 360 atgacaagcg cccagataac aatgggcatg ccttatgccg tgaccgacgc cgttctggct 420 cctcatgtcg gggggaggct gggagttcac atgccccgcc cccggccctc accctcatct 480 tcgaccgcca tcccatcgcc gccctcctgt gctacccggc cgcgcgatac cttatgggca 540 gcatga 546 32 CN 111556899 A 说 明 书 附 图 1/28 页 图1 33 CN 111556899 A 说 明 书 附 图 2/28 页 图2 34 CN 111556899 A 说 明 书 附 图 3/28 页 图3 35 CN 111556899 A 说 明 书 附 图 4/28 页 图4 36 CN 111556899 A 说 明 书 附 图 5/28 页 图5 37 CN 111556899 A 说 明 书 附 图 6/28 页 图6 38 CN 111556899 A 说 明 书 附 图 7/28 页 图7 39 CN 111556899 A 说 明 书 附 图 8/28 页 图8 40 CN 111556899 A 说 明 书 附 图 9/28 页 图9 41 CN 111556899 A 说 明 书 附 图 10/28 页 图10 42 CN 111556899 A 说 明 书 附 图 11/28 页 图11 43 CN 111556899 A 说 明 书 附 图 12/28 页 图12 44 CN 111556899 A 说 明 书 附 图 13/28 页 图13 45 CN 111556899 A 说 明 书 附 图 14/28 页 图14 46 CN 111556899 A 说 明 书 附 图 15/28 页 图15 47 CN 111556899 A 说 明 书 附 图 16/28 页 图16 48 CN 111556899 A 说 明 书 附 图 17/28 页 图17 49 CN 111556899 A 说 明 书 附 图 18/28 页 图18 50 CN 111556899 A 说 明 书 附 图 19/28 页 图19 51 CN 111556899 A 说 明 书 附 图 20/28 页 图20 52 CN 111556899 A 说 明 书 附 图 21/28 页 图21 53 CN 111556899 A 说 明 书 附 图 22/28 页 图22 54 CN 111556899 A 说 明 书 附 图 23/28 页 图23 55 CN 111556899 A 说 明 书 附 图 24/28 页 图24 56 CN 111556899 A 说 明 书 附 图 25/28 页 图25 57 CN 111556899 A 说 明 书 附 图 26/28 页 图26 58 CN 111556899 A 说 明 书 附 图 27/28 页 图27 59 CN 111556899 A 说 明 书 附 图 28/28 页 图28 60












