技术摘要:
本发明涉及用于制备3,6‑脱水‑L‑半乳糖的方法及3,6‑脱水‑L‑半乳糖的用途。更具体地,通过化学和酶的方法制备高产量的作为组成琼脂的单糖的3,6‑脱水‑L‑半乳糖,而且展示出3,6‑脱水‑L‑半乳糖的生理活性,如美白、保湿、抗氧化、抗炎症活性等,从而使之应用于 全部
背景技术:
琼脂(或琼脂糖)为组成红藻类的主要的多糖,其为两种单糖,即3,6-脱水-L-半乳 糖和D-半乳糖,通过α-1,3键与β-1,4键交叉相连而形成的聚合物。众所周知,通过使用化学 催 化 剂 如 盐 酸 、硫 酸 和乙 酸 来 非 特 异 性 地 水 解 琼 脂 糖 而 生 成 的 琼 脂 寡 糖 (Agarooligosaccharide)能够展示优异的生理活性,如抗氧化、抗炎、抗癌、增白和抗过敏 的活性。基于这些多种生理活性,琼脂寡糖和作为双糖的新琼脂二糖(Neoagarobiose)已被 广泛地用作食品和美容产业中的功能性物质。 作为组成所述琼脂寡糖的单糖之一的3,6-脱水-L-半乳糖存在以下问题:由于3, 6-脱水-L-半乳糖具有不稳定的还原端,并且在存在高浓度强酸的高温反应条件下易被转 化成羟甲基糠醛,通过常用的化学处理方法所生成的作为单糖的3,6-脱水-L-半乳糖的产 率极低,而且容易被过度降解(Jol et al(1999)Anal Biochem.268,213-222,Kim et al (2010)Bull Korean Soc.31(2)511-514)。此外,虽然使用化学处理的水解具有以下优点, 如由于生产成本低且处理条件简单,可容易应用于商业化,然而还存在以下问题,即由于所 述化学处理会非特异性地切断连接键,当特异性连接键被切断而获得产品时所生成的期望 产品的产率极低(Chen et al(2005)Food Technol Biotechnol.43(1)29-36)。进一步,近 年来有报道过通过特异性地切断3,6-脱水-L-半乳糖中的键合来生成单糖的酶,然而尚未 出现从反应产物中仅分离、提纯及定量3,6-脱水-L-半乳糖的研究。
技术实现要素:
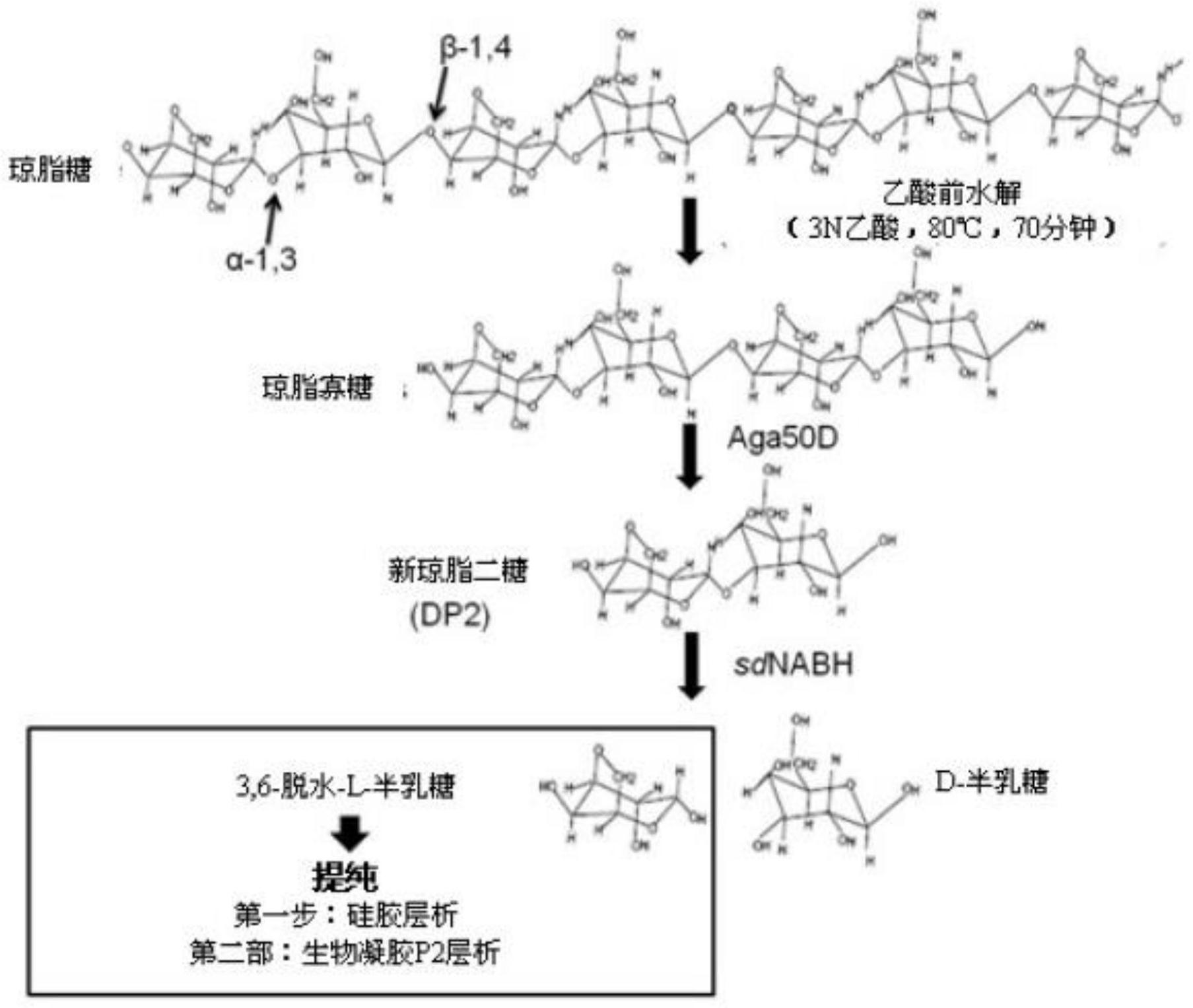
技术问题 因此,本发明在于,提供能够最大程度降低由化学处理引起的过度降解效果并通过酶 降解制备高产率的3,6-脱水-L-半乳糖的方法。 此外,本发明在于,通过查明3,6-脱水-L-半乳糖的生理活性并使之应用于工业 上。 技术方案 根据本发明的一方面,本发明提供用于制备3,6-脱水-L-半乳糖的方法,该方法包括: 通过使琼脂糖与弱酸在浓度为0.5-60%(w/v)、温度为40-150℃、旋转速度为100-200rpm的 条件下反应30分钟~6个小时来制备琼脂寡糖;以及,使该琼脂寡糖与琼脂糖降解酶和新琼 脂二糖水解酶在温度为20-40℃、旋转速度为0-200rpm的条件下反应30分钟~7天。 此时,所述琼脂糖降解酶可以为一种能够切断琼脂糖的D-半乳糖和3,6-脱水-L- 半乳糖之间的β-1,4-糖苷键的酶。更具体地,所述琼脂糖降解酶可由SEQ ID NO:1所示的氨 基酸序列表示。 3 CN 111544437 A 说 明 书 2/14 页 所述新琼脂二糖水解酶可由SEQ ID NO:3所示的氨基酸序列表示。 根据一个示例性实施例,所述琼脂糖降解酶和新琼脂二糖水解酶可源自降解糖噬 糖菌(Saccharophagus degradans,S.degradans)2-40。 根据一个示例性实施例的用于制备3,6-脱水-L-半乳糖的方法可进一步包括:通 过对所述3,6-脱水-L-半乳糖依次进行吸附层析和凝胶渗透层析来分离及提纯所述3,6-脱 水-L-半乳糖。 根据本发明的另一方面,本发明提供包含3,6-脱水-L-半乳糖的用于皮肤美白或 保湿的化妆品组合物。 根据本发明的又一方面,本发明提供3,6-脱水-L-半乳糖在皮肤美白或保湿中的 美容用途。 根据本发明的又一方面,本发明提供包含3,6-脱水-L-半乳糖的用于预防或治疗 皮肤色素沉着症的药物组合物。 根据本发明的又一方面,本发明提供3,6-脱水-L-半乳糖在制备用于预防或治疗 皮肤色素沉着症的药物组合物中的用途。 根据本发明的又一方面,本发明提供用于美白或保湿有需要皮肤美白或保湿的哺 乳动物的,优选地有需要皮肤美白或保湿的人的美容或医疗方法。其中,所述美容或医疗方 法包括:将有效量的3,6-脱水-L-半乳糖,优选地将有效量的包含3,6-脱水-L-半乳糖的药 物或化妆品组合物进行给药。 根据本发明的又一方面,本发明提供用于治疗与色素沉着的调节相关的皮肤的病 态、疾病和/或病变的美容或医疗方法。其中,所述方法包括:将包含3,6-脱水-L-半乳糖的 药物或化妆品组合物涂敷于皮肤上,而且所述病态、疾病和/或病变可以是由于黑色素合成 的增加而局部发生的,且其可以为选自黄褐斑、雀斑、雀斑样痣、母斑、由药物引起的色素沉 着、炎症后色素沉着、发生于皮炎上的过度色素沉着中的至少一种。 根据本发明的又一方面,本发明提供包含3,6-脱水-L-半乳糖的用于预防或治疗 炎症性疾病的药物组合物。 根据本发明的又一方面,本发明提供用于治疗动物的炎症性疾病的方法。其中,该 方法包括:将包含药学有效量的3,6-脱水-L-半乳糖的用于预防或治疗炎症性疾病的组合 物向受试者进行给药。 根据本发明的又一方面,本发明提供3,6-脱水-L-半乳糖在制备用于预防或治疗 炎症性疾病的药物组合物中的用途。 有益效果 根据本发明的实施例,通过在最大程度降低根据化学处理的过度降解效果的温和化学 处理条件下制备低聚糖并使之经过酶处理生成高产率的作为单糖的3,6-脱水-L-半乳糖。 此外,根据本发明,3,6-脱水-L-半乳糖的生理活性,如美白、保湿、抗氧化及抗炎 症的活性,首次得到验证,从而使之用于包括食品、化妆品、药品等各种领域中。因此,在生 产红藻源性生物能源时被认可为副产物或发酵抑制物质的3,6-脱水-L-半乳糖可应用于生 产生物能源领域中具有高附加值的物质。 4 CN 111544437 A 说 明 书 3/14 页 附图说明 图1为说明根据本发明一个实施例的从琼脂糖中制备3,6-脱水-L-半乳糖的过程 的图表。在图1中,DP表示多糖的聚合度。 图2展示了从琼脂糖中制备并提纯3,6-脱水-L-半乳糖的过程中获得的薄层层析 (TLC)。在该处理步骤中,道1表示琼脂糖,道2表示醋酸水解物,道3表示Aga50D反应产物,道 4表示sdNABH反应产物,道5表示通过硅胶层析法分离出的3,6-脱水-L-半乳糖,道6表示通 过生物凝胶P2层析法提纯的3,6-脱水-L-半乳糖,Y轴的AHG表示3,6-脱水-半乳糖,以及NAB 表示新琼脂二糖。 图3展示了作为提纯3,6-脱水-L-半乳糖过程中的第一步的硅胶层析-TLC的结果。 在图3中,AHG表示3,6-脱水-半乳糖。 图4展示了(a)D型3,6-脱水-半乳糖的标准物质和(b)根据本发明的一个示例性实 施例所提纯的3,6-脱水-L-半乳糖的GC/MS总离子色谱图。 图5展示了根据本发明的一个示例性实施例所分离并提纯的3,6-脱水-L-半乳糖 的氢核磁共振波谱(1H NMR)分析结果。 图6展示了根据本发明的一个示例性实施例所分离并提纯的3,6-脱水-L-半乳糖 的2D-HSQC NMR分析结果。 图7展示了3,6-脱水-L-半乳糖、新琼脂二糖、D-半乳糖和3,6-脱水-D-半乳糖的美 白活性。在图7中,α-MSH表示α-促黑素细胞激素,NAB表示新琼脂二糖,以及D-AHG和L-AHG则 分别表示D型和L型的3,6-脱水-半乳糖。 图8展示了3,6-脱水-L-半乳糖、新琼脂二糖、D-半乳糖和3,6-脱水-D-半乳糖的抗 氧化活性。 图9展示了在HEMs中L-AHG对由α-MSH诱导的酪氨酸酶表达的影响。其中,图9A展示 了根据L-AHG浓度进行处理后被暴露于α-MSH的细胞中的酪氨酸酶表达的结果,以及图9B展 示了将图9A的结果图示为对β-肌动蛋白的酪氨酸酶相对强度的示意图。 图10展示了在HEMs中L-AHG对由α-MSH诱导的TRP-1表达的影响。其中,图10A展示 了根据L-AHG浓度进行处理后被暴露于α-MSH的细胞中的TRP-1表达的结果,以及图10B展示 了将图10A的结果图示为对β-肌动蛋白的TRP-1相对强度的示意图。 图11展示了L-AHG对体外酪氨酸酶活性的影响。 图12展示了在人角质细胞中L-AHG对HAS2表达的影响。其中,图12A展示了根据经 过的时间用100μg/mL的L-AHG处理后的HAS2表达水平,以及图12B展示了根据L-AHG浓度进 行处理后的HAS2表达水平。 图13展示了在人角质细胞中L-AHG对ERK磷酸化的影响。其中,图13A展示了根据经 过的时间用100μg/mL的L-AHG处理后的ERK磷酸化结果,以及图13B展示了根据L-AHG浓度进 行处理后的ERK磷酸化结果。 图14展示了在人角质细胞中L-AHG对AKT磷酸化的影响。其中,图14A展示了根据经 过的时间用100μg/mL的L-AHG处理后的AKT磷酸化结果,以及图14B展示了根据L-AHG浓度进 行处理后的AKT磷酸化结果。 5 CN 111544437 A 说 明 书 4/14 页












