技术摘要:
本发明公开了一种具C环骈合内酯环新颖骨架的松香烷类化合物,以松香烷二萜醌类化合物为原料,在金属催化剂的作用下,通过与酸酐缩合得到具有C环骈合内酯环新颖骨架的松香烷类化合物。本发明构建的一类新的松香烷类化合物,有效改进了化合物的非平面性,不仅在结构上具 全部
背景技术:
松香烷二萜类化合物的研究最早是在19世纪初,由El l i n g s o n从松香 (colophony)中发现首个松香烷二萜化合物松香酸(Ellingson ,E .O .Abietic acid and some of its salts.Journal of the American Chemical Society.1914,36,325-335.) , 研究表明,其具有抗菌、抗胃酸分泌等多种药理作用(San Feliciano,A.;Gordaliza , M.; Salinero ,M .A .et al .Abietane acids:sources ,biological activities ,and therapeutic uses.Planta Medica.1993,59,485-90.)。之后引起了人们的广泛关注。自然 界中,松香烷二萜主要存在于唇形科、松科、菊科、大戟科、豆科、卫矛科等高等植物中,尤以 唇形科植物中分布较为广泛,其基本骨架为氢化菲结构。在唇形科植物中,又以鼠尾草属及 香茶菜属中分布最广。 此后,国内外学者相继发现同类化合物还具有抗肿瘤、抗炎、抗病毒等作用。该类 化合物中,研究较深入的是鼠尾草属植物中的二萜类化合物,主要结构类型为松香烷型二 萜醌类化合物,其中许多具有较显著的生理活性。药理学实验证实,该类化合物具有抗肿瘤 (Zhang ,Y .;Jiang ,P.X .;Ye ,M .et al . Tanshinones:sources ,pharmacokinetics and anti-cancer activities.International Journal of Molecular Sciences.2012,13, 13621-13666.)、消炎、扩冠、消除自由基、抗血小板凝聚等多种作用(Jiang ,Z.Q.;Gao,W.; Huang ,L .Q . Tanshinones ,critical pharmacological components in Salvia miltiorrhiza. Frontiers in Pharmacology.2019,10,1-14.)。为了更好地发挥其药效作 用,提高成药性,国内外许多学者开展了结构改造工作,其中有些化合物经过简单的结构修 饰,已在临床上广泛应用。如丹参酮IIA磺酸钠,为丹参酮IIA在 D环引入磺酸基的产物,在 临床上用于防治冠心病心绞痛。 目前对该类化合物的结构改造方法,归纳起来主要有两类:即针对A环和D环的修 饰。这是因为,在A环为脂环的情况下,苄位较活泼,反应位点也较多,可在不同位置上引入 各种类型的取代基;而D环的呋喃环,氢更是活性位点,如制备了丹参酮IIA磺酸钠盐,显著 提高了其水溶性。然而目前来看,这两种结构修饰的效果并不理想,对该类化合物的活性提 4 CN 111606917 A 说 明 书 2/13 页 高有限,研究发现,丹参酮IIA磺酸钠盐药效甚至低于丹参酮IIA,推测可能由于磺酸钠盐为 离子型化合物,难以通过以脂质及蛋白质成分为基础的生物膜结构系统(石远,李秀英,王 天怡等丹参酮IIA与丹参酮IIA磺酸钠体内药动学与药效学,中国药剂学杂志,2009,7(3), 143-153.)。丹参酮IIA磺酸钠盐的最大优点是成为水溶性化合物,可以注射给药,该药为我 国上世纪80年代批准的上市药物。但在现代,这种以牺牲药效提高水溶性的策略已经不常 用。此外,这些结构改造方法还受限于两个条件:(1)A环必须为脂环;(2) 必须有D-呋喃环 的存在。 申请人经过研究,发现该类化合物经过对C环邻醌片段进行结构修饰,可以显著提 高其抗菌、抗肿瘤活性(Zeng ,L .W .;Zhou ,C .X .;et al .Design , synthesis ,and antimicrobial activities of new tanshinone IIA esters .Natural Product Research,2016,30,2662-2668.侯阿芳,曾林伟,甘礼社等丹参新酮 C环酚酯衍生物的设计 合成及抗肿瘤活性研究.中国现代应用药学,2016,33, 1396-1402.),因此C环的结构改造 对提到其成药性具有重要的科学意义,然而因为骨架钝性的原因,该类化合物的C环恰好又 很难进行改造。申请人经过长期深入的研究,成功开发了一类以松香烷型二萜醌为前体合 成C环新骨架的改造方法,获得了C环骈合内酯环的新颖结构,实现了该类化合物药效潜力 更大的新骨架构建。
技术实现要素:
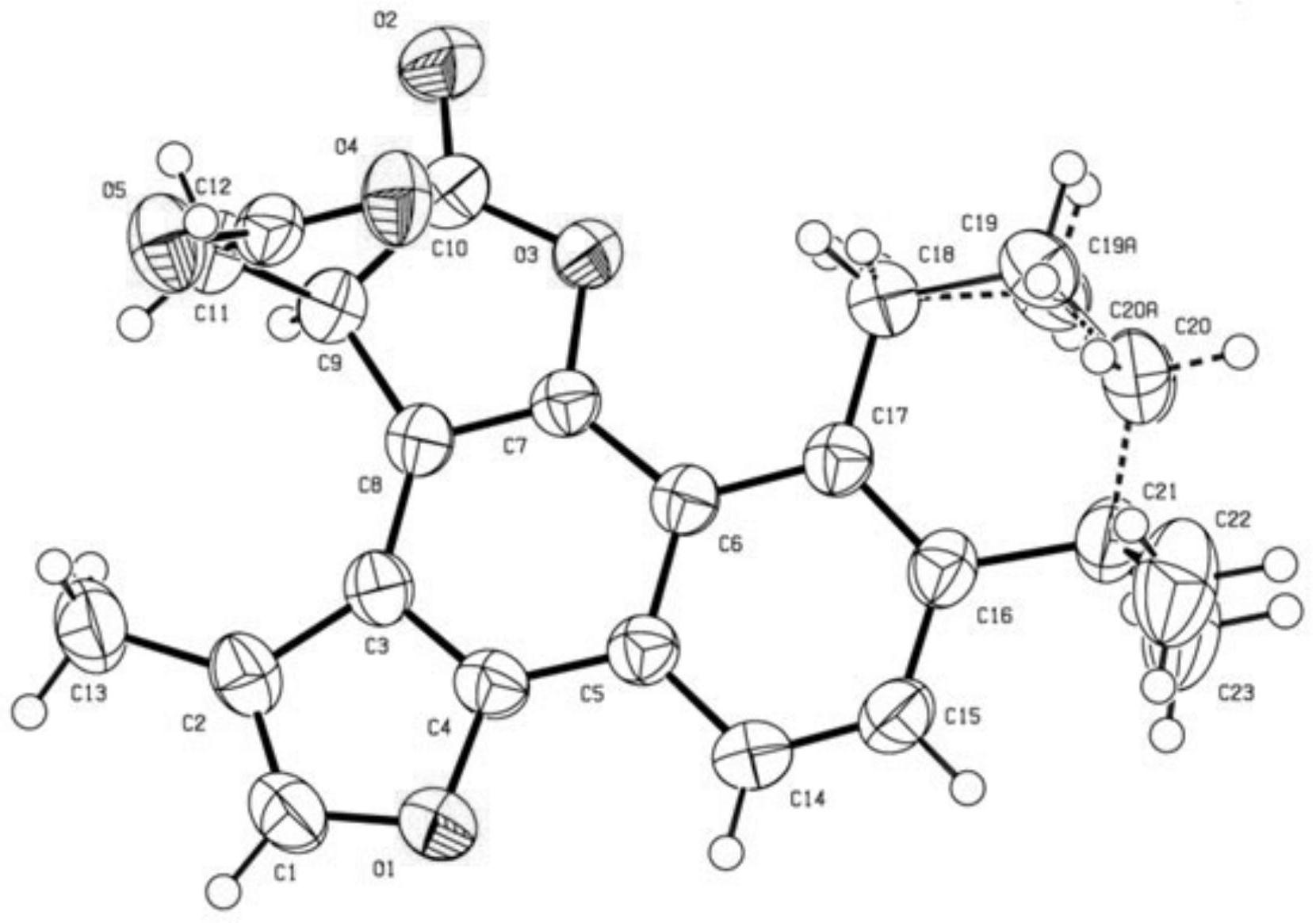
针对现有技术存在的不足,本发明的目的首先在于提供一种具C环骈合内酯环新 颖骨架的松香烷类化合物,有效改进了化合物的非平面性,不仅在结构上具有新颖性,而且 相应的生物活性也得到显著提升,提示该类化合物具有更大的成药潜力;其次在于提供一 种以松香烷型二萜醌为前体合成C环新骨架的松香烷类化合物的制备方法,并将其应用在 相关医学的临床使用中。 为了实现第一发明目的,本发明提供如下技术方案: 一种具有C环骈合内酯环新颖骨架的松香烷类化合物,包括A、B、C的三环骨架结 构,具有如下I、II、III的结构通式: 所述式I结构类型的化合物,n=0~2。 所述式I、II、III结构化合物,A环可以为脂环或芳环,B环和C环均为芳环。 应用时为具有如下式I、II、III结构的化合物或者其可药用盐。所述式I、II、 III 结构化合物的可药用盐是指内酯环侧链羧基与碱进行反应生成的可药用盐。 所述“式I、II、III结构化合物的可药用盐”中的可药用盐,其为不引起药理上的副 作用的、且常规使用的盐形式,没有特别的限制,包括式I、II、III结构化合物与任何无机碱 或有机碱反应所生成的盐,如钠盐、钾盐、镁盐、铵盐等。例如,可与无机碱诸如碳酸氢钠、碳 5 CN 111606917 A 说 明 书 3/13 页 酸钠、氢氧化钠、碳酸钾、氢氧化钾、氢氧化镁成盐,优选碳酸氢钠、碳酸钠和碳酸钾;也可与 有机碱诸如甲胺、乙胺、乙醇胺、乙二胺、二甲胺、三甲胺、二乙胺、三乙胺、丙胺、丁胺成盐, 优选二甲胺和二乙胺。 所述式I、II、III结构化合物,A环4位上取代基为烷基或氢; 当A环为脂环时,优选为4位有偕二甲基取代的脂环;当A环为芳环时,优选为4位有 甲基取代的芳环。 R1、R2为烷基或氢,C环外取代基为烷基,也形成呋喃环或二氢呋喃环骈合结构;当C 环外取代基为烷基时,优选R1为异丙基的取代基;当C环外成环时,优选呋喃环或二氢呋喃 环骈合结构。即当C环外13位取代基R1为异丙基时,14 位R2为氢;当13位异丙基末端被氧化 时,可与14位缩合形成呋喃环或二氢呋喃环结构。 所述式I、II、III结构化合物,I类结构是基础结构,II、III类结构为I类结构转化 而来。即当n=0时,I类结构通过进一步反应转化为II类结构;当n=1时, I类结构通过进一 步反应转化为III类结构。 本发明另一方面还提供了上述具C环骈合内酯环新颖骨架的松香烷类化合物的制 备方法,该制备方法包含以下依次进行的步骤: (1)I类结构化合物的合成 将原料松香烷型二萜醌类化合物及酸酐按摩尔比1:1~1:1.5置于反应瓶中,加入 溶剂、DMAP以及单质还原性金属,于氮气保护下加热,TLC监测反应完全后,过滤,滤液蒸干 后通过重结晶或柱层析,获得I类结构目标产物。 (2)II、III类结构化合物的合成 将I类结构化合物溶解后加入反应瓶中,加入DCC,DMAP,有机碱,于氮气保护下加 热,TLC监测反应完全后,过滤,滤液蒸干后通过重结晶或柱层析,根据n值不同,分别获得 II、III类结构目标产物。 经上述反应制备的四类化合物均为外消旋体,即C环的苄位碳为手性中心,包含R, S两种构型,通过手性拆分,可以得到单一光学活性体。 6 CN 111606917 A 说 明 书 4/13 页 所述步骤(1)、(2)中的原料及试剂,其中松香烷型二萜醌选自具有邻醌结构类型 的化合物,优选的,鼠尾草属植物中的邻醌类化合物,更优选的,鼠尾草属植物丹参中的丹 参酮I、丹参酮IIA、隐丹参酮、丹参新酮;酸酐选自环二酸酐,优选的,丁二酸酐、戊二酸酐、 己二酸酐;单质还原性金属选自镁粉、铁粉、锌粉;有机碱选自三乙胺及N,N-二异丙基乙胺 (DIPEA)。 本发明的构建C环骈合内酯环新颖骨架的松香烷类衍生物反应机理,以丹参酮IIA 和琥珀酸酐在DMAP和锌粉的作用下反应示意如下: 以丹参酮IIA和琥珀酸酐在DMAP和锌粉的作用下反应示意如下"~9"推测在整个 反应体系中,由于反应体系呈微碱性,而五元内酯环由于侧链比较长,内酯环比较容易开 环,转而另外一端的羧酸会与酚羟基成酯,形成比较稳定的七元内酯环,从而得到产物。 在该反应中,首先丹参酮IIA的10位羰基被锌粉还原,与被DMAP活化的琥珀酸酐发 生酰化反应,DMAP离去后,在少量水的作用下,锌以氢氧化锌形式脱去。随后异构化的酯羰 基与11位羰基缩合,脱去1分子水后芳构化形成产物。 本发明的I类结构通过进一步反应转化为II、III类结构的反应机理以丹参酮IIA 与戊二酸酐在碱性催化剂及缩合剂存在下反应示意如下: 7 CN 111606917 A 说 明 书 5/13 页 推测在整个反应体系中,由于反应体系呈微碱性,而五元内酯环由于侧链比较长, 内酯环比较容易开环,转而另外一端的羧酸会与酚羟基成酯,形成比较稳定的七元内酯环, 从而得到产物。 本发明再一方面还提供了一种肿瘤及心脑血管疾病的治疗药物,该药物中包含上 述的一种具C环骈合内酯环新骨架的松香烷类化合物。 在本发明的一个实施方案中,该药物中可以单独添加本发明的具C环骈合内酯环 新骨架的松香烷衍生物;也可以共同添加该类新骨架衍生物和其他已知的抗肿瘤及心脑血 管治疗药物活性成分。 在本发明的另一个实施方案中,该抗肿瘤及心脑血管疾病治疗药物中,作为活性 成分的该类松香烷二萜衍生物的含量范围为0.1%-99.9%。优选50%~99.9%。 本领域技术人员可以根据该药物的使用剂量、剂型、给药方式选择该药物中该类 衍生物的含量。 该抗肿瘤及心脑血管疾病治疗药物的制剂可以为片剂、胶囊剂、口崩片、滴丸、喷 雾剂、气雾剂、注射剂等。 本发明的有益效果在于,首先提供了一种新的具C环骈合内酯环新骨架的松香烷 化合物、其衍生物及其药学上可接受的盐及其制备方法;其次,该类化合物具有较好的抗肿 瘤及心脑血管活性。体外实验表明,该类化合物对人肺腺癌细胞A549的具有较好的抑制活 性;对心肌细胞H9C2具有显著的保护作用。体内动物试验表明,该类化合物经腹腔注射给 药,对肺癌荷瘤小鼠具有良好的抑瘤效果;对大鼠大脑中动脉阻塞模型(MCAO)可明显缩小 脑梗塞范围,对局灶性脑缺血损伤具有很好的保护作用,表明该类化合物在临床上具有重 要的应用价值。 附图说明 图1为化合物1的X单晶衍射图。 图2为化合物2的氢谱图。 图3为化合物2的碳谱图。 图4为化合物3的氢谱图。 8 CN 111606917 A 说 明 书 6/13 页 图5为化合物3的碳谱图。 图6为化合物4的氢谱图。 图7为化合物4的碳谱图。 图8为化合物5的氢谱图。 图9为化合物5的碳谱图。 图10为化合物6的质谱图。 图11为化合物6的碳谱图。 图12为化合物7的氢谱图。 图13为化合物7的高分辨质谱图。 图14为化合物8的高分辨质谱图。 图15为化合物9的高分辨质谱图。












