 技术摘要:
技术摘要: 本发明涉及一种组合物,其包含作为有效成分的益生菌和具有与IgE结合能力的多肽。特别地,根据本发明,在联合施用益生菌和含有IgE Fc受体的α亚基的胞外域的重组蛋白时,检测出显著的降低食物过敏的协同作用。由于与常规药物组合物相比,本发明的组合物能够对IgE介导的 全部
背景技术:
食物过敏是由于对非致病性食物抗原(过敏原)的免疫抵抗力降低而引起的疾病。
该疾病可能会由于饮食受限而导致生活质量下降,并且在发生急性过敏反应和慢性过敏反
应的情况下还可能危及生命。在工业化和西化的现代社会中,诸如过敏性鼻炎和特应性皮
炎之类的过敏性疾病以及此类的食物过敏正在迅速蔓延。此外,过敏性休克是一种严重的
过敏反应,其发病人数也在增加。这些免疫疾病严重损害了生活质量,社会的经济成本也随
之飙升。因此,迫切需要治疗这些疾病的方法。
尽管食物过敏性疾病可以通过IgE介导或非IgE介导的免疫反应发生,但IgE介导
的食物过敏是其中最常见的。在IgE介导的食物过敏中,过敏原与IgE结合,然后过敏原结合
的IgE交联FcεRI(一种效应细胞诸如肥大细胞和嗜碱性粒细胞上表达的高亲和力IgE Fc受
体),从而诱导效应细胞的活化。在效应细胞被活化的情况下,调节剂被释放,从而引起速发
型超敏反应。除了食物过敏性疾病以外,大多数的过敏性疾病也是由于免疫球蛋白E(IgE)
导致的过度免疫反应所引起的。IgE是一种通常以非常低的浓度存在于血清中的抗体。无害
的抗原也会产生IgE。在没有任何特定刺激的情况下IgE的数量增加时,可能会引起过敏性
疾病。数量异常增加的IgE可以与肥大细胞、嗜碱性粒细胞等表面表达的高亲和力IgE Fc受
体(FcεRI)结合。
IgE与IgE Fc受体之间的这种结合可导致肥大细胞或嗜碱性粒细胞释放一些化学
介质,例如组胺、白三烯、前列腺素、缓激肽和血小板活化因子。肥大细胞或嗜碱性粒细胞释
放的这些化学介质会导致过敏症状。特别地,在IgE和FcεRI彼此结合的情况下,可能表现出
恶化的过敏症状。已知在过敏的患者中,表达FcεRI的细胞会增加。
已经提出了治疗过敏性疾病的多种方法,例如避免过敏原、施用抗过敏药、调节体
内IgE的合成以及开发抗IgE抗体。但是,这些方法具有众多缺点,例如无法治愈过敏的根本
原因、药物功效不足以及发生严重的副作用。
同时,已有研究使用例如乳酸菌等微生物的方法来治疗或改善过敏性疾病。这种
健康的微生物被称为益生菌。但是,尚未建立发现和评估用于免疫控制(例如过敏抑制)的
益生菌的技术。特别地,关于益生菌潜在作用机理的研究还不够多,并且大多数研究是在体
外进行的。换句话说,尽管益生菌通常为口服摄入,但迄今为止,大多数研究都集中在使用
细胞系的体外实验中,并且这些实验方法存在一个主要缺点,即无法提供一种替代物来替
代对人类摄入益生菌的情况下可能表现出来的功能的研究。
此外,已有研究将免疫球蛋白组合物用于治疗过敏性疾病。据报道,这种组合物可
用于治疗IgE介导的疾病,包括过敏和哮喘(KR10-1783272B1)。特别地,已经开发出靶向IgE
抗体的Fc部分的奥马珠单抗(omalizumab,商品名:Xolair),并将其用作顽固性重度哮喘和
顽固性荨麻疹的治疗剂。然而,为了维持疗效,需要施用大剂量的奥马珠单抗。因此,据报道
4
CN 111587118 A 说 明 书 2/25 页
奥马珠单抗会导致高成本负担,以及具有诸如血管性水肿和过敏反应等副作用(The
Journal of Clinical Investigation,Volume 99,Number 5,March 1997,915-925)。
尽管奥马珠单抗引起副作用的潜在机制尚未阐明,但可以预测奥马珠单抗是一种
IgG1抗体。一项针对小鼠模型的研究表明,大量抗原特异性的IgG1抗体可以在抗原丰富的
环境中通过低亲和力的IgG受体FcγRIII和血小板活化因子诱导被动系统性过敏(PSA)。此
外,由于缺乏FcεRI信号传导,这种IgG介导的过敏反应会过度发生。因此,在向表现出具有
高水平IgE的患有过敏性疾病的患者中注射大量的奥马珠单抗的情况下,有可能引起被动
系统性过敏反应。近期有报道称人体内表达的低亲和力IgG受体FcγRIIA也与IgG介导的过
敏有关。另外,上市后的研究还报道有发生过敏性肉芽肿性血管炎和特发性严重血小板减
少症等异常反应。
技术问题
尽管已经对过敏性疾病进行了诸多研究,但迄今为止尚未开发出能够显著改善过
敏性疾病的方法。本发明的目的是提供一种用于治疗或预防此类过敏性疾病的组合物。
解决问题
本发明的一个方面提供了一种组合物,其包含作为活性成分的益生菌和具有与
IgE结合能力的多肽。
在另一方面提供了一种用于治疗或预防过敏性疾病的药物组合物,其包含所述组
合物作为活性成分。在另一方面提供了一种用于改善或减轻过敏症状的保健功能性食品组
合物,其包含该组合物作为活性成分。
在又一方面提供了一种用于治疗或预防过敏性疾病的试剂盒,其包括含有益生菌
的第一组合物和含有具有与IgE结合能力的多肽的第二组合物。
发明的有益效果
本发明中,包含作为活性成分的益生菌和具有与IgE结合能力的多肽的组合物表
现出改善体内过敏反应的优异效果。因此,该组合物可用于作为治疗或预防严重过敏性疾
病的药物组合物。此外,从本发明的组合物可以用于口服免疫治疗的角度来看,该组合物不
仅可以对食物过敏更有效的同时减少副作用,而且对于治疗患有IgE介导的过敏的儿童也
是理想的选择。因此,该组合物可用来作为改善或减轻过敏症状的保健功能性食品。
附图说明
图1显示了形成本发明的多肽二聚体的一个实施方案(IgETRAP)的单体的结构示意
图。IgETRAP的一个实施方案可以是由来自人FcεRIα(FcεRIα胞外域中从第26个氨基酸至第
205个氨基酸的区域,180个氨基酸)和人IgD/IgG4杂合Fc(245个氨基酸)的425个氨基酸组
成。IgD/IgG4杂合Fc具有FcRn结合位点(右阴影线),但是缺乏FcγR和C1q的结合位点(左阴
影线)。其中,IgD可以是从第133个氨基酸至第170个氨基酸的区域(38aa),IgG4可以是从第
121个氨基酸至第327个氨基酸的区域(207aa)。
图2显示了IgETRAP同源二聚体的三维结构模型。该结构显示FcεRIα(蓝色)、IgD铰
链(黄色)和IgG4 Fc(绿色)。
图3为在每种细胞系中产生的具有与IgE结合能力的多肽的SDS-PAGE结果图(图
3A)。其中可以看出在还原和非还原条件下均未产生截短的形式(图3A和3B)。
5
CN 111587118 A 说 明 书 3/25 页
图4显示了等电聚焦(GEL-IEF)实验的结果,进行该实验以鉴定在每个细胞系中产
生的具有与IgE结合能力的多肽的唾液酸含量的增加。由于引入唾液酸转移酶基因而导致
带负电荷的唾液酸含量的增加,因此具有降低的主要等电点(pI)的蛋白质的含量增加。由
此可知,通过添加唾液酸转移酶,酸性蛋白质的含量增加。
图5显示了本发明的一个实施方案中非还原形式和还原形式的多肽二聚体蛋白质
(IgETRAP)的SDS-PAGE结果。特别地,可以看出即使在对应于输入的培养上清液中,多肽二聚
体也具有高纯度。
图6显示了通过在非还原和还原条件下对IgETRAP进行SDS-PAGE分析而获得的结
果。
图7显示了奥马珠单抗与IgE的结合能力。该图显示了通过固定奥马珠单抗并根据
所处理的IgE浓度分析其结合能力而获得的结果。使用表面等离子共振(SPR)分析人IgE和
奥马珠单抗之间的相互作用,并计算每个分子的结合亲和力。
图8显示了本发明的一个实施方案中多肽二聚体蛋白(IgETRAP)对IgE的结合能力。
该图显示了通过固定IgETRAP并根据所处理的IgE浓度分析其结合能力而获得的结果。使用
表面等离子共振(SPR)分析人IgE和IgETRAP之间的相互作用,并计算每个分子的结合亲和
力。
图9-13显示了通过生物膜层干涉法(BLI)测定本发明的一个实施方案中多肽二聚
体蛋白(IgETRAP)和奥马珠单抗与IgG受体FcγRI(图9)、FcγRIIA(图10)、FcγRIIB(图11)、
FcγRIIIA(图12)和FcγRIIIB(图13)的相互作用。
图14为显示通过量化IgETRAP和IgG受体之间以及奥马珠单抗和IgG受体之间的结
合能力而获得的图。
图15A为显示本发明的一个实施方案中多肽二聚体蛋白(IgETRAP)在不同浓度下对
小鼠来源的肥大细胞的活性的抑制能力的图。
图15B为显示本发明的一个实施方案中多肽二聚体蛋白(IgETRAP)和Xolair(奥马
珠单抗)对表达人FcεRI的小鼠源性肥大细胞的活性的抑制能力的比较的图。
图16示显示了本发明的一个实施方案中多肽二聚体蛋白在食物过敏引起的疾病
模型中的效力。
图17显示了对于食物过敏诱导,IgETRAP、长双歧杆菌以及联合疗法的实验时间表。
i.p.,腹膜内;i.g.,灌胃。
图18显示了IgETRAP、长双歧杆菌和联合疗法抑制过敏反应性腹泻症状的效力。n=
每组16-18只小鼠,OVA vs OVA IgETRAP:*P<.05,OVA vs OVA 长双歧杆菌 IgETRAP,以及OVA
vs PBS:***P<.0001。
图19A显示了鉴定长双歧杆菌改善IgETRAP的治疗效果的实验计划。具体地,显示了
对于于食物过敏诱导以及IgETRAP和长双歧杆菌的单次或联合施用的实验计划。i.p.,腹膜
内;i.g.,灌胃。
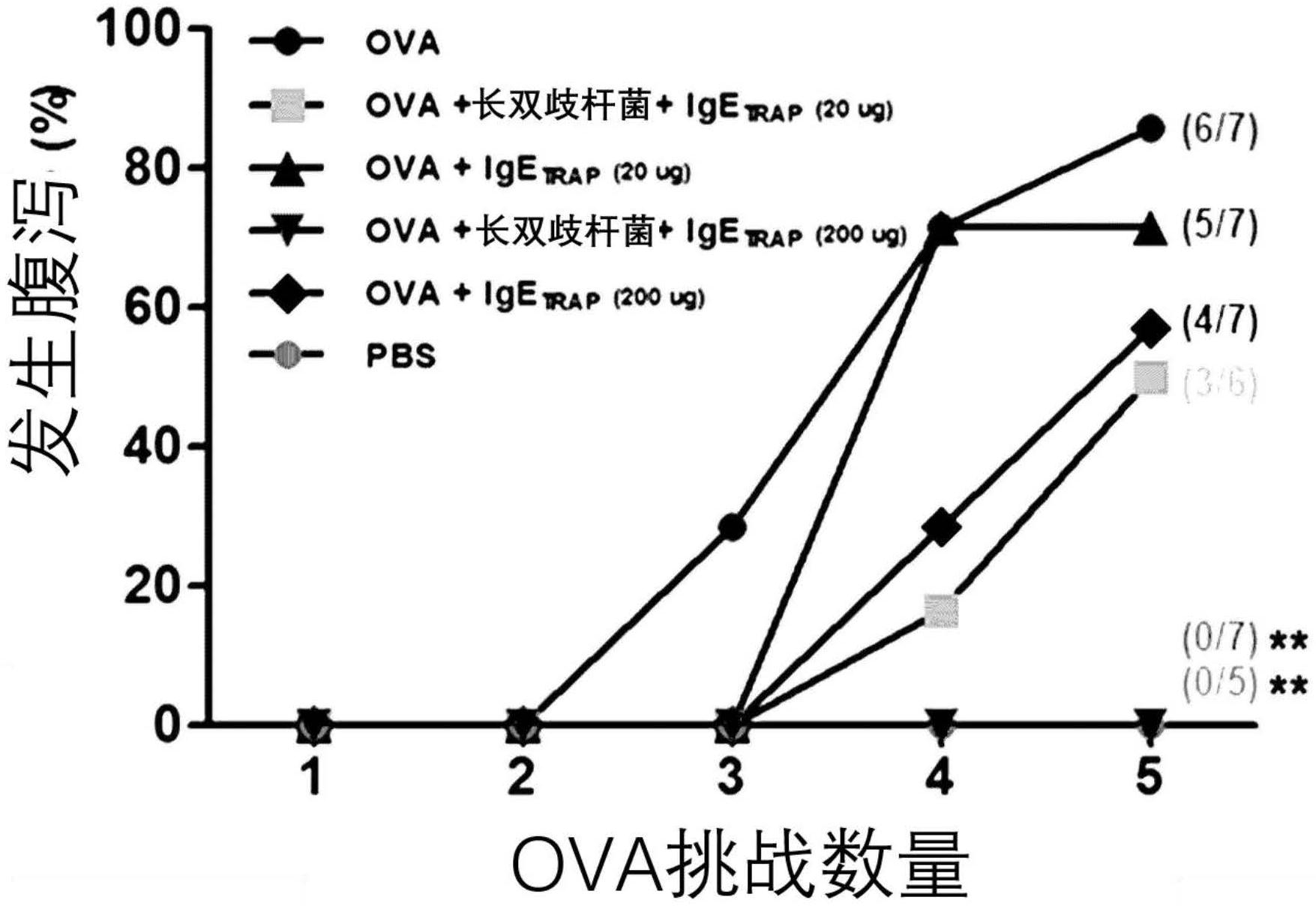
图19B显示在食物过敏引起的疾病模型中,确定联合施用益生菌和具有与IgE的结
合能力的多肽二聚体蛋白(IgETRAP)的效果取决于剂量的增加。图中显示了IgETRAP、长双歧杆
菌及其组合对抑制食物过敏性腹泻的影响。每组n=14只小鼠,OVA vs OVA 长双歧杆菌
IgETRAP(20μg),OVA vs OVA 长双歧杆菌 IgETRAP(200μg),OVA vs PBS:**P<.001。
6
CN 111587118 A 说 明 书 4/25 页
图20显示了在食物过敏诱发的疾病模型中,施用IgETRAP、长双歧杆菌及其组合时,
通过ELISA分析从各个实验组获得的血清中肥大细胞蛋白酶-1(MCPT-1)水平获得的结果。
图21显示了在食物过敏引起的疾病模型中,施用IgETRAP、长双歧杆菌及其组合时,
通过ELISA检测从各个实验组获得的血清中的总IgE(游离IgE和IgE-IgETRAP复合物)的水平
获得的结果。n=每组16-18只小鼠,OVA vs OVA IgETRAP,OVA vs OVA 长双歧杆菌 IgETRAP
以及OVA vs PBS:***P<.0001.
图22显示了在食物过敏引起的疾病模型中,在施用IgETRAP、长双歧杆菌及其组合
时,通过ELISA检测从各个实验组获得的血清中游离IgE的水平所获得的结果。n=每组16-
18只小鼠,OVA vs OVA IgETRAP,OVA vs OVA 长双歧杆菌 IgETRAP以及OVA vs PBS:***P<
.0001。
图23显示了通过在食物过敏引起的疾病模型中施用IgETRAP、长双歧杆菌及其组合
时,在各个实验组中鉴定对肥大细胞增殖和杯状细胞增殖的抑制作用而获得的结果。图中
显示了通过对各个实验组的空肠的代表性石蜡切片中的肥大细胞(红色)染色获得的结果
(放大400倍)。放大的空肠清楚地显示出肥大细胞(红色)。
图24显示了通过将图23中的肥大细胞放大400倍并鉴定出肥大细胞而获得的结
果。n=每组10-12只小鼠,OVA vs长双歧杆菌以及OVA vs IgETRAP:**P<.001,OVA vs OVA
长双歧杆菌 IgETRAP以及OVA vs PBS:***P<.0001。
图25显示了在食物过敏引起的疾病模型中,在施用IgETRAP、长双歧杆菌及其组合
时,通过鉴定在各个实验组中对肥大细胞增殖和杯状细胞增殖的抑制作用而获得的结果。
图中显示了通过对各个实验组的空肠的代表性石蜡切片中的杯状细胞染色并进行鉴定而
获得的结果(紫色,放大倍数400x)。
图26显示了通过从图25中的绒毛-隐窝单元(villus-crypt units,VCU)中随机选
择的杯状细胞并计数10个VCU而获得的结果。n=每组5-6只小鼠,OVA vs长双歧杆菌以及
OVA vs IgETRAP:*P<.05,OVA vs OVA 长双歧杆菌 IgETRAP以及OVA vs PBS:***P<.0001.
图27为由长双歧杆菌和IgETRAP的联合疗法引起的食物过敏抑制机理的示意图。摄
入的食物过敏原可通过将IgE与效应细胞上的高亲和力IgE Fc受体(FcεRI)结合而诱导效
应细胞(肥大细胞和嗜碱性粒细胞)的活化。活化的效应细胞释放调节剂,从而引起速发型
超敏反应。长双歧杆菌通过分泌胞外囊泡(EV)诱导肥大细胞凋亡,从而减少肥大细胞的数
量。同时,IgETRAP可以阻断IgE与效应细胞上的FcεRI结合,从而抑制效应细胞的活化和增
殖。长双歧杆菌和IgETRAP的联合施用使有效减轻食物过敏症状和杯状细胞的增生成为可
能。
图28为通过鉴定施用了长双歧杆菌(B.longum)和IgETRAP后肠组织中IL-33表达变
化获得的图。施用长双歧杆菌和IgETRAP可降低食物过敏模型小鼠空肠中IL-33mRNA的表达。
n=每组16-18只小鼠,OVA vs OVA 长双歧杆菌 IgETRAP:*P<.05。
图29为通过鉴定腹膜内注射IgETRAP和干酪乳杆菌(L.casei)后的腹泻频率获得的
图。每组n=7-10只小鼠。
图30为通过鉴定腹膜内注射IgETRAP和乳酸乳球菌(Lc.lactis)后的腹泻频率获得
的图。每组n=5只小鼠。
图31为通过鉴定腹膜内注射IgETRAP和嗜热链球菌(S.thermophilus)后的腹泻频
7
CN 111587118 A 说 明 书 5/25 页
率获得的图。每组n=6-10只小鼠。
图32显示了通过鉴定腹膜内注射IgETRAP和鼠李糖乳杆菌(L.rhamnosus)后的腹泻
频率获得的图。每组n=5-10只小鼠。
图33为通过鉴定腹膜内注射IgETRAP和罗伊氏乳杆菌(L.reuteri)后的腹泻频率获
得的图。每组n=5-10只小鼠。
图34为通过鉴定腹膜内注射IgETRAP和发酵乳杆菌(L.fermentum)后的腹泻频率获
得的图。每组n=7-10只小鼠。
图35为通过将IgETRAP口服施用给正常小鼠并且鉴定小鼠血清中吸附的IgETRAP获得
的图。
发明详述
在本发明的一个方面,提供了一种组合物,其包含作为活性成分的益生菌和具有
与IgE结合能力的多肽。
如本文所用,术语“益生菌”统指在以适当量摄入的情况下对人体有益的微生物,
表明其为有益于人体的细菌。益生菌可以是乳酸菌或双歧杆菌。乳酸菌统指发酵糖以产生
乳酸的细菌。大多数肠道有益细菌被分类为乳酸菌,乳酸菌可以降解糖,其中糖的50%或更
多被产生为乳酸。
乳酸菌可以是选自由乳杆菌(Lactobacillus)、乳球菌(Lactococcus)、肠球菌
(Enterococcus)和链球菌(Streptococcus)组成的组中的任一种。具体地,乳杆菌可以是选
自由嗜酸乳杆菌(L.acidophilus)、干酪乳杆菌(L.casei)、加氏乳杆菌(L.gasseri)、德氏
乳杆菌保加利亚亚种(L.delbrueckii ssp.bulgaricus)、瑞士乳杆菌(L.helveticus)、发
酵乳杆菌(L.fermentum)、副干酪乳杆菌(L.paracasei)、植物乳杆菌(L.plantarum)、罗伊
氏乳杆菌(L.reuteri)、鼠李糖乳杆菌(L.rhamnosus)、戊糖乳杆菌(L.pentosus)和唾液乳
杆菌(L .sa liva rius)组成的组中的任何一种。另外,乳球菌可以是乳酸乳球菌
(Lc .la c t i s) ,链球菌可以是嗜热链球菌(S .t h e m o p h i l u s)。另外,双歧杆菌
(Bifidobacterium)可以是选自由两歧双歧杆菌(B.bifidum)、短双歧杆菌(B.breve)、长双
歧杆菌(B.longum)和动物双歧杆菌乳酸菌亚种(B.animalis ssp.lactis)组成的组中的任
何一种。
优选地,所述益生菌可以是干酪乳杆菌(Lactobacillus casei)或长双歧杆菌
(Bifidobacterium longum)。特别地,长双歧杆菌的登录号可为KACC 91563(KR10-
1778734B1)。特别地,KACC 91563菌株靶向肥大细胞(过敏反应中的重要细胞),因此可以用
作治疗过敏反应的乳酸菌。通常,益生菌可以活细菌的形式使用,所述活细菌可以冻干的形
式使用。另外,益生菌可以以死细菌的形式使用。
如本文所用,术语“具有与IgE结合能力的多肽”是指能够与IgE结合的多肽。如本
发明所用,术语“IgE”是指称为免疫球蛋白E的抗体蛋白。IgE对肥大细胞、嗜血嗜碱性粒细
胞等具有亲和力。另外,IgE抗体和与其对应的抗原(过敏原)之间的反应会引起炎症反应。
另外,已知IgE是引起过敏性反应的抗体。
具体地,具有与IgE结合能力的多肽可以是重组蛋白中的任何一种,包括抗IgE抗
体、IgE Fc受体、IgE Fc受体的α亚基的胞外域、IgE Fc受体的α亚基胞外域片段的片段,以
及IgE Fc受体的α亚基的胞外结构域或其片段。
8
CN 111587118 A 说 明 书 6/25 页
在此,抗IgE抗体是指能够将IgE识别为抗原并结合IgE的抗体。在此,抗IgE抗体的
片段可以是选自由Fab、scFv、F(ab)2和Fv组成的组中的任何一种,只要该片段可以结合IgE
即可。抗体片段是指除可结晶区域(Fc区域)以外的抗原结合结构域,所述可结晶区域(Fc区
域)执行功能(效应子功能)以将由于与抗原结合而引起的刺激转移至细胞或补体。抗IgE抗
体的一个实施方案可以是奥马珠单抗。
如本发明所用,术语“IgE Fc受体”也称为Fcε受体,并与IgE的Fc部分结合。该受体
有两种类型。对IgE Fc具有高亲和力的受体称为Fcε受体I(Fc RI)。对IgE Fc具有低亲和力
的受体称为Fcε受体II(FcεRII)。FcεRI在肥大细胞和嗜碱性粒细胞中表达。在与FcεRI结合
的IgE抗体被多价抗原交联的情况下,肥大细胞或嗜碱性粒细胞中发生脱粒,从而释放出包
括组胺在内的各种化学递质。这种释放导致立即发生的过敏反应。
FcεRI是由二硫键连接的一条α链、一条β链和两条γ链组成的膜蛋白。在这些链
中,与IgE结合的部分是α链(FcεRIα)。FcεRIα的大小约为60kDa,且是由存在于细胞膜内的
疏水域和存在于细胞膜外的亲水域组成。特别地,IgE结合至α链的胞外域。
具体地,IgE Fc受体的α亚基可以具有如NP_001992.1中所示的氨基酸序列。此外,
IgE Fc受体的α亚基的胞外域(FcεRIa-ECD)可以具有如SEQ ID NO:1所示的氨基酸序列。在
本说明书中,IgE Fc受体的α亚基的胞外域可以是IgE Fc受体的α亚基的胞外域的片段或变
体,只要该片段或变体能够结合IgE即可。
可以通过在野生型FcεRIa-ECD(胞外域)中取代、缺失或插入一种或多种蛋白质的
方法来制备得到变体,只要该方法不改变FcεRI的α链的功能即可。此类的多种蛋白质或肽
可以与SEQ ID NO:1的氨基酸序列具有90%、91%、92%、93%、94%、95%、96%、97%、
98%、99%或更高的同源性。此外,如SEQ ID NO:1所示的FcεRIa-ECD可以由具有如SEQ ID
NO:5所示序列的多核苷酸编码。
因此,可以将IgE Fc受体的α亚基的胞外域本身或IgE Fc受体的α亚基的胞外域的
片段用作具有与IgE的结合能力的多肽。胞外域的片段的一个实施方案可以是其中IgE Fc
受体的α亚基的胞外域的N-末端的一些氨基酸被缺失的形式。在一个实施方案中,胞外域的
片段可以是其中N端的1至30个氨基酸被缺失的片段。另外,胞外域的片段可以是其中N末端
的5至25个氨基酸被缺失的片段。另外,胞外域的片段可以是N末端的1、2、3、4、5、6、7、8、9或
10个氨基酸被缺失的形式。另外,胞外域的片段的一个实施方案可以是其中IgE Fc受体的α
亚基的胞外域的C-末端的一些氨基酸被缺失的形式。在一个实施方案中,胞外域的片段可
以是其中C末端的1至30个氨基酸被缺失的片段。另外,胞外域的片段可以是其中C末端的5
至25个氨基酸缺失的片段。另外,胞外域的片段可以是缺失C末端的1、2、3、4、5、6、7、8、9或
10个氨基酸的形式。另外,胞外域的片段的一个实施方案可以是其中IgE Fc受体的α亚基的
胞外域的N-末端和C-末端的一些氨基酸被缺失的形式。在一个实施方案中,胞外域的片段
可以N末端和C末端分别有1、2、3、4、5、6、7、8、9或10个氨基酸被缺失的形式。
然而,野生型IgE受体的α亚基的胞外域或其片段在体内的持久性差。为了改善这
一点,可以通过各种方法修饰IgE受体的α亚基的胞外域或其片段。作为修饰方法的一个实
施方案,可以将聚乙二醇(PEG)结合到上面。作为修饰方法的另一个实施方案,可以将免疫
球蛋白的Fc区结合到上面。在此,除了天然形式的免疫球蛋白Fc之外,还可以使用经修饰的
Fc区。
9
CN 111587118 A 说 明 书 7/25 页
另外,如本发明所用,术语“经修饰的Fc区”是指抗体的Fc部分的其中一部分已被
修饰的区域。其中,术语“Fc区”是指包含免疫球蛋白的重链恒定区2(CH2)和重链恒定区3
(CH3)、并且不包含免疫球蛋白的重链和轻链可变区以及轻链恒定区1(CH1)的蛋白质。特别
地,经修饰的Fc区是指通过在Fc区中进行一些氨基酸取代或通过组合不同类型的Fc区而获
得的区域。具体地,经修饰的Fc区可以具有如SEQ ID NO:2所示的氨基酸序列。此外,如SEQ
ID NO:2所示的经修饰的Fc区可以由具有如SEQ ID NO:6所示序列的多核苷酸编码。
另外,本发明中的经修饰的Fc区可以是具有天然形式的糖链、相对于天然形式有
增加的糖链或相对于天然形式有较少的糖链的形式,或者可以是被去除糖链的形式。可以
通过例如化学方法、酶促方法和使用微生物的基因工程方法等常规方法来修饰免疫球蛋白
Fc的糖链。
其中,本发明中的“经修饰的Fc区”可以是由于没有与FcγR或C1q的结合位点而缺
乏抗体依赖性细胞毒性(ADCC)和补体依赖性细胞毒性(CDC)功能的区域。
另外,FcεRIα-ECD或其片段可以通过连接子与野生型Fc或经修饰的Fc区连接。所
述连接子可以由20至60个连续氨基酸、25至50个连续氨基酸或30至40个氨基酸组成。如下
所示,在一个实施方案中,所述连接子可以由30或49个氨基酸组成。同样,所述连接子可以
包含至少一种半胱氨酸。具体地,所述连接子可以包含一个、两个或三个半胱氨酸。优选地,
所述连接子包含一个半胱氨酸。在一个实施方案中,所述连接子可以是衍生自IgD抗体的铰
链区。另外,所述连接子可以是通过修饰IgD抗体的铰链区获得的铰链变体。所述铰链变体
可以通过修饰IgD抗体的铰链序列中的一些以最小化在蛋白质生产过程中截短形式的产生
而获得。
在一个实施方案中,所述铰链可以包含以下序列:
Arg Asn Thr Gly Arg Gly Gly Glu Glu Lys Lys Xaa1 Xaa2 Lys Glu Lys Glu
Glu Gln Glu Glu Arg Glu Thr Lys Thr Pro Glu Cys Pro(SEQ ID NO:17),其中Xaa1可
以是Lys或Gly,Xaa2可以是Glu、Gly或Ser。具体地,所述连接子可具有如SEQ ID NO:3和SEQ
ID NO:19所示的氨基酸序列,从而使蛋白质在生产过程中产生的截短形式最小化。
在另一个实施方案中,所述铰链可以包含以下序列:
Ala Gln Pro Gln Ala Glu Gly Ser Leu Ala Lys Ala Thr Thr Ala Pro Ala
Thr Thr Arg Asn Thr Gly Arg Gly Gly Glu Glu Lys Lys Xaa3 Xaa4 Lys Glu Lys Glu
Glu Gln Glu Glu Arg Glu Thr Lys Thr Pro Glu Cys Pro(SEQ ID NO:18),其中Xaa3可
以是Lys或Gly,Xaa4可以是Glu、Gly或Ser。具体地,所述连接子可具有如SEQ ID NO:4所示
的氨基酸序列,从而使蛋白质在生产过程中最小化截短形式的产生。
特别地,在具有如SEQ ID NO:4所示氨基酸序列的连接子中,至少一个Thr可以被
糖基化。具体而言,在如SEQ ID NO:18所示的氨基酸中,第13、14、18和19个Thr可以被糖基
化。优选地,所有四个氨基酸都可以被糖基化。其中,所述的糖基化可以是O-糖基化。
作为本发明的一个实施方案中与IgE具有结合能力的多肽,IgETRAP是指FcεRIα胞
外域和IgD/IgG4杂合Fc结构域的Fc融合蛋白。IgE Fc受体FcεR由α链、β链和两条相同的二
硫键连接的γ链组成。FcεRIβ和FcεRIγ没有胞外域。然而,FcεRI3具有两个细胞外免疫球
蛋白相关结构域,并参与IgE结合。因此,为了产生更安全和有效的IgE抑制剂,将人FcεRI胞
外域与人IgD/IgG4杂合Fc结构域连接(图1和2)以产生IgETRAP。与奥马珠单抗不同,IgETRAP不
10
CN 111587118 A 说 明 书 8/25 页
与IgG受体结合,并可能降低IgG介导的过敏反应的风险(图9-13)。此外,IgETRAP对IgE的亲
和力比奥马珠单抗高69倍。因此,作为食物过敏的治疗剂,IgETRAP比奥马珠单抗更安全有
效。
具有与IgE结合能力的多肽用于阻断效应细胞上的FcεRI3与IgE之间的结合。人
IgD/IgG4杂合Fc包含IgD的上部CH2结构域以及IgG4的最后CH2和CH3结构域,它们不具有Fc
γR或C1q的结合位点(图1)。但是,该杂合Fc可以具有新生儿Fc受体的结合位点(图1)。另
外,同二聚体形式的IgETRAP的理论分子量为约97.6kDa。然而,由于糖基化,其实际分子量为
约150kDa(图6)。
与常规使用的抗IgE抗体相比,本发明实施方案的具有与IgE结合能力的多肽二聚
体蛋白质不仅在体内具有优异的安全性和持久性,而且由于具有结合力而与IgE非常牢固
地结合。与常规使用的抗IgE抗体奥马珠单抗相比,其对IgE的抗性约高70倍,从而可以延长
给药周期。另外,本发明的多肽二聚体蛋白是通过应用经修饰的Fc获得的物质,所述经修饰
的Fc仅具有IgE作为单一靶标并且不与Fcγ受体结合,因此缺乏抗体依赖性细胞毒性
(ADCC)和补体依赖性细胞毒性(CDC)功能。因此,与包含IgG1 Fc区域的常规抗IgE抗体不
同,该多肽二聚体蛋白不与Fcγ受体结合,因此可以抑制由于与肥大细胞表面上的Fcγ受
体结合而引起的介体的释放。因此,本发明的具有与IgE的结合能力的多肽可以使严重的副
作用如过敏反应的发生最小化,所述副作用可以由肥大细胞上的IgG1和Fcγ受体III之间
的结合引起。因此,根据本发明的多肽二聚体蛋白质可以用作新的药物组合物,其可以代替
含有常规抗IgE抗体的治疗剂。
另外,本发明提供的具有与IgE结合能力的多肽的一个实施方案可以是单体形式。
特别地,在使用的连接子中不存在半胱氨酸的情况下,该多肽可以呈单体形式。
另外,本发明提供的具有与IgE结合能力的多肽的一个实施方案可以是多肽二聚
体。在此,如上所述,多肽二聚体可以是两个单体彼此结合的形式,并且每个单体通过IgE
Fc受体的α亚基的胞外域与经修饰的Fc区结合而得。多肽二聚体可以是相同的两个单体通
过位于连接子位点的半胱氨酸彼此结合的形式。此外,多肽二聚体可以是两种不同单体彼
此结合的形式。例如,在两种单体彼此不同的情况下,多肽二聚体可以是其中一种单体包含
IgE Fc受体的α亚基的胞外域,而另一种单体包含IgE Fc受体的α亚基的胞外域的片段的形
式。其中,一个实施方案中单体可以具有如SEQ ID NO:20、SEQ ID NO:21或SEQ ID NO:22所
示的氨基酸序列。
本发明的另一方面,提供了一种用于治疗或预防过敏性疾病的药物组合物,该组
合物包含益生菌和具有与IgE结合能力的多肽作为活性成分。
益生菌和具有与IgE结合能力的多肽如上所述。可以适当地确定组合物中益生菌
和具有与IgE结合能力的多肽的混合量。在一个实施方案中,组合物中益生菌的含量可以为
1×105cfu至1×1012cfu。可选择地,组合物中的益生菌的含量可以为1×106cfu至1×
1011cfu、1×107cfu至1×1010cfu或1×109cfu至5×109cfu。另外,具有与IgE结合能力的多
肽的量可以为但不限于0.1μg至5mg、0.5μg至1mg、1μg至500μg、10μg至400μg或200μg至300μ
g。另外,可以适当地改变组合物中益生菌和具有与IgE结合能力的多肽的混合比例。
在本说明书中,“过敏性疾病”是指由例如肥大细胞脱粒等肥大细胞活化介导的过
敏反应引起的病理症状。此类的过敏性疾病包括食物过敏、特应性皮炎、哮喘、过敏性鼻炎、
11
CN 111587118 A 说 明 书 9/25 页
过敏性结膜炎、过敏性皮炎、过敏性接触性皮炎、过敏性休克、荨麻疹、瘙痒、昆虫过敏、慢性
特发性荨麻疹、药物过敏等。特别是,过敏性疾病可以是IgE介导的。
在本发明的一个实施方案中,具有IgE结合能力的多肽,其包含FcεRI1胞外域,通
过与IgE结合而阻断IgE与效应细胞上的FcεRI的结合,因此可以称为IgETRAP。此外,已确认
长双歧杆菌可改善IgETRAP的治疗效果并显著降低治疗所需的IgETRAP剂量。
在本发明的用于治疗或预防过敏性疾病的组合物中,根据其用途、制剂、掺合目的
等可以包含任何量(有效量)的活性成分,只要该活性成分可以表现出抗过敏活性即可。所
述活性成分的常规的有效量可确定在组合物总重量的0.001%-20.0%的范围内。其中,“有
效量”是指能够引起抗过敏作用的活性成分的量。这种有效量可以在本领域技术人员的普
通技术范围内通过实验确定。
其中,所述药物组合物可以进一步包含药学上可接受的载体。药学上可接受的载
体可以是使用任何载体,只要该载体是适合递送给患者的无毒物质即可。可以包含蒸馏水、
酒精、脂肪、蜡和惰性固体作为载体。药物组合物中也可以包含药学上可接受的佐剂(缓冲
剂和分散剂)。特别地,可以使用任何药学上可接受的制剂,只要益生菌和具有与IgE结合能
力的多肽可以在制剂中保持稳定性即可。
具体地,本发明的药物组合物除了包含活性成分之外,还包含药学上可接受的载
体,并且可根据本领域已知的常规方法基于药物的给药途径制成口服或肠胃外制剂。其中,
术语“药学上可接受的”是指其毒性不超过所施用(处方)的受试者所能容纳的程度,不抑制
活性成分的活性。
在将本发明的药物组合物制成口服制剂的情况下,可以将药物组合物根据现有技
术中已知的方法制成粉剂、颗粒剂、片剂、丸剂、糖衣片、胶囊剂、液体制剂、凝胶剂、糖浆剂、
混悬剂、晶片,以及合适的载体。其中,合适的药学上可接受的载体的实例可以包括糖例如
乳糖、葡萄糖、蔗糖、右旋糖、山梨糖醇、甘露醇和木糖醇,淀粉例如玉米淀粉、马铃薯淀粉和
小麦淀粉,纤维素例如纤维素、甲基纤维素、乙基纤维素、羧甲基纤维素钠以及羟丙基甲基
纤维素、聚乙烯吡咯烷酮、水、羟基苯甲酸甲酯(methylhydroxybenzoate)、羟基苯甲酸丙酯
(propylhydroxybenzoate)、硬脂酸镁、矿物油、麦芽、明胶,滑石粉、多元醇、植物油等。在制
成制剂的情况下,可以根据需要添加稀释剂和/或赋形剂如填充剂、增量剂、粘合剂、湿润
剂、崩解剂和表面活性剂来进行制备。
在将本发明的药物组合物制成肠胃外制剂的情况下,可以根据本领域已知的方法
将所述药物组合物与合适的载体一起制成注射剂、透皮药物、鼻吸入剂和栓剂形式的制剂。
在制备成注射剂的情况下,可以将无菌水、乙醇、如甘油和丙二醇等多元醇或其混合物作为
合适的载体。对于载体而言,可以优选使用等渗溶液如林格氏溶液(Ringer's solution)、
含有三乙醇胺的磷酸盐缓冲盐水(PBS)、注射用无菌水和5%右旋糖等。
药物组合物的制备是本领域已知的,具体地,可以参考雷明顿药物科学
(Remington's Pharmaceutical Sciences)(第19版,1995)等。该文献应当被认为是本说明
书的一部分。
根据患者的状况、体重、性别、年龄、疾病严重程度或给药途径,本发明的药物组合
物的优选的日剂量范围为0.01μg/kg-10g/kg,并且优选为0.01mg/kg-1g/kg。每天可进行一
次或多次给药。此类的剂量决不应被解释为对本发明范围的限制。
12
CN 111587118 A 说 明 书 10/25 页
可以施用(开处方)本发明组合物的受试者可以为哺乳动物和人,特别优选为人。
除了活性成分之外,本发明的用于抗过敏的组合物还可包含其安全性已被验证以及已知其
具有抗过敏活性的任何化合物或天然提取物,从而提高并增强其抗过敏活性。其中,药物组
合物可以进一步包含从长双歧杆菌KACC 91563(Bifidobacterium longum KACC 91563)分
离的细胞外内质网。
本发明的另一方面,提供了一种用于改善或减轻过敏症状的保健功能性食品组合
物,其包含含有益生菌和具有与IgE结合能力的多肽作为活性成分的组合物。其中,食品组
合物还可以包含从长双歧杆菌KACC 91563分离的细胞外内质网作为活性成分。
同时,本发明的食品组合物可以进一步包含在形态学上可接受的载体。另外,食物
组合物可以与另一种食物或食物成分一起使用,并且可以根据常规方法适当地使用。活性
成分的混合量可以根据其预期用途(预防、健康或治疗)适当地确定。
对食物的种类没有特别限制。食物的实例包括肉、香肠、面包、巧克力、糖果、点心、
零食、包括冰淇淋的乳制品、各种汤、饮料、茶、饮料、酒精饮料和维生素复合物。包括所有常
规意义上的功能性保健食品。可以添加上述物质的食物包含通常在制造期间添加的成分,
并且成分的实例包括蛋白质、碳水化合物、脂肪、营养物、调味剂和调味料。上述碳水化合物
是典型的糖,例如,单糖,如葡萄糖和果糖;二糖,如麦芽糖和蔗糖;和多糖,如糊精和环糊
精;以及糖醇如木糖醇、山梨糖醇和赤藓糖醇。作为调味剂,可以使用天然甜味剂例如索马
甜和甜叶菊提取物,合成调味剂例如糖精和阿斯巴甜等。
例如,在将本发明的食品组合物制成饮料的情况下,除本发明的组合物外,还可以
进一步包含柠檬酸、液态果糖、糖、葡萄糖、乙酸、苹果酸、果汁、提取物等。
除如上所述外,本发明的组合物还可包含各种营养素、维生素、电解质、调味剂、着
色剂、果胶及其盐、藻酸及其盐、有机酸、保护性胶体增稠剂、pH调节剂、稳定剂、防腐剂、甘
油、酒精、碳酸饮料中使用的碳酸化剂等。另外,本发明的组合物可以包含用于生产果汁饮
料和蔬菜饮料的果肉。这些成分可以单独使用或混合使用。
此外,本发明的食品组合物可以落入合法的任何产品类别或功能分类中,只要该
食品组合物在制造和分发时符合执行法规即可。例如,所述的食品组合物可以是《健康功能
食品法(Health Functional Foods Act)》中所述的健康功能食品,或可以是《食品卫生法
的食品法规(Food Code of Food Sanitation Act)》(食品标准和规格,由食品药品监督管
理局颁布)中所述的属于糖果、豆类、茶、饮料、特殊用途食品等的各种食品类型。关于可以
包含在本发明的食品组合物中的其他食品添加剂,可以参考食品卫生法(Food Sanitation
Act)的食品法规(Food Code)或食品添加剂法规(Food Additive Code)。
在本发明的又一个方面,提供了一种用于治疗或预防过敏性疾病的试剂盒,其包
含含有益生菌的第一组合物以及含有具备与IgE结合能力的多肽第二组合物。其中,第二组
合物可以是用于皮下或静脉内施用的组合物。
在本发明的又一个方面,提供了一种用于治疗或预防过敏性疾病的方法,该方法
包括施用益生菌和施用具有与IgE结合能力的多肽的步骤。
所述益生菌如上所述,并且可以口服施用。其中,具有IgE结合能力的多肽可以口
服给药,也可以非肠道给药。在此,肠胃外给药可以通过例如皮下给药、静脉内给药、粘膜给
药等方法进行。
13
CN 111587118 A 说 明 书 11/25 页
在小鼠食物过敏模型中,已经显示出IgETRAP不仅降低了游离IgE水平,而且减少了
肥大细胞的数目,从而减轻了食物过敏症状(图21-26)。预计由IgETRAP引起的肥大细胞数量
减少是由于IgE通过增加肥大细胞的存活率而增加了肥大细胞的数量。此外,单独施用
IgETRAP和长双歧杆菌显著抑制了小肠杯状细胞的过度增殖,并且在联合施用时被进一步抑
制(图23-26)。由于已知诸如IL-13的Th2细胞因子诱导杯状细胞过度增殖,因此预期
IgETRAP,长双歧杆菌及其组合缓和了小肠中Th2细胞因子的环境。为此,IgETRAP和长双歧杆菌
显示出通过活化第二组先天性淋巴样细胞(ILC2s)降低小肠中促进IL-13分泌的IL-33mRNA
表达的趋势;并且其组合以更有效的方式显著降低IL-33的表达(图28)。另外,IL-33不仅分
泌在IgE活化的肥大细胞中,而且还参与促进肥大细胞的脱粒。因此,IL-33与食物过敏的严
重程度密切相关。这表明IgETRAP和长双歧杆菌可以通过多种机制改善食物过敏症状。
目前,据报道长双歧杆菌诱导肥大细胞凋亡并改善食物过敏症状,这与本发明人
的结果一致。但是,每天服用长双歧杆菌治疗食物过敏的效果不如单独服用IgETRAP。然而,
长双歧杆菌显著改善了IgETRAP的治疗效果(图18),与长双歧杆菌结合使用的IgETRAP的治疗
效果类似于以10倍高剂量单独施用IgETRAP所获得的治疗效果(图19B)。另外,据报道,一些
肠细菌可以通过增加Treg细胞或降低IgE和Th2细胞因子的水平来改善过敏性疾病。因此,
预期除了长双歧杆菌之外的其他益生菌能够改善IgETRAP的治疗效果。实际上,已经确定在
组合施用各种类型的益生菌和IgETRAP时表现出提高的治疗效果(图29至34)。
在本发明的又一方面,提供了一种用于治疗或预防过敏性疾病的方法,其包括对
个体施用具有与IgE结合能力的多肽和益生菌的组合的步骤。该个体可以是哺乳动物,优选
是人类。其中,给药可以口服或肠胃外进行。其中,可以将对IgE和益生菌具有结合能力的多
肽制成适合口服的制剂。另外,肠胃外给药可以通过皮下给药、静脉内给药、粘膜给药和肌
肉给药等方法进行。
实施方式
在下文中,将参考以下实施例更详细地描述本发明。然而,以下实施例仅旨在解释
本发明,并且本发明的范围不限于此。
材料和方法
IgETRAP细胞系的构建及其纯化
IgETRAP的核苷酸序列是通过将FcεRIα胞外域的C末端(第26-205位)与IgD/IgG4
杂合Fc结构域的N末端(IgD,第133-170位;IgG4,第121-327位)连接构建而成的。该蛋白在
二氢叶酸还原酶缺陷的中国仓鼠卵巢DG44细胞中表达。使用HiTrap rProtein A FF色谱柱
(GE Healthcare)纯化IgETRAP,并在还原和非还原条件下通过SDS-PAGE鉴定其纯度。
3D结构建模
使用WinCoot设计,并根据蛋白质数据库中FcεRIα(PDB登录号1F6A)和IgD/IgG4Fc
(PDB登录号1ADQ)的信息,使用PyMOL软件进行构建IgETRAP的结构模型。
表面等离子共振(SPR)测定
使用ProteOn XPR36(Bio-Rad)仪器进行SPR测定。使用动力学分析测定奥马珠单
抗和IgETRAP与人IgE的结合程度(Calbiochem)。850个反应单位(response unit,RU)的置于
醋酸盐缓冲液(pH 5 .5)中的奥马珠单抗和500个RU置于的醋酸盐缓冲液(pH 4 .0)中的
IgETRAP固定在ProteOnTMGLC传感器芯片(Bio-Rad)上。含有Tween-20的PBS作为运行缓冲液,
14
CN 111587118 A 说 明 书 12/25 页
流速设置为30μl/min。使用ProteOn Manager软件(Bio-Rad)分析每个数据集的图表。
生物膜层干涉法(BLI)测定
使用Octet RED384系统(Pall ForteBio,CA,USA)测定IgETRAP和奥马珠单抗与IgG
受体的结合程度。在300mM醋酸盐缓冲液(pH 5)中稀释的FcγRI、FcγRIIA、FcγRIIB、Fcγ
RIIIA和FcγRIIIB重组蛋白(R&D Systems Inc.,5μg/ml)被固定在已用400mM EDC和10mM
磺基-NHS组合活化的第二代氨基偶联传感器(Amine Reactive 2Generation,AR2G)上。然
后,分别在300秒内测量与不同浓度的IgETRAP和奥马珠单抗的结合和解离。在此,使用的动
力学缓冲液是含有0.1%Tween-20和1%牛血清的PBS,所有实验均在30℃下用样品平板摇
床以1,000rpm的速率进行。
β-己糖胺酶释放测定
在包含10%热灭活的FBS、10ng/mL小鼠IL-3(PeproTech,Inc.)和50ng/mL小鼠SCF
(PeproTech,公司)的RPMI中37℃培养骨髓来源的肥大细胞(BMMC)。在分析之前,将1μg/mL
的抗二硝基苯基IgE(Sigma-Aldrich)和不同浓度的IgETRAP在室温下孵育30分钟。将骨髓来
源的肥大细胞与抗二硝基苯基IgE(Sigma-Aldrich)和IgETRAP的混合物中于37℃孵育30分
钟,然后向其中加入0.1μg/ml的抗二硝基苯基IgE。将所得产物再次在37℃下孵育30分钟。
收集培养上清液,并与3mM的对硝基苯基-N-乙酰基-β-D-氨基葡萄糖苷在37℃孵育20分钟。
加入0.1M碳酸钠缓冲液(pH 10)以终止反应,并测量在405nm的吸光度。通过与使用0.1%
Triton X-100溶解的BMMC的总细胞内含量进行比较,计算释放的β-己糖胺酶的比率。
食物过敏诱导和长双歧杆菌(B.longum)的施用
在第0天和第14天,将50μg的OVA(V级;Sigma-Aldrich)和1mg的硫酸铝钾佐剂
(Sigma-Aldrich)腹膜内施用于小鼠。14天后,每隔2天对小鼠口服施用50mg的OVA(III级;
Sigma-Aldrich),共5次。在口服OVA之前,将小鼠禁食约4-5小时。通过在OVA接种后对小鼠
长达1小时的监控来评估腹泻的发生。将长双歧杆菌(B.longum)冻干并以3×109cfu/g的比
例与小鼠粉末饲料混合。允许小鼠随意食用饲料。为了保持新鲜度,每2-3天更换一次与长
双歧杆菌(B.longum)混合的小鼠饲料。
组织学
将小肠部分的空肠用4%多聚甲醛固定并包埋在石蜡中以形成块。然后,制作石蜡
切片的载玻片。将载玻片去石蜡化,用萘酚AS-D氯乙酸酯酶试剂盒(Sigma-Aldrich)对肥大
细胞进行染色。用高碘酸-希夫氏染色试剂盒(ScyTek Laboratories,Inc.)对玻片上的杯
状细胞进行染色。使用Pannoramic MIDI(3D HISTECH Ltd.)拍摄染色后的载玻片的图像。
ELISA
使用小鼠总IgE ELISA试剂盒(BioLegend)和MCPT-1ELISA试剂盒(Invitrogen)并
根据制造商的操作规程来检测小鼠血清中IgE和MCPT-1的总浓度。为了检测游离的IgE,将
1mg/mL的IgETRAP包被到平板上,然后使其在4℃反应过夜。其余的分析根据Mouse Total
IgE ELISA试剂盒中制造商的操作规程进行。
统计分析
使用GraphPad Prism 5软件(GraphPad Software Inc.)对所有数据进行统计分
析。使用对数秩(Mantel-Cox)测定的Kaplan-Meier生存曲线分析来计算腹泻的发生率。单
因素方差分析(One-way ANOVA)与Newman-Keuls多重比较测试用于确定测试中有意义的差
15
CN 111587118 A 说 明 书 13/25 页
异。
I.IgETRAP的制备和表征
实施例1.含有FcεRIα-ECD和经修饰的Fc区的多肽的制备
根据美国专利号7,867,491中公开的方法,制备IgE Fc受体的α亚基的胞外域(Fcε
RIα-ECD)的C末端经修饰的多肽。
首先,制备包含FcγRI的α链的胞外结构域(具有如SEQ ID NO:1所示的氨基酸序
列)和经修饰的免疫球蛋白Fc(如SEQ ID NO:2所示)的融合蛋白。具体地,为了表达分别通
过如SEQ ID NO:19所示的铰链、如SEQ ID NO:3所示的铰链、如SEQ ID NO:4所示的铰链连
接所得到的蛋白质(FcεRIαECD-Fc1)、蛋白质(FcεRIαECD-Fc2)和蛋白质(FcεR1αECD-Fc3),
将通过连接编码每种蛋白的基因获得的表达盒克隆到pAD15载体(Genexin,Inc.)中,以构
建FcεRIαECD-Fc蛋白表达载体。然后,将每种表达载体转导至CHO DG44细胞(来自美国哥伦
比亚大学的Chasin博士)。
其中,在转导至细胞系中时,同时转导通过将α-2,6-唾液酸转移酶的基因克隆至
pCI Hygro载体(Invitrogen)中而获得的表达载体,以分别制备能够表达添加了唾液酸的
FcεRIαECD-Fc2ST和FcεRIαECD-Fc3ST蛋白。
作为初步筛选程序,使用无5-羟色胺(HT)的10%dFBS培养基(Gibco,USA,30067-
334)、MEMα培养基(Gibco,12561,USA,目录号12561-049)和HT 培养基(USA,Gibco,11067-
030)进行HT筛选。然后,使用HT筛选出的克隆进行甲氨蝶呤(MTX)扩增,以使用二氢叶酸还
原酶(DHFR)系统扩大生产率。
在MTX扩增完成后,为了评估生产率,进行约1-5次传代培养以使细胞稳定。之后,
进行MTX扩增细胞的单位生产率评价。结果显示在下表1中。
表1
如表1所示,在2μM的甲氨蝶呤扩增后,FcεRIαECD-Fc3细胞系显示出16.9μg/106个
细胞的生产率。另一方面,在1μM的甲氨蝶呤扩增后,与2,6-唾液酸转移酶共转导的FcεRIα
ECD-Fc3细胞系(FcεRIαECD-Fc3ST)的生产率为17.5μg/106个细胞。此外,在0.5μM的甲氨蝶
呤扩增下,FcεRIαECD-Fc2细胞系显示出20.9μg/106个细胞的生产率。另外,在0.1μM的甲氨
蝶呤扩增下,与2,6-唾液酸转移酶共转导的FcεRIαECD-Fc2细胞系(FcεRIαECD-Fc2ST)显示
出25.1μg/106个细胞的生产率。即可以确认的是,在0.1μM的氨甲蝶呤扩增条件下,与2,6-
唾液酸转移酶共转染的FcεRIαECD-Fc2细胞系显示出最优异的生产率。
实施例2.FcεRIαECD融合蛋白的纯化及其纯度的鉴定
在以上实施例1中筛选的细胞系中,i)FcεRIαECD-Fc3,ii)FcεRIαECD-Fc3ST,和
16
CN 111587118 A 说 明 书 14/25 页
iii)FcεRIαECD-Fc2ST,以60ml规模通过分批培养方法进行培养。使用Protein-A亲和柱纯
化所得的培养物,然后对纯化的蛋白进行SDS-PAGE和尺寸排阻HPLC(SE-HPLC)以鉴定蛋白
的纯度。
如图3A和3B所示,通过SE-HPLC法纯化的所有蛋白质的纯度均为93%以上。另外,
SDS-PAGE分析的结果鉴定出,在非还原条件和还原条件下分别检测到具有约150kDa和约
75kDa大小的蛋白质(图3A,泳道1至6)。由此发现,结合Fc的FcεRIαECD形成二聚体。另外,在
SDS-PAGE结果中没有观察到诸如截短形式的杂质。特别地,即使在解冻/冷冻过程之后(图
3A,泳道7至8),也已经确定所有蛋白质具有93%或更高的纯度,并且没有杂质。
其中,在以下测试条件下进行Gel-IEF,以鉴定在引入唾液酸转移酶之后蛋白质中
唾液酸含量的程度。由此可知,由于唾液酸含量的增加,酸性蛋白质的含量有所增加。
表2
为了鉴定纯化产量的再现性,将FcεRIαECD-Fc2ST细胞系在1L烧瓶中以250mL的规
模分批培养,并使用Protein-A亲和柱纯化。随后,在Tris-甘氨酸SDS(TGS)缓冲液和200V的
条件下,将培养上清液和纯化的产物在4%至15%的TGXTM凝胶(Bio-Rad Laboratories,
Inc.)上运行30分钟,然后进行SDS PAGE分析。结果显示,不仅通过仅第一步纯化就纯化出
了纯度很高(98%以上)的蛋白质,并且即使在培养上清液中也表达了很高纯度的蛋白质。
这表明,可以将在相关细胞系中表达的FcεRIαECD-Fc蛋白开发为医疗产品,从而简化过程
开发步骤,因而医疗产品的开发成本极有可能显著下降。
实验实施例1.鉴定FcεRIαECD融合蛋白与IgE的结合能力
比较检测了通过上述实施例2的方法纯化的四种蛋白质i)FcεRIαECD-Fc2,ii)Fcε
RIαECD-Fc2ST,iii)FcεRIαECD-Fc3和iv)FcεRIαECD-Fc3ST,以及市售的抗IgE抗体奥马珠
单抗(omalizumab,商品名:Xolair)对IgE的结合能力。具体而言,通过在蛋白GLC传感器芯
片(Bio-Rad Laboratories)的通道上包被IgE,并使得不同浓度的奥马珠单抗或每种FceR1
αECD-Fc蛋白以每分钟30μl的速度流动,来测量与IgE的结合能力。
通过使用25mM NaOH作为再生缓冲液鉴定出零基线,然后重复上述步骤进行实验。
之后,使用蛋白质结合分析仪(ProteOn XPR36,Bio-Rad Laboratories,Inc.,USA)鉴定结
合曲线。结果示于表3、以及图7和8。图8中的IgETRAP表示FceR1αECD-Fc2ST,它是与本发明的
具有与IgE结合能力的多肽的一个实施方案。
表3
17
CN 111587118 A 说 明 书 15/25 页
如表3所示,测量的本发明的一个实施方案的多肽二聚体的结合速率(ka)的值比
奥马珠单抗低1.5-2.0倍。即,发现与奥马珠单抗相比,其与除IgE以外的物质的结合能力低
1.5-2.0倍。另外,测量的本发明的一个实施方案的多肽二聚体的解离速率(kd)的值比奥马
珠单抗高40至106倍。另外,如图7和图8所示,在结合一定的时间后,奥马珠单抗无法与IgE
结合,而本发明的FcεRIαECD D融合蛋白的多肽二聚体一旦结合至IgE,就不会与IgE分离。
即,可以看出本发明的多肽二聚体不易与IgE分离,并且与奥马珠单抗相比具有更好的维持
其结合状态的能力。从结果可以看出,本发明的一个实施方案的多肽二聚体的平衡解离常
数(KD
)的值比奥马珠单抗高22-69倍。
由此可知,与奥马珠单抗相比,本发明的FcεRIαECD融合蛋白与IgE的结合能力显
著提高。特别地,已确定添加了唾液酸的FcεRIαECD-Fc2(FcεRIαECD-Fc2ST)表现出最强的
IgE结合能力,其比奥马珠单抗高69倍。特别地,对于FceR1αECD-Fc2ST而言,IgETRAP的结合
速率(Ka)和解离速率(Kd)分别比奥马珠单抗低约1.5倍和94.5倍(图7和8,以及表4)。之前
已报道IgE与FcεRIα的解离非常缓慢。已测定IgETRAP的解离也非常缓慢(图8)。结果显示,
IgETRAP与人IgE的结合能力比奥马珠单抗高69倍(图8和表4)。
表4
实验实施例2.鉴定IgETRAP与IgG介导的IgG受体的结合能力
IgETRAP不结合与IgG介导的过敏性休克相关的低亲和力IgG受体。由于过敏性休克
是奥马珠单抗的主要副作用,预期可能是由于其与低亲和力IgG受体结合所致,因此使用
BLI测定用于检测IgETRAP与IgG受体的结合能力,并将奥马珠单抗作为对照。具体而言,使用
Octet RED384系统(Pall ForteBio,CA,USA)测定IgETRAP和奥马珠单抗与IgG受体的结合程
度。
在300mM醋酸盐缓冲液(pH 5)中稀释的FcγRI、FcγRIIA、FcγRIIB、FcγRIIIA和
FcγRIIIB重组蛋白(R&D Systems Inc.,5μg/ml)被固定在已用400mM EDC和10mM磺基-NHS
组合活化的第二代氨基偶联传感器(Amine Reactive 2Generation,AR2G)上。然后,分别在
18
CN 111587118 A 说 明 书 16/25 页
300秒内测量与不同浓度的IgETRAP和奥马珠单抗的结合和解离。在此,使用的动力学缓冲液
是含有0.1%Tween-20和1%牛血清的PBS,所有实验均在30℃下用样品平板摇床以1 ,
000rpm的速率进行。
如所预期的,奥马珠单抗显示出与高亲和力IgG受体FcγRI以及低亲和力IgG受体
如FcγRIIA、FcγRIIB、FcγRIIIA和FcγRIIIB的显著的结合能力(图9-14)。这意味着,
IgETRAP与奥马珠单抗不同,其不能与IgG受体如FcγRIIA和FcγRIII结合,因此具有极低的
诱导IgG介导的过敏反应的风险(图9-14)。奥马珠单抗和IgETRAP与IgG受体的结合能力被定
量检测并且结果显示在图14中。
实验实施例3.通过β-己糖胺酶测定法鉴定在小鼠骨髓来源的肥大细胞中的FcεRI
αECD融合蛋白的活性
进行β-己糖胺酶测定,以分析本发明的FcεRIαECD融合蛋白的体外活性。具体地,
将本发明的一个实施方案的FcεRIαECD-Fc2蛋白在不同浓度下与小鼠IgE(1μg/mL)混合,并
在室温(20℃)下孵育30分钟以准备样品。用汉克平衡盐溶液(Hank 's balanced salt
solution,HBSS)缓冲液洗涤培养物中的小鼠骨髓肥大细胞,以除去培养基,从而活化肥大
细胞,同时测量细胞数。然后调整细胞数,将5×105细胞注入40μL HBSS缓冲液中。
然后,将事先进行孵育制得的50μL样品溶液加入到活化的肥大细胞中。然后,将所
得产物在5%CO2培养箱中于37℃孵育30分钟。随后,在加入10μL DNP(2 ,4-二硝基苯酚,
100ng/mL)(一种外源抗原)后,再次在37℃的5%CO2中孵育30分钟,然后分离出30μL的上清
液。充分混合30μL分离的上清液和30μL底物(4-硝基苯基N-乙酰基-β-D-氨基葡萄糖苷,
5.84mM),然后在5%CO2中于37℃孵育20分钟。接着,加入140μL作为终止溶液的0.1M碳酸钠
缓冲液(pH 10)以终止反应。此后,测量在405nm处的吸光度,以鉴定在活化的肥大细胞中由
外源抗原分泌的α-己糖胺酶的分泌量。结果示于图15A。
在1μg/ml小鼠IgE的存在下,IgETRAP以以剂量依赖性的方式抑制肥大细胞的脱粒,
IC50为0.45μg/ml的(显示出50%的抑制作用所必需的药物浓度)(图15A)。在IgE:IgETRAP的
分子比为0.79时,IgETRAP完全抑制了骨髓肥大细胞的脱粒(表5)。
表5
具体地,如图15A所示,本发明的一个实施方案的多肽二聚体在浓度为小鼠IgE的
一半(0.5μg/mL)的情况下,显示出对肥大细胞的抑制率约为49.4%,并且其浓度与小鼠IgE
相同(1μg/mL)的情况下,显示出对肥大细胞的抑制率约为99.4%。即可以看出,本发明的
FceRIa-ECD多肽二聚体极大地抑制了IgE诱导的骨髓来源的肥大细胞的活性。
实验实施例4.使用β-己糖胺酶测定法比较FcεRIαECD融合蛋白和抗人IgE抗体在
表达人FcεRI的骨髓来源的肥大细胞中的活性
进行β-己糖胺酶测定,以通过体外活性分析鉴定FcεRIαECD融合蛋白相对于
Xolair的优越性。制备不同浓度的相应药物FcεRIαECD-Fc2ST(IgETRAP)和Xolair,然后与人
IgE(1μg/mL)混合。接着在室温下进行30分钟的孵育。在药物的预孵育过程中,导入人FcεRI
19
CN 111587118 A 说 明 书 17/25 页
基因,并制备从已去除FcεRI gene基因的来源于小鼠骨髓并由其分化出的肥大细胞。制备
的肥大细胞用HBSS缓冲液洗涤,然后将5×105细胞注入60μL HBSS缓冲液中。将20μL预孵育
的样品添加到制备的肥大细胞中,然后在5%CO2培养箱中于37℃孵育30分钟。
随后,在加入20μL抗人IgE抗体(BioLegend,目录号325502,0.5μg/mL)以诱导与外
源抗原相似的反应,将所得产物再次在5%CO2培养箱中于37℃孵育30分钟。随后,在4℃以
1,500rpm离心后,分离出30μL的上清液。将30μL分离的上清液和30μL底物(4-硝基苯基N-乙
酰基-β-氨基葡萄糖,5.84mM)充分混合,然后在5%CO2培养箱中于37℃孵育25分钟。然后,
加入140μL的0.1M碳酸钠缓冲液(pH 10)以终止反应。
接着,检测在405nm处的吸光度以比较分泌的β-己糖胺酶的相对量,并且鉴定出基
于每种药物浓度的肥大细胞的抑制作用。结果示于图15B。如图15B所示,测得FcεRIαECD融
合蛋白的IC50约为11.16ng/mL,Xolair蛋白的IC50约为649.8ng/mL。因此,已确定FcεRIαECD
融合蛋白对肥大细胞活性的抑制能力比Xolair高58倍。
实验实施例5.FcεRIαECD融合蛋白的体内测定:食物过敏模型
以14天的间隔向Balb/c小鼠(Orientbio Inc .)腹膜内施用两次50μg卵清蛋白
(OVA)和1mg明矾以引起过敏。此后,在第28、30、32、34和36天总共口服五次共50mg OVA,以
诱发肠道食物过敏。
在口服OVA两次后,即在第31天,将小鼠分为三组,每组包含7只小鼠。三组分别为:
第一组接受高浓度(200μg)的FcεRIαECD-Fc2ST融合蛋白,第二组接受低浓度的FcεRIαECD-
Fc2ST融合蛋白(20μg),第三组未接受任何药物。口服OVA时,测定是否由于食物过敏引起了
腹泻。在第37天处死小鼠,分析每个组的小鼠中小肠肥大细胞数量、血液中IgE的浓度和血
液中肥大细胞脱粒的酶(肥大细胞蛋白酶-1(MCPT-1))浓度。
如图16可知,经证明与未接受任何药物的小鼠组相比,接受多肽二聚体FcεRIα
ECD-Fc2ST的小鼠组在高浓度时显示出缓解食物过敏的效果,并且呈浓度依赖性。
II.具有IgE结合能力的多肽和益生菌的组合的制备及其作用的鉴定
实施例3.益生菌的培养和施用
将干酪乳杆菌(Lactobacillus casei,KACC 12413)、乳酸乳球菌(Lactococcus
lactis,KACC 13877)、发酵乳杆菌(Lactobacillus fermentum,KACC 11441)和鼠李糖乳杆
菌(L.rhamnosus,KACC 11953)接种在MRS肉汤或脑心浸液(BHI)培养基中并在37℃培养箱
(N-Biotek,目录号NB201L)放置24小时。考虑到罗伊氏乳杆菌(Lactobacillus reuteri,
KACC 11452)和嗜热链球菌(Streptococcus thermophiles,KACC 11857)的好氧特性,将它
们在摇床培养箱(N-biotek)中于37℃和50rpm下培养24小时。
将培养的益生菌溶解在含有10%脱脂乳和10%蔗糖的冻干培养基中,并使用冷冻
干燥机(Labcono)冻干。然后,将所得产物粉末化。通过连续稀释测量完整的益生菌中每克
存在的菌落形成单位(cfu)。
在实验过程中,使用oral zonde,每隔2-3天以每只小鼠1×109-2.5×109cfu的剂
量连续饲喂冻干益生菌。阴性对照组饲喂等量的冻干培养基。
实施例4.包含益生菌和具有与IgE结合能力的多肽的组合物的制备
将实施例1中获得的具有与IgE结合能力的多肽和实施例3中获得的益生菌混合以
制备用于治疗过敏反应的组合物。
20
CN 111587118 A 说 明 书 18/25 页
实验实施例6.鉴定FcεRIα-Fc融合蛋白对改善过敏反应的作用
以14天的间隔向Balb/c小鼠(Orientbio Inc .)腹膜内施用两次50μg卵清蛋白
(OVA)和1mg明矾,以诱发过敏。此后,在第28、30、32、34和36天共口服五次共50mg OVA,以诱
发肠道食物过敏。已被诱发食物过敏的小鼠被分为五组,每组七只。这五组分别是:第一组
接受高浓度(200μg)的FcεRIαECD重组蛋白,第二组接受低浓度(20μg)的FcεRIαECD重组蛋
白,第三组接受高浓度(200μg)的FcεRIαECD重组蛋白加长双歧杆菌(B.longum),第四组接
受低浓度(20μg)的FcεRIαECD重组蛋白加长双歧杆菌(B.longum),第五组未接受任何药物。
口服OVA时,测定是否由于食物过敏引起了腹泻。在第37天处死小鼠,分析每个组
的小鼠中小肠肥大细胞数量、血液中IgE的浓度和血液中肥大细胞脱粒的酶(肥大细胞蛋白
酶-1(MCPT-1))浓度。如图19B所示,与未接受任何药物的小鼠组相比,接受FcεRIαECD多肽
二聚体和长双歧杆菌(B.longum)的组合的小鼠组显示出减轻食物过敏的效果。
实验实施例7.IgETRAP和益生菌的联合给药对改善过敏的影响鉴定
为了评估IgETRAP对食物过敏的影响,在BALB/c小鼠中诱导了剂量依赖性急性腹
泻,以产生具有过敏原诱导的食物过敏的小鼠模型。具体地,除了以100μg/头施用IgETRAP
(一种FcεRIαECD重组蛋白)外,以与实验实施例6相同的方式进行实验。此外,将益生菌长双
歧杆菌冻干并以3×109cfu/g的剂量与粉状小鼠饲料混合。允许小鼠随意摄取饲料。为了保
持新鲜度,每2至3天更换一次与长双歧杆菌混合的小鼠饲料。结果,如下面的表6和图18所
示,同时接受益生菌长双歧杆菌和IgETRAP(一种FcεRIαECD多肽二聚体)的实验组显示出优
异的过敏减轻效果。
表6
使用该模型,本发明人发现单独施用IgETRAP有效地减少了腹泻的发生,并且已经
发现与单独施用IgETRAP相比,联合施用IgETRAP和长双歧杆菌显著减少了腹泻的发生(图
18)。据报道,长双歧杆菌通过细胞凋亡减少了肥大细胞的数量,并减轻了食物过敏症状。但
是,腹膜内注射IgETRAP的组比每日接受长双歧杆菌的组表现出更好的治疗效果(图18)。有
趣的是,即使在使用浓度降低了10倍的IgETRAP的情况下,IgETRAP和长双歧杆菌的联合治
疗也表现出与单独使用IgETRAP的治疗相似的效果(图19B)。
实验实施例8.鉴定IgETRAP和长双歧杆菌联合施用时的效果:MCPT-1和IgE水平
此外,测量血清MCPT-1的水平以鉴定肥大细胞脱粒。单独施用IgETRAP和长双歧杆
菌不会降低MCPT-1的水平,但是IgETRAP和长双歧杆菌的联合施用显著降低了MCPT-1的水平
21
CN 111587118 A 说 明 书 19/25 页
(图20)。因此,可以看出长双歧杆菌和IgETRAP协同抑制肥大细胞脱粒。在食物过敏的小鼠模
型中,为了研究降低IgE的治疗剂的功效,使用ELISA来分析血清中总IgE和游离IgE的水平。
IgETRAP以及IgETRAP和长双歧杆菌的组合稍微增加了总IgE的水平(图21)。然而,IgETRAP以及
IgETRAP和长双歧杆菌的组合大大降低了游离IgE的水平(图22)。相反,单独施用长双歧杆菌
不影响总IgE和游离IgE的水平(图21和22)。因此,IgETRAP和长双歧杆菌以几种方式减轻食
物过敏症状,表明这种组合可以对食物过敏发挥有效的治疗作用。
实验实施例9.鉴定IgETRAP和长双歧杆菌组合对肥大细胞数量和杯状细胞增生的
抑制作用
为了研究IgETRAP和长双歧杆菌及其组合是否减少肥大细胞的数量,使用氯乙酸酯
酶活性对肥大细胞染色。结果表明,单独施用IgETRAP和长双歧杆菌显著减少了肥大细胞的
数量,并且两者的组合更为有效(图23和24)。可以看出,长双歧杆菌的结果与以前报道的一
致。研究了IgETRAP、长双歧杆菌及其组合疗法能否抑制由Th2细胞因子环境诱导的杯状细胞
增生。如所预期的,已确认食物过敏性小鼠的小肠中的杯状细胞的大小增加,并且随着细胞
数目的增加而发生增生(图25和26)。
已经确定,IgETRAP和长双歧杆菌的施用显著降低了杯状细胞的大小和数量,并且
在联合施用IgETRAP和长双歧杆菌的情况下,这种效果变得更明显(图25和26)。另外,可以看
出,IgETRAP和长双歧杆菌倾向于降低IL-33的mRNA表达,并且在联合施用的情况下该效果变
得更显著(图28)。这些结果表明,IgETRAP和长双歧杆菌显著抑制肠肥大细胞的数量和杯状
细胞增生,并且在联合施用的情况下表现出进一步改善的效果。
实验实施例10.小鼠口服施用IgETRAP后血清中IgETRAP的存在的鉴定
小鼠口服施用300μg IgETRAP,2小时后,通过眼眶后采血来收集血清。在室温下反
应30分钟后,通过在4℃和1300rpm下离心15分钟获得上清液(血清)。在96孔免疫板中包被
抗FcεRI抗体(Abcam,ab54411),并在4℃下反应过夜。用洗涤缓冲液(含有0.05%Tween-20
的PBS)洗涤板,然后向其中加入封闭缓冲液(含有1%牛血清白蛋白的PBS)。反应1小时后,
再次用洗涤缓冲液洗涤板,并将标准样品和稀释的小鼠血清样品添加至板。反应2小时后,
并再次用洗涤缓冲液洗涤。向其中加入抗人IgG4 Fc抗体(Abcam,ab99823),并反应1小时。
再次用洗涤缓冲液洗涤板,并向其中加入TMB底物(Supmodics)。在遮光的情况下使其反应
20分钟后,添加终止反应液(1M H2SO4)以终止反应。将波长设置为450nm,用酶标仪(Epoch
micro microplate spectrophotometer)测量浓度值。结果,在正常小鼠的血清中检测到
IgETRAP(图35)。从这些结果可以看出,在口服施用IgETRAP蛋白的情况下,通过与粘膜中的
FcRn结合将IgETRAP蛋白递送至血清中,因此可以显示出治疗效果。
实验实施例11.在食物过敏模型中鉴定通过联合施用IgETRAP和各种益生菌获得的
效果
为了评估IgETRAP和益生菌对食物过敏的效果,在BALB/c小鼠中诱导了剂量依赖性
急性腹泻,以产生具有过敏原诱导的食物过敏的小鼠模型。具体地,以与实验实施例7相同
的方式进行实验,不同之处在于,如图17的实验方案以100μg/头向小鼠腹膜内给予IgETRAP
(一种FcεRIαECD重组蛋白)。此外,在实验过程中,每隔2到3天使用口服zonde,以每只小鼠1
×109到2.5×109cfu的剂量连续饲喂冻干益生菌,并向阴性对照饲喂等量的冻干培养基。
在图29中示出了通过鉴定施用IgETRAP和干酪乳杆菌后的腹泻频率获得的结果。在
22
CN 111587118 A 说 明 书 20/25 页
图30中示出了通过鉴定服用IgETRAP和乳酸乳杆菌后的腹泻频率获得的结果。在图31中示出
了通过鉴定施用IgETRAP和嗜热链球菌后的腹泻频率获得的结果。在图32显示了通过鉴定施
用IgETRAP和鼠李糖乳杆菌后的腹泻频率获得的结果。在图33示出了通过鉴定施用IgETRAP和
罗伊氏乳杆菌后的腹泻频率而获得的结果。在图34中示出了通过鉴定施用IgETRAP和发酵乳
杆菌后的腹泻频率而获得的结果。
参考简写列表
B.longum:Bifidobacterium longum,长双歧杆菌
OIT:Oral immunotherapy,口服免疫疗法
PSA:Passive systemic anaphylaxis,被动系统性过敏反应
SPR:Surface plasmon resonance,表面等离子共振
BLI:Bio-layer interferometry,生物膜层干涉法
[0200] BMMC:Bone marrow-derived mast cell,骨髓来源的肥大细胞
[0201] cfu:Colony-forming unit,菌落形成单位
[0202] MCPT-1:Mast cell protease-1,肥大细胞蛋白酶-1
[0203] OVA:Ovalbumin,卵清蛋白
[0204] Treg cell:Regulatory T cell,调节性T细胞
[0205] Th2 cell:Type 2 helper T cell,2型辅助性T细胞
[0206] ILC2:Group 2 innate lymphoid cell,第二组先天性淋巴样细胞
[0207] 序列表
[0208] SEQ ID NO:1
[0209]
[0210] SEQ ID NO:2
[0211]
[0212] SEQ ID NO:3
[0213] RNTGRGGEEK KGSKEKEEQE ERETKTPECP
[0214] SEQ ID NO:4
[0215] AQPQAEGSLA KATTAPATTR NTGRGGEEKK GSKEKEEQEE RETKTPECP
[0216] SEQ ID NO:5
23
CN 111587118 A 说 明 书 21/25 页
[0217]
[0218] SEQ ID NO:6
[0219]
[0220] SEQ ID NO:7
[0221]
[0222] SEQ ID NO:8
[0223]
[0224] SEQ ID NO:9
[0225] MDAMLRGLCC VLLLCGAVFV SPSHA
[0226] SEQ ID NO:10
[0227] atggacgcca tgctgagagg cctgtgctgt gtgctgctgc tgtgcggcgc cgtgttcgtg
tcccctagcc acgcc
[0228] SEQ ID NO:11
24
CN 111587118 A 说 明 书 22/25 页
[0229]
[0230] SEQ ID NO:12
[0231]
[0232]
[0233] SEQ ID NO:13
25
CN 111587118 A 说 明 书 23/25 页
[0234]
[0235] SEQ ID NO:14
[0236]
[0237]
[0238] SEQ ID NO:15
26
CN 111587118 A 说 明 书 24/25 页
[0239]
[0240] SEQ ID NO:16
[0241]
[0242]
[0243] SEQ ID NO:17
[0244] RNTGRGGEEK KXXKEKEEQE ERETKTPECP
[0245] SEQ ID NO:18
[0246] AQPQAEGSLA KATTAPATTR NTGRGGEEKK XXKEKEEQEE RETKTPECP
[0247] SEQ ID NO:19
[0248] RNTGRGGEEK KKEKEKEEQE ERETKTPECP
[0249] SEQ ID NO:20
27
CN 111587118 A 说 明 书 25/25 页
[0250]
[0251] SEQ ID NO:21
[0252]
[0253]
[0254] SEQ ID NO:22
[0255]
28
CN 111587118 A 序 列 表 1/18 页
SEQUENCE LISTING
<110> GI 医诺微新
<120> 包含益生菌和具有与IgE结合能力的多肽的组合物及其用途
<130> P20113063WP
<150> KR 10-2018-0004421
<151> 2018-01-12
<160> 22
<170> PatentIn version 3.5
<210> 1
<211> 180
<212> PRT
<213> Artificial Sequence
<220>
<223> FCeRI1 ECD
<400> 1
Val Pro Gln Lys Pro Lys Val Ser Leu Asn Pro Pro Trp Asn Arg Ile
1 5 10 15
Phe Lys Gly Glu Asn Val Thr Leu Thr Cys Asn Gly Asn Asn Phe Phe
20 25 30
Glu Val Ser Ser Thr Lys Trp Phe His Asn Gly Ser Leu Ser Glu Glu
35 40 45
Thr Asn Ser Ser Leu Asn Ile Val Asn Ala Lys Phe Glu Asp Ser Gly
50 55 60
Glu Tyr Lys Cys Gln His Gln Gln Val Asn Glu Ser Glu Pro Val Tyr
65 70 75 80
Leu Glu Val Phe Ser Asp Trp Leu Leu Leu Gln Ala Ser Ala Glu Val
85 90 95
Val Met Glu Gly Gln Pro Leu Phe Leu Arg Cys His Gly Trp Arg Asn
100 105 110
Trp Asp Val Tyr Lys Val Ile Tyr Tyr Lys Asp Gly Glu Ala Leu Lys
115 120 125
Tyr Trp Tyr Glu Asn His Asn Ile Ser Ile Thr Asn Ala Thr Val Glu
130 135 140
Asp Ser Gly Thr Tyr Tyr Cys Thr Gly Lys Val Trp Gln Leu Asp Tyr
145 150 155 160
Glu Ser Glu Pro Leu Asn Ile Thr Val Ile Lys Ala Pro Arg Glu Lys
165 170 175
Tyr Trp Leu Gln
29
CN 111587118 A 序 列 表 2/18 页
180
<210> 2
<211> 215
<212> PRT
<213> Artificial Sequence
<220>
<223> 经修饰的Fc
<400> 2
Ser His Thr Gln Pro Leu Gly Val Phe Leu Phe Pro Pro Lys Pro Lys
1 5 10 15
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
20 25 30
Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp
35 40 45
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe
50 55 60
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
65 70 75 80
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu
85 90 95
Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
100 105 110
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys
115 120 125
Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
130 135 140
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
145 150 155 160
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
165 170 175
Arg Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser
180 185 190
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
195 200 205
Leu Ser Leu Ser Leu Gly Lys
210 215
<210> 3
<211> 30
<212> PRT
30
CN 111587118 A 序 列 表 3/18 页
<213> Artificial Sequence
<220>
<223> IgD铰链变体
<400> 3
Arg Asn Thr Gly Arg Gly Gly Glu Glu Lys Lys Gly Ser Lys Glu Lys
1 5 10 15
Glu Glu Gln Glu Glu Arg Glu Thr Lys Thr Pro Glu Cys Pro
20 25 30
<210> 4
<211> 49
<212> PRT
<213> Artificial Sequence
<220>
<223> IgD铰链变体
<400> 4
Ala Gln Pro Gln Ala Glu Gly Ser Leu Ala Lys Ala Thr Thr Ala Pro
1 5 10 15
Ala Thr Thr Arg Asn Thr Gly Arg Gly Gly Glu Glu Lys Lys Gly Ser
20 25 30
Lys Glu Lys Glu Glu Gln Glu Glu Arg Glu Thr Lys Thr Pro Glu Cys
35 40 45
Pro
<210> 5
<211> 540
<212> DNA
<213> Artificial Sequence
<220>
<223> FCeRI1 ECD的核苷酸序列
<400> 5
gtgccccaga agcccaaggt gagcctgaac cctccctgga acagaatctt caagggcgag 60
aacgtgaccc tgacctgcaa cggcaacaac ttcttcgagg tgagcagcac caagtggttc 120
cacaatggca gcctgagcga ggagaccaac agctccctga acatcgtgaa cgccaagttc 180
gaggacagcg gcgagtacaa gtgccagcac cagcaggtga acgagagcga gcccgtgtac 240
ctggaggtgt tcagcgactg gctgctgctg caggccagcg ccgaggtggt gatggagggc 300
cagcccctgt tcctgagatg ccacggctgg agaaactggg acgtgtacaa ggtgatctac 360
tacaaggatg gcgaggccct gaagtactgg tacgagaacc acaacatctc catcaccaac 420
gccaccgtgg aggacagcgg cacctactac tgcacaggca aggtgtggca gctggactac 480
gagagcgagc ccctgaacat caccgtgatc aaggctccca gagagaagta ctggctgcag 540
<210> 6
31
CN 111587118 A 序 列 表 4/18 页
<211> 561
<212> DNA
<213> Artificial Sequence
<220>
<223> 经修饰的Fc的核苷酸序列
<400> 6
tgcgtggtcg tggatgtgag ccaggaagat cccgaagtgc agttcaactg gtacgtggat 60
ggcgtggaag tgcacaacgc caagaccaag cccagagaag agcagttcaa ctccacctac 120
agagtggtga gcgtgctgac cgtgctgcac caggactggc tgaacggcaa ggagtacaag 180
tgcaaggtgt ccaacaaagg cctgcccagc tccatcgaga agaccatcag caaagccaaa 240
ggccagccca gagaacccca ggtgtacacc ctgcctccca gccaggaaga gatgaccaag 300
aaccaggtgt ccctgacctg cctggtgaaa ggcttctacc ccagcgacat cgccgtggag 360
tgggaaagca acggccagcc cgagaacaat tacaagacaa cccctcccgt gctggatagc 420
gatggcagct tctttctgta cagcagactg accgtggaca agagcagatg gcaggaaggc 480
aacgtgttca gctgcagcgt gatgcacgaa gccctgcaca accactacac ccagaagagc 540
ctgtccctga gcctgggcaa g 561
<210> 7
<211> 174
<212> DNA
<213> Artificial Sequence
<220>
<223> IgD铰链变体的核苷酸序列
<400> 7
aggaacaccg gcagaggagg cgaggaaaag aaaggaagca aggagaagga ggagcaggag 60
gaaagagaaa ccaagacccc cgagtgcccc agccacaccc agcccctggg cgtgttcctg 120
ttccccccca agcccaagga caccctgatg atcagcagaa cccccgaggt gacc 174
<210> 8
<211> 231
<212> DNA
<213> Artificial Sequence
<220>
<223> IgD铰链变体的核苷酸序列
<400> 8
gcccagcccc aggccgaggg cagcctggct aaggccacca cagctcccgc caccaccagg 60
aacaccggca gaggaggcga ggaaaagaaa ggaagcaagg agaaggagga gcaggaggaa 120
agagaaacca agacccccga gtgccccagc cacacccagc ccctgggcgt gttcctgttc 180
ccccccaagc ccaaggacac cctgatgatc agcagaaccc ccgaggtgac c 231
<210> 9
<211> 25
32
CN 111587118 A 序 列 表 5/18 页
<212> PRT
<213> Artificial Sequence
<220>
<223> 信号肽
<400> 9
Met Asp Ala Met Leu Arg Gly Leu Cys Cys Val Leu Leu Leu Cys Gly
1 5 10 15
Ala Val Phe Val Ser Pro Ser His Ala
20 25
<210> 10
<211> 75
<212> DNA
<213> Artificial Sequence
<220>
<223> 信号肽核苷酸
<400> 10
atggacgcca tgctgagagg cctgtgctgt gtgctgctgc tgtgcggcgc cgtgttcgtg 60
tcccctagcc acgcc 75
<210> 11
<211> 450
<212> PRT
<213> Artificial Sequence
<220>
<223> FceRIa ECD-铰链-Fc2
<400> 11
Met Asp Ala Met Leu Arg Gly Leu Cys Cys Val Leu Leu Leu Cys Gly
1 5 10 15
Ala Val Phe Val Ser Pro Ser His Ala Val Pro Gln Lys Pro Lys Val
20 25 30
Ser Leu Asn Pro Pro Trp Asn Arg Ile Phe Lys Gly Glu Asn Val Thr
35 40 45
Leu Thr Cys Asn Gly Asn Asn Phe Phe Glu Val Ser Ser Thr Lys Trp
50 55 60
Phe His Asn Gly Ser Leu Ser Glu Glu Thr Asn Ser Ser Leu Asn Ile
65 70 75 80
Val Asn Ala Lys Phe Glu Asp Ser Gly Glu Tyr Lys Cys Gln His Gln
85 90 95
Gln Val Asn Glu Ser Glu Pro Val Tyr Leu Glu Val Phe Ser Asp Trp
100 105 110
33
CN 111587118 A 序 列 表 6/18 页
Leu Leu Leu Gln Ala Ser Ala Glu Val Val Met Glu Gly Gln Pro Leu
115 120 125
Phe Leu Arg Cys His Gly Trp Arg Asn Trp Asp Val Tyr Lys Val Ile
130 135 140
Tyr Tyr Lys Asp Gly Glu Ala Leu Lys Tyr Trp Tyr Glu Asn His Asn
145 150 155 160
Ile Ser Ile Thr Asn Ala Thr Val Glu Asp Ser Gly Thr Tyr Tyr Cys
165 170 175
Thr Gly Lys Val Trp Gln Leu Asp Tyr Glu Ser Glu Pro Leu Asn Ile
180 185 190
Thr Val Ile Lys Ala Pro Arg Glu Lys Tyr Trp Leu Gln Arg Asn Thr
195 200 205
Gly Arg Gly Gly Glu Glu Lys Lys Gly Ser Lys Glu Lys Glu Glu Gln
210 215 220
Glu Glu Arg Glu Thr Lys Thr Pro Glu Cys Pro Ser His Thr Gln Pro
225 230 235 240
Leu Gly Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu
260 265 270
Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
340 345 350
Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu
355 360 365
Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp
405 410 415
Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His
34
CN 111587118 A 序 列 表 7/18 页
420 425 430
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu
435 440 445
Gly Lys
450
<210> 12
<211> 1350
<212> DNA
<213> Artificial Sequence
<220>
<223> FceRIa ECD-铰链-Fc2的核苷酸序列
<400> 12
atggacgcca tgctgagagg cctgtgctgt gtgctgctgc tgtgcggcgc cgtgttcgtg 60
tcccctagcc acgccgtgcc ccagaagccc aaggtgagcc tgaaccctcc ctggaacaga 120
atcttcaagg gcgagaacgt gaccctgacc tgcaacggca acaacttctt cgaggtgagc 180
agcaccaagt ggttccacaa tggcagcctg agcgaggaga ccaacagctc cctgaacatc 240
gtgaacgcca agttcgagga cagcggcgag tacaagtgcc agcaccagca ggtgaacgag 300
agcgagcccg tgtacctgga ggtgttcagc gactggctgc tgctgcaggc cagcgccgag 360
gtggtgatgg agggccagcc cctgttcctg agatgccacg gctggagaaa ctgggacgtg 420
tacaaggtga tctactacaa ggatggcgag gccctgaagt actggtacga gaaccacaac 480
atctccatca ccaacgccac cgtggaggac agcggcacct actactgcac aggcaaggtg 540
tggcagctgg actacgagag cgagcccctg aacatcaccg tgatcaaggc tcccagagag 600
aagtactggc tgcagaggaa caccggcaga ggaggcgagg aaaagaaagg aagcaaggag 660
aaggaggagc aggaggaaag agaaaccaag acccccgagt gccccagcca cacccagccc 720
ctgggcgtgt tcctgttccc ccccaagccc aaggacaccc tgatgatcag cagaaccccc 780
gaggtgacct gcgtggtcgt ggatgtgagc caggaagatc ccgaagtgca gttcaactgg 840
tacgtggatg gcgtggaagt gcacaacgcc aagaccaagc ccagagaaga gcagttcaac 900
tccacctaca gagtggtgag cgtgctgacc gtgctgcacc aggactggct gaacggcaag 960
gagtacaagt gcaaggtgtc caacaaaggc ctgcccagct ccatcgagaa gaccatcagc 1020
aaagccaaag gccagcccag agaaccccag gtgtacaccc tgcctcccag ccaggaagag 1080
atgaccaaga accaggtgtc cctgacctgc ctggtgaaag gcttctaccc cagcgacatc 1140
gccgtggagt gggaaagcaa cggccagccc gagaacaatt acaagacaac ccctcccgtg 1200
ctggatagcg atggcagctt ctttctgtac agcagactga ccgtggacaa gagcagatgg 1260
caggaaggca acgtgttcag ctgcagcgtg atgcacgaag ccctgcacaa ccactacacc 1320
cagaagagcc tgtccctgag cctgggcaag 1350
<210> 13
<211> 469
<212> PRT
<213> Artificial Sequence
35
CN 111587118 A 序 列 表 8/18 页
<220>
<223> FceRIa ECD-铰链-Fc3
<400> 13
Met Asp Ala Met Leu Arg Gly Leu Cys Cys Val Leu Leu Leu Cys Gly
1 5 10 15
Ala Val Phe Val Ser Pro Ser His Ala Val Pro Gln Lys Pro Lys Val
20 25 30
Ser Leu Asn Pro Pro Trp Asn Arg Ile Phe Lys Gly Glu Asn Val Thr
35 40 45
Leu Thr Cys Asn Gly Asn Asn Phe Phe Glu Val Ser Ser Thr Lys Trp
50 55 60
Phe His Asn Gly Ser Leu Ser Glu Glu Thr Asn Ser Ser Leu Asn Ile
65 70 75 80
Val Asn Ala Lys Phe Glu Asp Ser Gly Glu Tyr Lys Cys Gln His Gln
85 90 95
Gln Val Asn Glu Ser Glu Pro Val Tyr Leu Glu Val Phe Ser Asp Trp
100 105 110
Leu Leu Leu Gln Ala Ser Ala Glu Val Val Met Glu Gly Gln Pro Leu
115 120 125
Phe Leu Arg Cys His Gly Trp Arg Asn Trp Asp Val Tyr Lys Val Ile
130 135 140
Tyr Tyr Lys Asp Gly Glu Ala Leu Lys Tyr Trp Tyr Glu Asn His Asn
145 150 155 160
Ile Ser Ile Thr Asn Ala Thr Val Glu Asp Ser Gly Thr Tyr Tyr Cys
165 170 175
Thr Gly Lys Val Trp Gln Leu Asp Tyr Glu Ser Glu Pro Leu Asn Ile
180 185 190
Thr Val Ile Lys Ala Pro Arg Glu Lys Tyr Trp Leu Gln Ala Gln Pro
195 200 205
Gln Ala Glu Gly Ser Leu Ala Lys Ala Thr Thr Ala Pro Ala Thr Thr
210 215 220
Arg Asn Thr Gly Arg Gly Gly Glu Glu Lys Lys Gly Ser Lys Glu Lys
225 230 235 240
Glu Glu Gln Glu Glu Arg Glu Thr Lys Thr Pro Glu Cys Pro Ser His
245 250 255
Thr Gln Pro Leu Gly Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr
260 265 270
Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val
275 280 285
36
CN 111587118 A 序 列 表 9/18 页
Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val
290 295 300
Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser
305 310 315 320
Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu
325 330 335
Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser
340 345 350
Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro
355 360 365
Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys Asn Gln
370 375 380
Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala
385 390 395 400
Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr
405 410 415
Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu
420 425 430
Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser
435 440 445
Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser
450 455 460
Leu Ser Leu Gly Lys
465
<210> 14
<211> 1407
<212> DNA
<213> Artificial Sequence
<220>
<223> FceRIa ECD-铰链-Fc3的核苷酸序列
<400> 14
atggacgcca tgctgagagg cctgtgctgt gtgctgctgc tgtgcggcgc cgtgttcgtg 60
tcccctagcc acgccgtgcc ccagaagccc aaggtgagcc tgaaccctcc ctggaacaga 120
atcttcaagg gcgagaacgt gaccctgacc tgcaacggca acaacttctt cgaggtgagc 180
agcaccaagt ggttccacaa tggcagcctg agcgaggaga ccaacagctc cctgaacatc 240
gtgaacgcca agttcgagga cagcggcgag tacaagtgcc agcaccagca ggtgaacgag 300
agcgagcccg tgtacctgga ggtgttcagc gactggctgc tgctgcaggc cagcgccgag 360
gtggtgatgg agggccagcc cctgttcctg agatgccacg gctggagaaa ctgggacgtg 420
tacaaggtga tctactacaa ggatggcgag gccctgaagt actggtacga gaaccacaac 480
37
CN 111587118 A 序 列 表 10/18 页
atctccatca ccaacgccac cgtggaggac agcggcacct actactgcac aggcaaggtg 540
tggcagctgg actacgagag cgagcccctg aacatcaccg tgatcaaggc tcccagagag 600
aagtactggc tgcaggccca gccccaggcc gagggcagcc tggctaaggc caccacagct 660
cccgccacca ccaggaacac cggcagagga ggcgaggaaa agaaaggaag caaggagaag 720
gaggagcagg aggaaagaga aaccaagacc cccgagtgcc ccagccacac ccagcccctg 780
ggcgtgttcc tgttcccccc caagcccaag gacaccctga tgatcagcag aacccccgag 840
gtgacctgcg tggtcgtgga tgtgagccag gaagatcccg aagtgcagtt caactggtac 900
gtggatggcg tggaagtgca caacgccaag accaagccca gagaagagca gttcaactcc 960
acctacagag tggtgagcgt gctgaccgtg ctgcaccagg actggctgaa cggcaaggag 1020
tacaagtgca aggtgtccaa caaaggcctg cccagctcca tcgagaagac catcagcaaa 1080
gccaaaggcc agcccagaga accccaggtg tacaccctgc ctcccagcca ggaagagatg 1140
accaagaacc aggtgtccct gacctgcctg gtgaaaggct tctaccccag cgacatcgcc 1200
gtggagtggg aaagcaacgg ccagcccgag aacaattaca agacaacccc tcccgtgctg 1260
gatagcgatg gcagcttctt tctgtacagc agactgaccg tggacaagag cagatggcag 1320
gaaggcaacg tgttcagctg cagcgtgatg cacgaagccc tgcacaacca ctacacccag 1380
aagagcctgt ccctgagcct gggcaag 1407
<210> 15
<211> 406
<212> PRT
<213> Artificial Sequence
<220>
<223> 人a-2,6-唾液酸转移酶
<400> 15
Met Ile His Thr Asn Leu Lys Lys Lys Phe Ser Cys Cys Val Leu Val
1 5 10 15
Phe Leu Leu Phe Ala Val Ile Cys Val Trp Lys Glu Lys Lys Lys Gly
20 25 30
Ser Tyr Tyr Asp Ser Phe Lys Leu Gln Thr Lys Glu Phe Gln Val Leu
35 40 45
Lys Ser Leu Gly Lys Leu Ala Met Gly Ser Asp Ser Gln Ser Val Ser
50 55 60
Ser Ser Ser Thr Gln Asp Pro His Arg Gly Arg Gln Thr Leu Gly Ser
65 70 75 80
Leu Arg Gly Leu Ala Lys Ala Lys Pro Glu Ala Ser Phe Gln Val Trp
85 90 95
Asn Lys Asp Ser Ser Ser Lys Asn Leu Ile Pro Arg Leu Gln Lys Ile
100 105 110
Trp Lys Asn Tyr Leu Ser Met Asn Lys Tyr Lys Val Ser Tyr Lys Gly
115 120 125
38
CN 111587118 A 序 列 表 11/18 页
Pro Gly Pro Gly Ile Lys Phe Ser Ala Glu Ala Leu Arg Cys His Leu
130 135 140
Arg Asp His Val Asn Val Ser Met Val Glu Val Thr Asp Phe Pro Phe
145 150 155 160
Asn Thr Ser Glu Trp Glu Gly Tyr Leu Pro Lys Glu Ser Ile Arg Thr
165 170 175
Lys Ala Gly Pro Trp Gly Arg Cys Ala Val Val Ser Ser Ala Gly Ser
180 185 190
Leu Lys Ser Ser Gln Leu Gly Arg Glu Ile Asp Asp His Asp Ala Val
195 200 205
Leu Arg Phe Asn Gly Ala Pro Thr Ala Asn Phe Gln Gln Asp Val Gly
210 215 220
Thr Lys Thr Thr Ile Arg Leu Met Asn Ser Gln Leu Val Thr Thr Glu
225 230 235 240
Lys Arg Phe Leu Lys Asp Ser Leu Tyr Asn Glu Gly Ile Leu Ile Val
245 250 255
Trp Asp Pro Ser Val Tyr His Ser Asp Ile Pro Lys Trp Tyr Gln Asn
260 265 270
Pro Asp Tyr Asn Phe Phe Asn Asn Tyr Lys Thr Tyr Arg Lys Leu His
275 280 285
Pro Asn Gln Pro Phe Tyr Ile Leu Lys Pro Gln Met Pro Trp Glu Leu
290 295 300
Trp Asp Ile Leu Gln Glu Ile Ser Pro Glu Glu Ile Gln Pro Asn Pro
305 310 315 320
Pro Ser Ser Gly Met Leu Gly Ile Ile Ile Met Met Thr Leu Cys Asp
325 330 335
Gln Val Asp Ile Tyr Glu Phe Leu Pro Ser Lys Arg Lys Thr Asp Val
340 345 350
Cys Tyr Tyr Tyr Gln Lys Phe Phe Asp Ser Ala Cys Thr Met Gly Ala
355 360 365
Tyr His Pro Leu Leu Tyr Glu Lys Asn Leu Val Lys His Leu Asn Gln
370 375 380
Gly Thr Asp Glu Asp Ile Tyr Leu Leu Gly Lys Ala Thr Leu Pro Gly
385 390 395 400
Phe Arg Thr Ile His Cys
405
<210> 16
<211> 1218
<212> DNA
39
CN 111587118 A 序 列 表 12/18 页
<213> Artificial Sequence
<220>
<223> 人a-2,6-唾液酸转移酶的核苷酸序列
<400> 16
atgatccaca ccaacctgaa gaagaagttc agctgctgcg tgctggtgtt cctgctgttc 60
gccgtgatct gcgtgtggaa ggagaagaag aaaggcagct actacgacag cttcaagctg 120
cagaccaagg agttccaggt gctgaagagc ctgggcaagc tggccatggg cagcgacagc 180
cagagcgtgt ccagctcctc cacccaggat ccccacagag gcagacagac cctgggcagc 240
ctgagaggcc tggccaaggc caagcccgag gccagcttcc aggtgtggaa caaggacagc 300
agcagcaaga acctgatccc cagactgcag aagatctgga agaactacct gagcatgaac 360
aagtacaagg tgagctacaa aggacccgga cccggcatca agttcagcgc cgaggccctg 420
aggtgccacc tgagagacca cgtgaacgtg agcatggtgg aagtgaccga cttccccttc 480
aacaccagcg agtgggaagg ctacctgccc aaggagagca tcaggaccaa ggctggcccc 540
tggggcagat gcgccgtggt gagcagcgct ggcagcctga agagctccca gctgggcaga 600
gagatcgacg accacgatgc cgtgctgagg ttcaatggcg ctcccaccgc caacttccag 660
caggacgtgg gcaccaagac cacaatccgg ctgatgaaca gccagctggt gacaaccgag 720
aagcggttcc tgaaggacag cctgtacaac gagggcatcc tgatcgtgtg ggatcccagc 780
gtgtaccaca gcgacatccc caagtggtac cagaatcccg actacaactt cttcaacaac 840
tacaagacct atagaaagct gcaccccaac cagcccttct acatcctgaa gccccagatg 900
ccctgggagc tgtgggacat cctgcaggag atcagccctg aagagatcca gcccaaccct 960
ccctccagcg gcatgctggg cattatcatc atgatgaccc tgtgcgacca ggtggacatc 1020
tacgagttcc tgcccagcaa gagaaagacc gacgtgtgct actactatca gaagttcttc 1080
gacagcgcct gcaccatggg cgcctaccac cccctgctgt acgagaagaa cctggtgaag 1140
cacctgaacc agggcaccga cgaggacatc tacctgctgg gcaaagccac cctgcccggc 1200
ttcagaacca tccactgc 1218
<210> 17
<211> 30
<212> PRT
<213> Artificial Sequence
<220>
<223> IgD铰链变体
<220>
<221> misc_feature
<222> (12)
<223> Xaa is Lys or Gly
<220>
<221> misc_feature
<222> (13)
<223> Xaa is Glu, Gly or Ser
40
CN 111587118 A 序 列 表 13/18 页
<400> 17
Arg Asn Thr Gly Arg Gly Gly Glu Glu Lys Lys Xaa Xaa Lys Glu Lys
1 5 10 15
Glu Glu Gln Glu Glu Arg Glu Thr Lys Thr Pro Glu Cys Pro
20 25 30
<210> 18
<211> 49
<212> PRT
<213> Artificial Sequence
<220>
<223> IgD铰链变体
<220>
<221> misc_feature
<222> (31)
<223> Xaa is Lys or Gly
<220>
<221> misc_feature
<222> (32)
<223> Xaa is Glu, Gly or Ser
<400> 18
Ala Gln Pro Gln Ala Glu Gly Ser Leu Ala Lys Ala Thr Thr Ala Pro
1 5 10 15
Ala Thr Thr Arg Asn Thr Gly Arg Gly Gly Glu Glu Lys Lys Xaa Xaa
20 25 30
Lys Glu Lys Glu Glu Gln Glu Glu Arg Glu Thr Lys Thr Pro Glu Cys
35 40 45
Pro
<210> 19
<211> 30
<212> PRT
<213> Artificial Sequence
<220>
<223> IgD铰链
<400> 19
Arg Asn Thr Gly Arg Gly Gly Glu Glu Lys Lys Lys Glu Lys Glu Lys
1 5 10 15
Glu Glu Gln Glu Glu Arg Glu Thr Lys Thr Pro Glu Cys Pro
20 25 30
<210> 20
41
CN 111587118 A 序 列 表 14/18 页
<211> 425
<212> PRT
<213> Artificial Sequence
<220>
<223> FceRIa ECD-铰链-Fc1
<400> 20
Val Pro Gln Lys Pro Lys Val Ser Leu Asn Pro Pro Trp Asn Arg Ile
1 5 10 15
Phe Lys Gly Glu Asn Val Thr Leu Thr Cys Asn Gly Asn Asn Phe Phe
20 25 30
Glu Val Ser Ser Thr Lys Trp Phe His Asn Gly Ser Leu Ser Glu Glu
35 40 45
Thr Asn Ser Ser Leu Asn Ile Val Asn Ala Lys Phe Glu Asp Ser Gly
50 55 60
Glu Tyr Lys Cys Gln His Gln Gln Val Asn Glu Ser Glu Pro Val Tyr
65 70 75 80
Leu Glu Val Phe Ser Asp Trp Leu Leu Leu Gln Ala Ser Ala Glu Val
85 90 95
Val Met Glu Gly Gln Pro Leu Phe Leu Arg Cys His Gly Trp Arg Asn
100 105 110
Trp Asp Val Tyr Lys Val Ile Tyr Tyr Lys Asp Gly Glu Ala Leu Lys
115 120 125
Tyr Trp Tyr Glu Asn His Asn Ile Ser Ile Thr Asn Ala Thr Val Glu
130 135 140
Asp Ser Gly Thr Tyr Tyr Cys Thr Gly Lys Val Trp Gln Leu Asp Tyr
145 150 155 160
Glu Ser Glu Pro Leu Asn Ile Thr Val Ile Lys Ala Pro Arg Glu Lys
165 170 175
Tyr Trp Leu Gln Arg Asn Thr Gly Arg Gly Gly Glu Glu Lys Lys Lys
180 185 190
Glu Lys Glu Lys Glu Glu Gln Glu Glu Arg Glu Thr Lys Thr Pro Glu
195 200 205
Cys Pro Ser His Thr Gln Pro Leu Gly Val Phe Leu Phe Pro Pro Lys
210 215 220
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
225 230 235 240
Val Val Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr
245 250 255
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
42
CN 111587118 A 序 列 表 15/18 页
260 265 270
Gln Phe Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His
275 280 285
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
290 295 300
Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln
305 310 315 320
Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met
325 330 335
Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro
340 345 350
Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn
355 360 365
Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu
370 375 380
Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val
385 390 395 400
Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln
405 410 415
Lys Ser Leu Ser Leu Ser Leu Gly Lys
420 425
<210> 21
<211> 425
<212> PRT
<213> Artificial Sequence
<220>
<223> FceRIa ECD-铰链-Fc2
<400> 21
Val Pro Gln Lys Pro Lys Val Ser Leu Asn Pro Pro Trp Asn Arg Ile
1 5 10 15
Phe Lys Gly Glu Asn Val Thr Leu Thr Cys Asn Gly Asn Asn Phe Phe
20 25 30
Glu Val Ser Ser Thr Lys Trp Phe His Asn Gly Ser Leu Ser Glu Glu
35 40 45
Thr Asn Ser Ser Leu Asn Ile Val Asn Ala Lys Phe Glu Asp Ser Gly
50 55 60
Glu Tyr Lys Cys Gln His Gln Gln Val Asn Glu Ser Glu Pro Val Tyr
65 70 75 80
Leu Glu Val Phe Ser Asp Trp Leu Leu Leu Gln Ala Ser Ala Glu Val
43
CN 111587118 A 序 列 表 16/18 页
85 90 95
Val Met Glu Gly Gln Pro Leu Phe Leu Arg Cys His Gly Trp Arg Asn
100 105 110
Trp Asp Val Tyr Lys Val Ile Tyr Tyr Lys Asp Gly Glu Ala Leu Lys
115 120 125
Tyr Trp Tyr Glu Asn His Asn Ile Ser Ile Thr Asn Ala Thr Val Glu
130 135 140
Asp Ser Gly Thr Tyr Tyr Cys Thr Gly Lys Val Trp Gln Leu Asp Tyr
145 150 155 160
Glu Ser Glu Pro Leu Asn Ile Thr Val Ile Lys Ala Pro Arg Glu Lys
165 170 175
Tyr Trp Leu Gln Arg Asn Thr Gly Arg Gly Gly Glu Glu Lys Lys Gly
180 185 190
Ser Lys Glu Lys Glu Glu Gln Glu Glu Arg Glu Thr Lys Thr Pro Glu
195 200 205
Cys Pro Ser His Thr Gln Pro Leu Gly Val Phe Leu Phe Pro Pro Lys
210 215 220
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
225 230 235 240
Val Val Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr
245 250 255
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
260 265 270
Gln Phe Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His
275 280 285
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
290 295 300
Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln
305 310 315 320
Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met
325 330 335
Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro
340 345 350
Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn
355 360 365
Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu
370 375 380
Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val
385 390 395 400
44
CN 111587118 A 序 列 表 17/18 页
Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln
405 410 415
Lys Ser Leu Ser Leu Ser Leu Gly Lys
420 425
<210> 22
<211> 444
<212> PRT
<213> Artificial Sequence
<220>
<223> FceRIa ECD-铰链-Fc3
<400> 22
Val Pro Gln Lys Pro Lys Val Ser Leu Asn Pro Pro Trp Asn Arg Ile
1 5 10 15
Phe Lys Gly Glu Asn Val Thr Leu Thr Cys Asn Gly Asn Asn Phe Phe
20 25 30
Glu Val Ser Ser Thr Lys Trp Phe His Asn Gly Ser Leu Ser Glu Glu
35 40 45
Thr Asn Ser Ser Leu Asn Ile Val Asn Ala Lys Phe Glu Asp Ser Gly
50 55 60
Glu Tyr Lys Cys Gln His Gln Gln Val Asn Glu Ser Glu Pro Val Tyr
65 70 75 80
Leu Glu Val Phe Ser Asp Trp Leu Leu Leu Gln Ala Ser Ala Glu Val
85 90 95
Val Met Glu Gly Gln Pro Leu Phe Leu Arg Cys His Gly Trp Arg Asn
100 105 110
Trp Asp Val Tyr Lys Val Ile Tyr Tyr Lys Asp Gly Glu Ala Leu Lys
115 120 125
Tyr Trp Tyr Glu Asn His Asn Ile Ser Ile Thr Asn Ala Thr Val Glu
130 135 140
Asp Ser Gly Thr Tyr Tyr Cys Thr Gly Lys Val Trp Gln Leu Asp Tyr
145 150 155 160
Glu Ser Glu Pro Leu Asn Ile Thr Val Ile Lys Ala Pro Arg Glu Lys
165 170 175
Tyr Trp Leu Gln Ala Gln Pro Gln Ala Glu Gly Ser Leu Ala Lys Ala
180 185 190
Thr Thr Ala Pro Ala Thr Thr Arg Asn Thr Gly Arg Gly Gly Glu Glu
195 200 205
Lys Lys Gly Ser Lys Glu Lys Glu Glu Gln Glu Glu Arg Glu Thr Lys
210 215 220
45
CN 111587118 A 序 列 表 18/18 页
Thr Pro Glu Cys Pro Ser His Thr Gln Pro Leu Gly Val Phe Leu Phe
225 230 235 240
Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val
245 250 255
Thr Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe
260 265 270
Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro
275 280 285
Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr
290 295 300
Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val
305 310 315 320
Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala
325 330 335
Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln
340 345 350
Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly
355 360 365
Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro
370 375 380
Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser
385 390 395 400
Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg Trp Gln Glu
405 410 415
Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His
420 425 430
Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly Lys
435 440
46
CN 111587118 A 说 明 书 附 图 1/34 页
图1
图2
47
CN 111587118 A 说 明 书 附 图 2/34 页
图3A
48
CN 111587118 A 说 明 书 附 图 3/34 页
图3B
49
CN 111587118 A 说 明 书 附 图 4/34 页
图4
50
CN 111587118 A 说 明 书 附 图 5/34 页
图5
51
CN 111587118 A 说 明 书 附 图 6/34 页
图6
52
CN 111587118 A 说 明 书 附 图 7/34 页
图7
图8
53
CN 111587118 A 说 明 书 附 图 8/34 页
图9
54
CN 111587118 A 说 明 书 附 图 9/34 页
图10
55
CN 111587118 A 说 明 书 附 图 10/34 页
图11
56
CN 111587118 A 说 明 书 附 图 11/34 页
图12
57
CN 111587118 A 说 明 书 附 图 12/34 页
图13
58
CN 111587118 A 说 明 书 附 图 13/34 页
图14
图15A
59
CN 111587118 A 说 明 书 附 图 14/34 页
图15B
60
CN 111587118 A 说 明 书 附 图 15/34 页
图16
61
CN 111587118 A 说 明 书 附 图 16/34 页
图17
图18
62
CN 111587118 A 说 明 书 附 图 17/34 页
图19A
63
CN 111587118 A 说 明 书 附 图 18/34 页
图19B
64
CN 111587118 A 说 明 书 附 图 19/34 页
图20
65
CN 111587118 A 说 明 书 附 图 20/34 页
图21
66
CN 111587118 A 说 明 书 附 图 21/34 页
图22
67
CN 111587118 A 说 明 书 附 图 22/34 页
图23
68
CN 111587118 A 说 明 书 附 图 23/34 页
图24
69
CN 111587118 A 说 明 书 附 图 24/34 页
图25
70
CN 111587118 A 说 明 书 附 图 25/34 页
图26
71
CN 111587118 A 说 明 书 附 图 26/34 页
图27
72
CN 111587118 A 说 明 书 附 图 27/34 页
图28
73
CN 111587118 A 说 明 书 附 图 28/34 页
图29
74
CN 111587118 A 说 明 书 附 图 29/34 页
图30
75
CN 111587118 A 说 明 书 附 图 30/34 页
图31
76
CN 111587118 A 说 明 书 附 图 31/34 页
图32
77
CN 111587118 A 说 明 书 附 图 32/34 页
图33
78
CN 111587118 A 说 明 书 附 图 33/34 页
图34
79
CN 111587118 A 说 明 书 附 图 34/34 页
图35
80













